Clear Sky Science · pl
Wzbogacony przez CAF COL4A6 promuje progresję raka żołądka i przebudowę zrębu mimo odwrotnej korelacji w transkryptomach zbiorczych
Dlaczego otoczenie guza ma znaczenie
Większość osób myśli o raku jako o chorobie złośliwych komórek, ale to badanie pokazuje, że „gleba” wokół guza może być równie ważna jak same komórki nowotworowe. W raku żołądka rusztowanie tkankowe i komórki wspierające otaczające guz mogą albo hamować chorobę, albo sprzyjać jej wzrostowi, szerzeniu się i oporności na leczenie. Badanie ujawnia, jak określone białko strukturalne o nazwie COL4A6 zachowuje się diametralnie inaczej w zależności od miejsca lokalizacji, oraz jak specyficzna grupa komórek podporowych — fibroblasty związane z nowotworem — może zmienić to białko w potężnego wspólnika progresji guza.
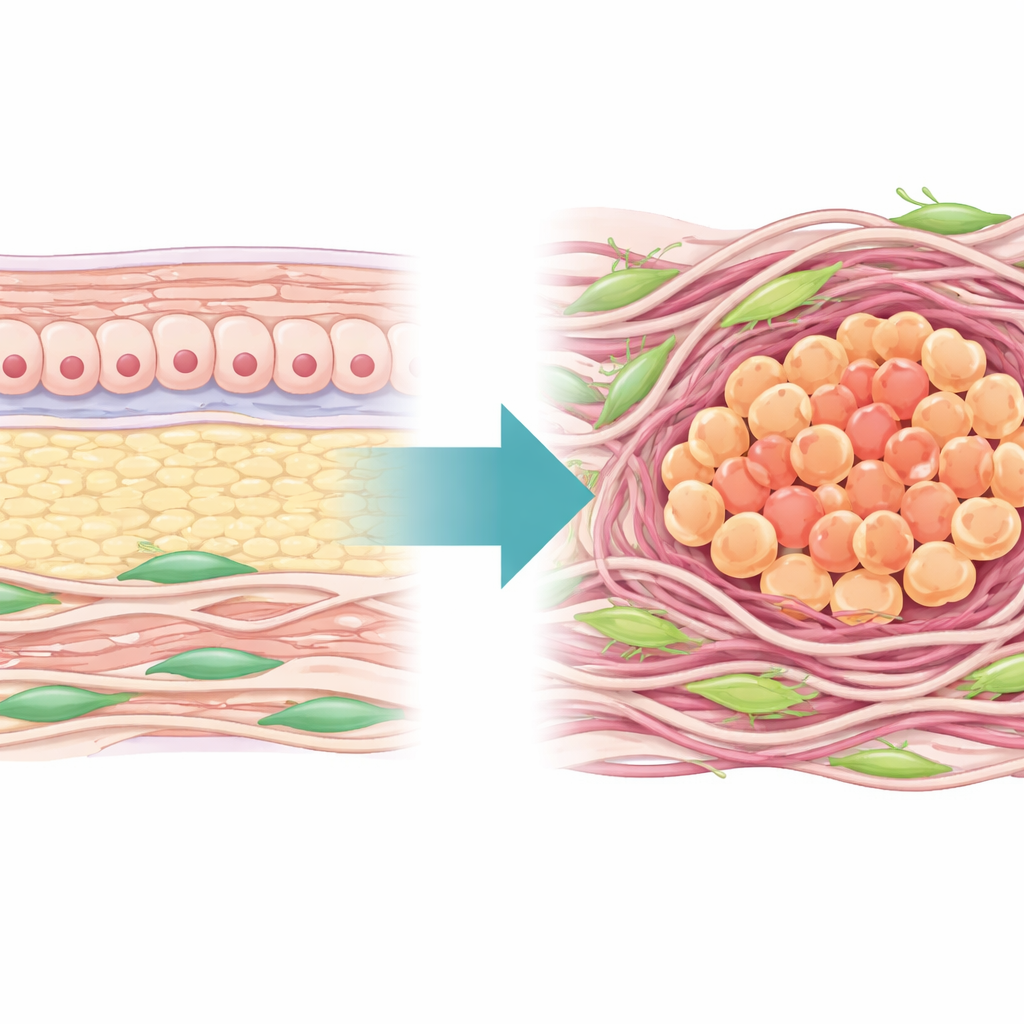
Bliższe spojrzenie na sąsiedztwo guza
Autorzy zaczęli od zmapowania „krajobrazu” macierzy pozakomórkowej — sieci białek i włókien otaczających komórki — w setkach ludzkich guzów żołądka. Stwierdzili, że niemal połowa podstawowych genów macierzy była zmieniona w tkance nowotworowej w porównaniu z przyległą tkanką normalną, potwierdzając, że środowisko fizyczne guzów żołądka jest silnie przebudowane. Wykorzystując te geny, stworzyli Wynik Ryzyka Matrisomu, który wiarygodnie odróżniał tkankę guza od tkanki normalnej i dzielił pacjentów na dwie główne grupy: jedną z gęstą, silnie przebudowaną macierzą i gorszym przeżyciem, oraz drugą z luźniejszą macierzą i lepszymi wynikami. Grupa o wysokiej zawartości macierzy wykazywała również cechy „zimnego” guza pod względem odporności — z wieloma komórkami o działaniu supresyjnym i niewielką liczbą aktywnych limfocytów T — oraz zmniejszoną wrażliwość na standardową chemioterapię.
Białko o rozdwojonej osobowości
Jeden składnik macierzy, COL4A6, wyróżniał się, ponieważ wydawał się zachowywać jak czynnik „ochronny”, gdy badacze analizowali jedynie zbiorcze odczyty ekspresji genów z całych próbek guza. Statystycznie wyższe poziomy genu COL4A6 w tych zbiorczych zestawach danych wiązały się z niższym pozornym ryzykiem, co skłoniło niektórych do przypuszczeń, że może on hamować nowotwór. Jednak w tym badaniu podejrzewano ukryte zjawisko: pomiary zbiorcze mieszają sygnały z wielu typów komórek. Gdy zespół przeanalizował rzeczywiste plastry tkanki guza od pacjentów, odkrył, że białko COL4A6 było w rzeczywistości wyraźnie zwiększone w nowotworach w porównaniu z normalną tkanką żołądka, a włókna kolagenowe stawały się grubsze i liczniejsze w miarę zaawansowania guzów.
Fibroblasty jako ukryci sprawcy
Przy użyciu obrazowania fluorescencyjnego i sekwencjonowania jednokomórkowego badacze ustalili, skąd naprawdę pochodzi COL4A6. Nie były to same komórki nowotworowe, lecz przede wszystkim rodzaj komórek podporowych zwanych fibroblastami związanymi z nowotworem (CAF), ulokowanymi w tkance łącznej guza. Sygnały COL4A6 ściśle pokrywały się z markerem CAF, ujawniając, że to te fibroblasty są głównym źródłem. Wyjaśniało to wcześniejsze nieporozumienie: podczas gdy komórki nabłonkowe nowotworu mogą tracić ekspresję COL4A6 na poziomie genu, pula fibroblastów zwiększa produkcję i odkłada białko w otaczającej macierzy — wzorzec, który pomiary zbiorcze zacierają.
Jak COL4A6 napędza wzrost i rozsiew
Aby sprawdzić, jak COL4A6 pochodzący od CAF wpływa na guzy, zespół hodował komórki raka żołądka razem z kulturami fibroblastów zmodyfikowanymi tak, by produkowały więcej lub mniej COL4A6. Gdy fibroblasty nadprodukowały COL4A6, pobliskie komórki nowotworowe stały się bardziej ruchome i inwazyjne oraz przeszły w bardziej agresywny, zmieniający kształt stan znany jako przejście nabłonkowo-mezenchymalne. U myszy guzy utworzone z udziałem fibroblastów bogatych w COL4A6 rosły większe, miały gęstsze depozyty kolagenu i silne sygnały COL4A6 utkane w zrębie. Jednocześnie COL4A6 wydawał się działać również na same fibroblasty, reorganizując ich wewnętrzne rusztowanie w grube włókna napięcia i zwiększając klasyczne markery aktywacji. W istocie COL4A6 pomagał przekształcać fibroblasty w potężnych przebudowujących, którzy usztywniają tkankę, budują bariery fizyczne i tworzą niszę sprzyjającą inwazji guza oraz oporności na leki.
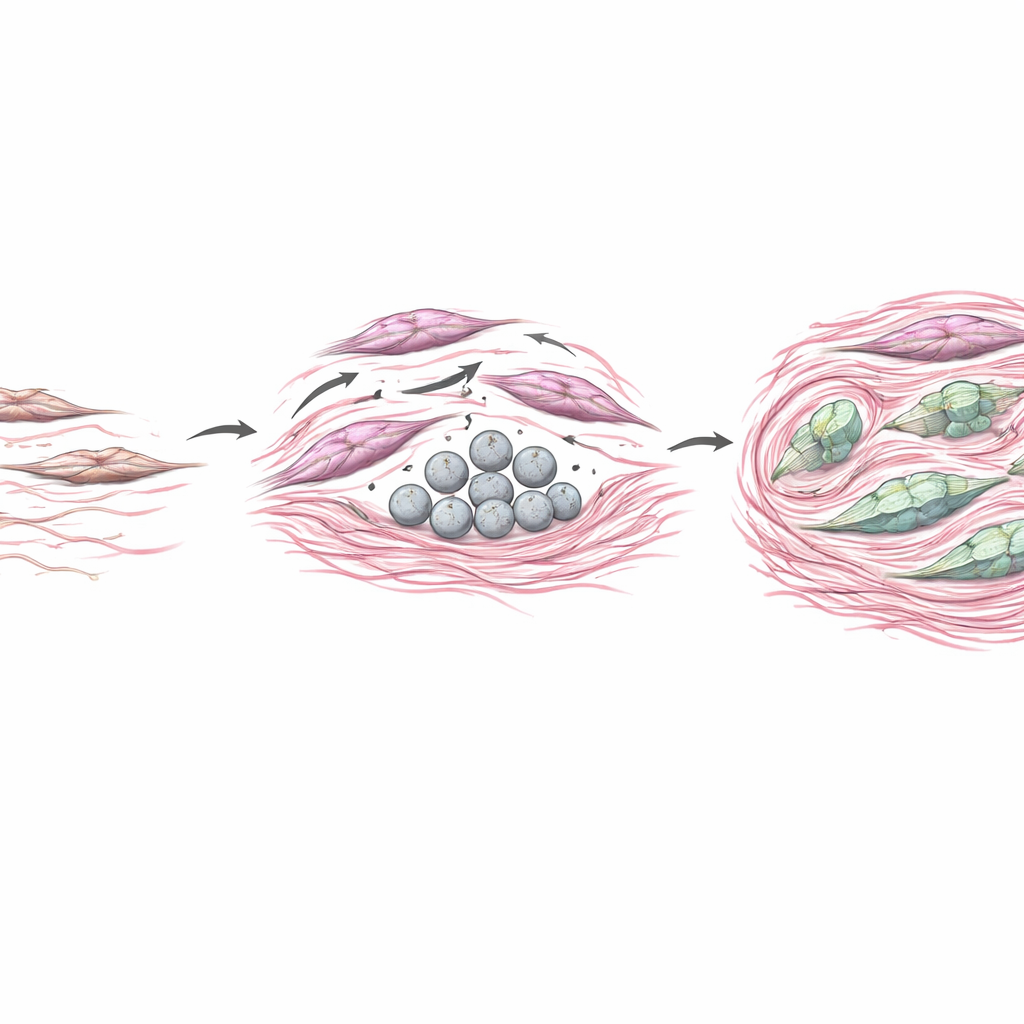
Co to oznacza dla pacjentów
Dla osób niebędących specjalistami główny wniosek jest taki, że ta sama cząsteczka może wyglądać na pomocną lub szkodliwą w zależności od tego, jak i gdzie jest mierzona. COL4A6 może wydawać się „ochronny”, gdy uśrednia się sygnał ze wszystkich komórek w guzie, ale gdy spojrzy się na właściwy przedział, ukazuje się jako kluczowy promotor choroby, produkowany przez aktywowane fibroblasty, które budują gęste, wrogie środowisko. Poprzez zdefiniowanie podtypów guzów opartych na macierzy i ujawnienie osi CAF–COL4A6 jako czynnika napędzającego unikanie układu odpornościowego oraz oporność na chemioterapię, badanie sugeruje nowe sposoby stratafikacji pacjentów z rakiem żołądka i wskazuje zrąb guza jako obiecujący cel. Terapie zakłócające działanie COL4A6 w fibroblastach lub zmiękczające otaczającą macierz mogłyby w przyszłości pomóc przemienić zimne, oporne na leczenie guzy żołądka w guzy bardziej wrażliwe na leki i immunoterapię.
Cytowanie: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Słowa kluczowe: rak żołądka, mikrośrodowisko guza, fibroblasty związane z nowotworem, macierz pozakomórkowa, COL4A6