Clear Sky Science · ar
COL4A6 المعزز بواسطة الخلايا الليفية المرتبطة بالسرطان يعزز تطور سرطان المعدة وإعادة تشكيل النسج الداعمة على الرغم من علاقة عكسية في النسخ الشاملة
لماذا يهم ما يحيط بالورم
يميل معظم الناس إلى اعتبار السرطان مرضًا للخلايا الخارجة عن السيطرة، لكن هذه الدراسة تبين أن «التربة» المحيطة بالورم قد تكون بنفس أهمية الخلايا السرطانية نفسها. في سرطان المعدة، يمكن أن يعمل هيكل النسج وخلايا الدعم المحيطة بالورم إما على إبطاء المرض أو دفعه للنمو والانتشار والمقاومة للعلاج. يكشف هذا البحث كيف يتصرف بروتين بنيوي محدد يدعى COL4A6 بشكل مختلف جداً اعتمادًا على موضعه، وكيف أن مجموعة معينة من خلايا الدعم، وهي الخلايا الليفية المرتبطة بالسرطان، يمكن أن تحول هذا البروتين إلى شريك قوي في تقدم الورم.
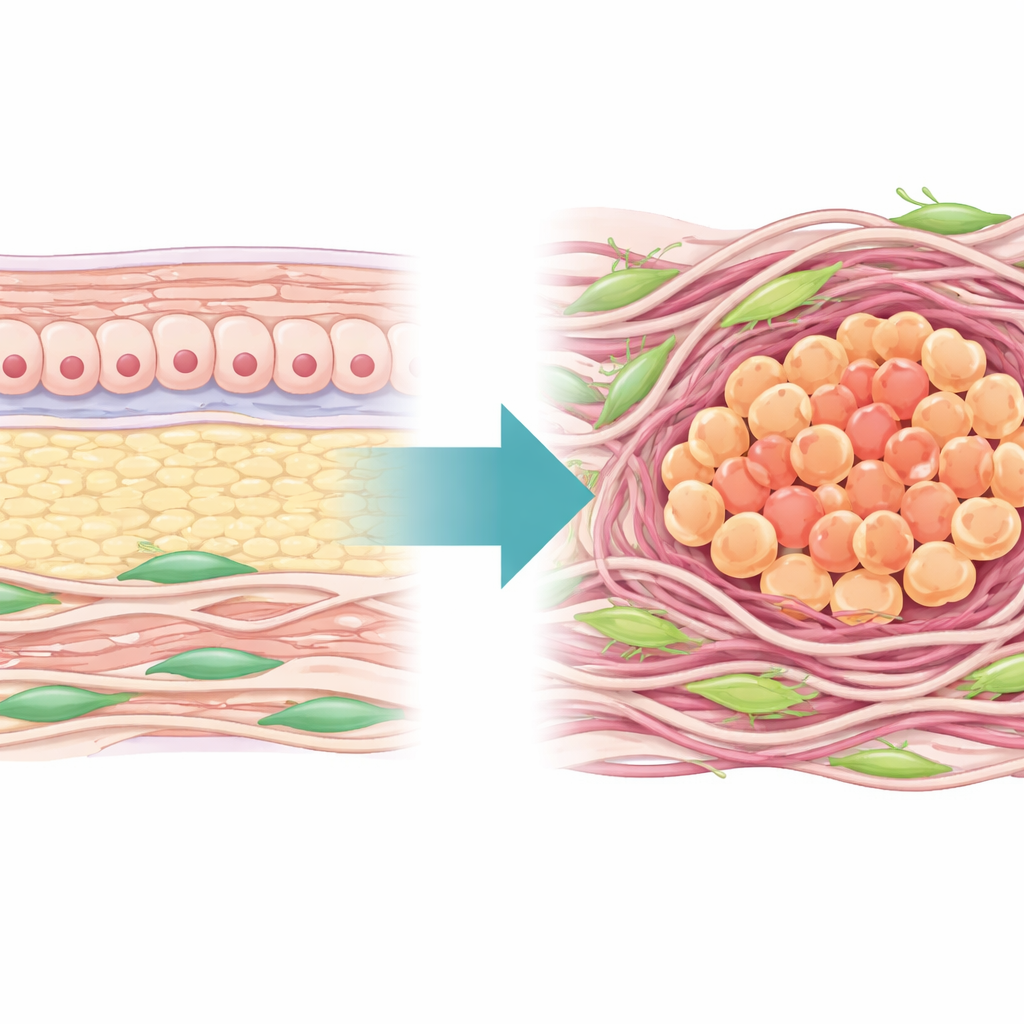
نظرة أقرب إلى حي الورم
بدأ المؤلفون برسم «خريطة» للمصفوفة خارج الخلوية — شبكة البروتينات والألياف المحيطة بالخلايا — في مئات أورام المعدة البشرية. وجدوا أن ما يقرب من نصف الجينات الأساسية للمصفوفة تغيرت في الأنسجة السرطانية مقارنة بالأنسجة الطبيعية المجاورة، مؤكّدين أن البيئة الفيزيائية لأورام المعدة تخضع لإعادة تشكيل كبيرة. وباستخدام هذه الجينات، بنوا مقياسًا لمخاطر المصفوفة (Matrisome Risk Score) يمكنه التمييز بشكل موثوق بين النسيج الورمي والطبيعي وتقسيم المرضى إلى مجموعتين رئيسيتين: إحداهما ذات مصفوفة كثيفة ومعاد تشكيلها بشدة وترتبط ببقاء أسوأ، والأخرى ذات مصفوفة أكثر رخاوة ونتائج أفضل. أظهرت مجموعة المصفوفة العالية أيضًا دلائل على أن الورم محاط ببيئة مناعية «باردة»، مع العديد من الخلايا الكابحة وقلة الخلايا التائية الفاعلة، فضلاً عن حساسية أقل للعلاجات الكيميائية القياسية.
بروتين ذو شخصية منقسمة
برز مكوّن في المصفوفة، COL4A6، لأنه بدا وكأنه يعمل كعامل «حامي» عندما فحص الباحثون قياسات الجينات المجمعة (bulk) من عينات الأورام الكاملة. إحصائيًا، ارتبطت مستويات أعلى من جين COL4A6 في هذه البيانات المجمعة بمخاطر ظاهرية أقل، مما دفع بعض الباحثين لافتراض أنه قد يساعد في تقييد السرطان. لكن هذه الدراسة اشتبهت في وجود منعطف مخفي: القياسات المجمعة تمزج إشارات أنواع خلوية عديدة. عندما فحص الفريق شرائح الأنسجة الورمية الفعلية من المرضى، وجدوا أن بروتين COL4A6 كان بالفعل مرتفعًا بقوة في السرطانات مقارنة بنسيج المعدة الطبيعي، وأن ألياف الكولاجين صارت أكثر سمكًا وأكثر وفرة مع تقدم الأورام.
الخلايا الليفية كسائقين معتمدين
باستخدام التصوير الفلوري وتسلسل الخلية الواحدة، اكتشف الباحثون مصدر COL4A6 الحقيقي. لم تكن الخلايا السرطانية نفسها هي المصدر الرئيسي، بل نوع من خلايا الدعم يُسمى الخلايا الليفية المرتبطة بالسرطان (CAFs) الموجودة في النسج الضامة للورم. تداخلت إشارات COL4A6 ارتباطًا وثيقًا مع علامة مميزة للخلايا الليفية، كاشفة أن هذه الخلايا الليفية كانت المصدر الرئيسي. وهذا يوضح الالتباس السابق: بينما قد تفقد الخلايا الظهارية السرطانية تعبير COL4A6 على مستوى الجين، فإن مقصورة الخلايا الليفية تزيد من إنتاجه وتودعه في المصفوفة المحيطة، وهو نمط تُطمسه اختبارات البيانات المجمعة.
كيف يغذي COL4A6 النمو والانتشار
لاختبار أثر COL4A6 المشتق من الخلايا الليفية على الأورام، رَبّى الفريق خلايا سرطان المعدة مع ثقافات خلايا ليفية مهندَسة لإنتاج كميات أكبر من COL4A6 أو أقل منها. عندما فرطت الخلايا الليفية في إنتاج COL4A6، أصبحت الخلايا السرطانية المجاورة أكثر حركة وغزوًا، وتحولت إلى حالة أكثر عدوانية ومتقلبة الشكل تعرف بالانتقال الظهاري-اللحائي (epithelial–mesenchymal transition). في الفئران، نمت الأورام التي تشكلت مع خلايا ليفية غنية بـCOL4A6 أكبر حجمًا، وكان لديها رواسب كولاجين أكثر كثافة، وأظهرت إشارات COL4A6 قوية منسوجة عبر النسج الداعمة. في الوقت نفسه، بدا أن COL4A6 يؤثر رجعيًا على الخلايا الليفية نفسها، معيدًا تنظيم هياكلها الداخلية إلى ألياف إجهاد سميكة ومعززًا علامات التنشيط الكلاسيكية. في الجوهر، ساعد COL4A6 في تحويل الخلايا الليفية إلى معدّلين أقوياء يشددون النسيج، ويبنون حواجز فيزيائية، ويخلقون موئلًا يدعم غزو الورم ومقاومة الأدوية.
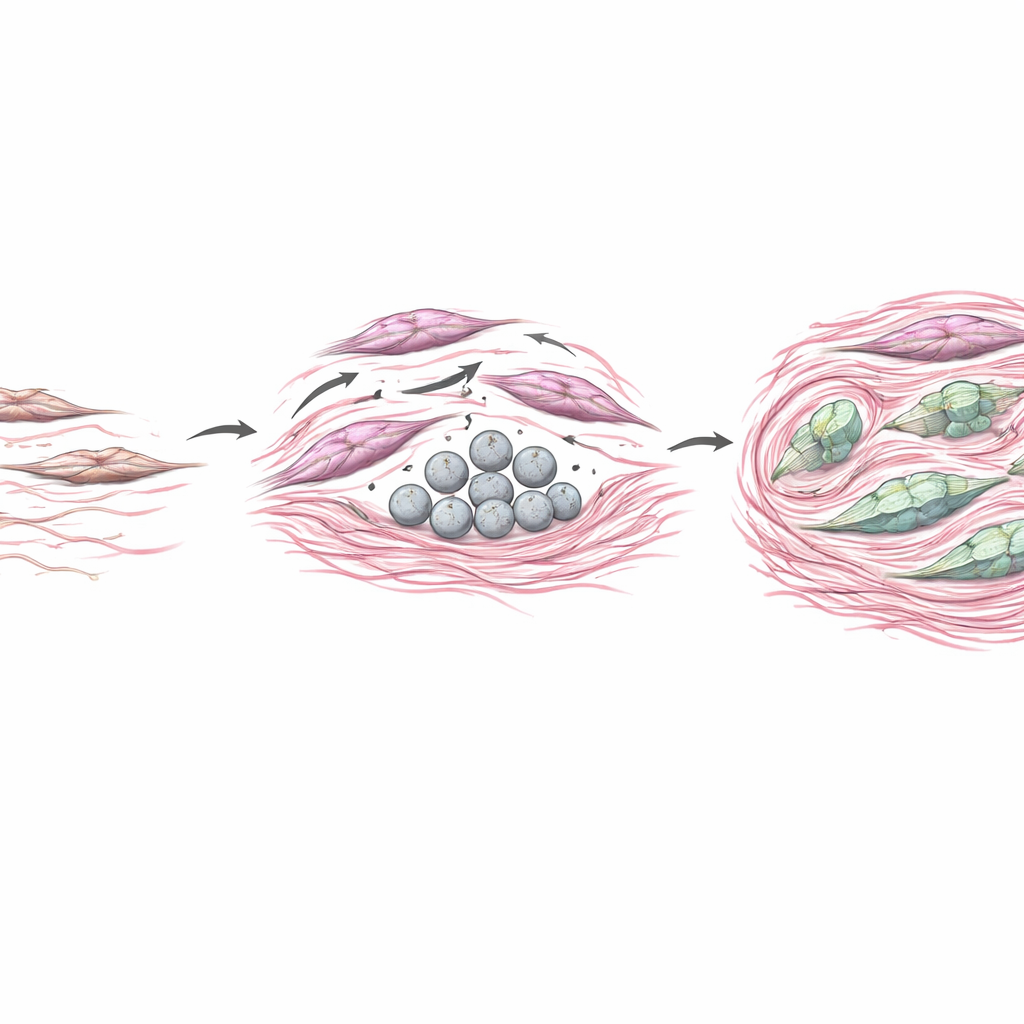
ماذا يعني هذا للمرضى
للغير مختصين، الرسالة الرئيسية هي أن نفس الجزيء يمكن أن يبدو مفيدًا أو مضرًا اعتمادًا على كيفية وموضع قياسه. قد يبدو COL4A6 «حاميًا» عند أخذه كمعدل عبر جميع خلايا الورم، لكن عند النظر إليه في المقصورة الصحيحة يظهر كعامل رئيسي يروّج للمرض، ينتجه الخلايا الليفية المنشّطة التي تبني بيئة كثيفة وعدائية. من خلال تعريف أنواع الأورام بناءً على المصفوفة وكشف محور الخلايا الليفية–COL4A6 كدافع للتهرب المناعي ومقاومة العلاج الكيميائي، تقترح الدراسة طرقًا جديدة لتصنيف مرضى سرطان المعدة وتسلط الضوء على النسج الداعمة للورم كهدف واعد. قد تساعد العلاجات التي تعطل COL4A6 في الخلايا الليفية أو تلطف المصفوفة المحيطة يومًا ما على تحويل أورام المعدة الباردة المقاومة للعلاج إلى أورام أكثر استجابة للأدوية والمناعية.
الاستشهاد: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
الكلمات المفتاحية: سرطان المعدة, البيئة المجهرية للورم, الخلايا الليفية المرتبطة بالسرطان, المصفوفة خارج الخلوية, COL4A6