Clear Sky Science · nl
CAF-verrijkte COL4A6 bevordert de progressie van maagkanker en remodelering van het stroma ondanks een omgekeerde associatie in bulk-transcriptomen
Waarom de omgeving van de tumor ertoe doet
De meeste mensen zien kanker als een ziekte van woekerende cellen, maar deze studie laat zien dat de “grond” rond de tumor net zo belangrijk kan zijn als de kankercellen zelf. Bij maagkanker kunnen het weefsel‑skelet en de ondersteunende cellen rondom de tumor de ziekte remmen of juist aanzetten tot groei, uitzaaiing en therapieresistentie. Dit onderzoek onthult hoe een bepaald skeleteiwit, COL4A6, heel verschillend kan functioneren afhankelijk van waar het zich bevindt, en hoe een specifieke groep ondersteunende cellen, kanker‑geassocieerde fibroblasten, dit eiwit kunnen omzetten in een krachtige medeplichtige bij tumorprogressie.
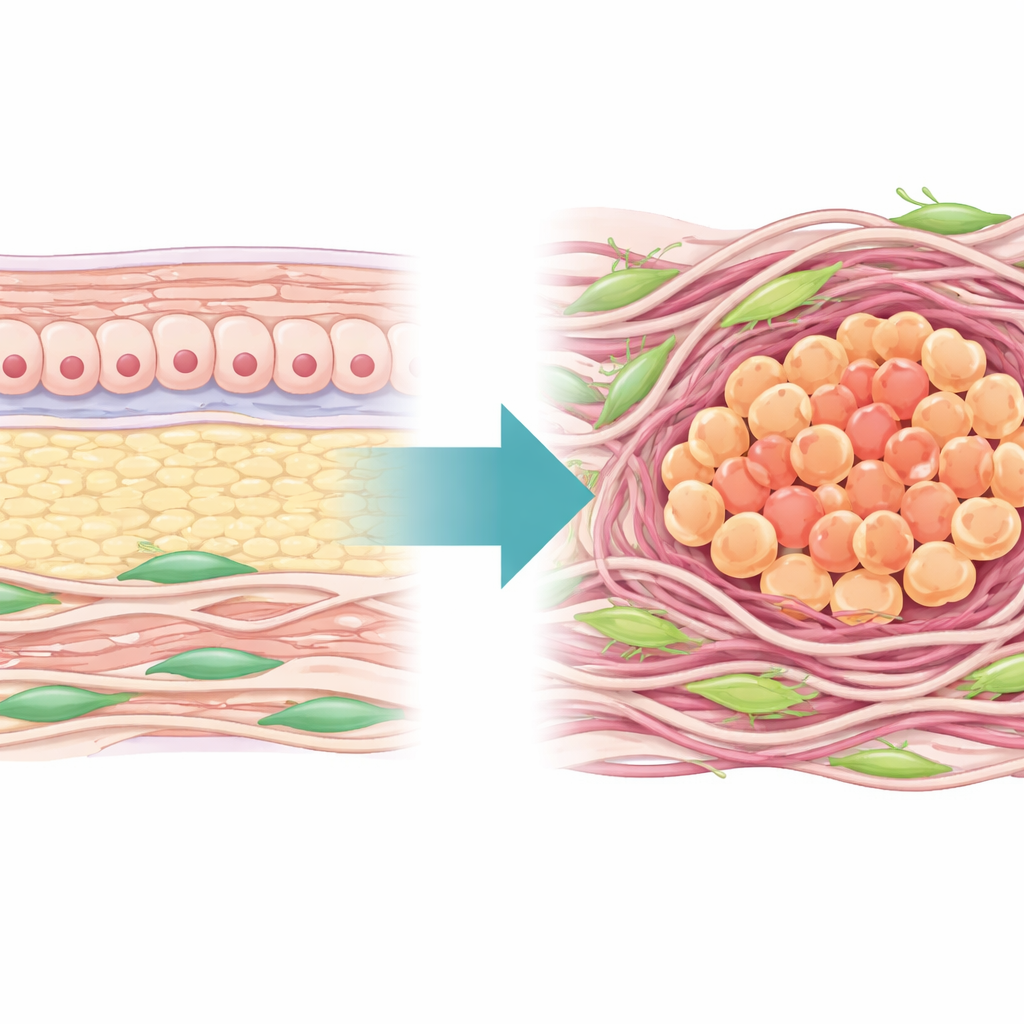
Een nadere blik op de buurt rond de tumor
De auteurs begonnen met het in kaart brengen van het “landschap” van de extracellulaire matrix — het web van eiwitten en vezels dat cellen omgeeft — in honderden menselijke maagtumoren. Ze vonden dat bijna de helft van de kernmatrixgenen veranderd was in kankergezwellen vergeleken met aangrenzend normaal weefsel, wat bevestigt dat de fysieke omgeving van maagtumoren sterk wordt heringericht. Met deze genen bouwden ze een Matrisome Risk Score die betrouwbaar tumorweefsel van normaal weefsel kon onderscheiden en patiënten in twee hoofdgroepen verdeelde: één met een dichte, sterk geremodelde matrix en slechtere overleving, en een andere met een lossere matrix en betere uitkomsten. De groep met hoge matrixwaarden toonde ook kenmerken van een immuuncold tumor, met veel remmende cellen en weinig actieve T‑cellen, en een verminderde gevoeligheid voor standaardchemotherapie.
Een eiwit met een gespleten persoonlijkheid
Één matrixcomponent, COL4A6, viel op omdat het in bulk‑genexpressiegegevens leken te functioneren als een “beschermende” factor. Statistisch werden hogere COL4A6‑genniveaus in deze bulkdatasets geassocieerd met een lager ogenschijnlijk risico, wat sommige onderzoekers deed vermoeden dat het kanker zou kunnen remmen. Deze studie vermoedde echter een verborgen verklaring: bulkmetingen mengen signalen van veel celtypen. Toen het team echte tumorsecties van patiënten onderzocht, vonden ze dat COL4A6‑eiwit feitelijk sterk verhoogd was in kankers vergeleken met normaal maagweefsel, en dat collagene vezels dikker en talrijker werden naarmate tumoren vorderden.
Fibroblasten als verborgen aanjagers
Met fluorescentiebeeldvorming en single‑cell sequencing ontdekten de onderzoekers waar COL4A6 werkelijk vandaan kwam. Het waren niet de kankercellen zelf, maar primair een type ondersteunende cel genoemd kanker‑geassocieerde fibroblasten (CAF’s), genesteld in het bindweefsel van de tumor. COL4A6‑signalen vielen nauw samen met een CAF‑marker, wat onthulde dat deze fibroblasten de voornaamste bron waren. Dit verklaarde de eerdere verwarring: terwijl kankerepitheelcellen op genniveau mogelijk minder COL4A6 tot expressie brengen, verhoogt het fibroblastische compartiment de productie en deponeert het eiwit in de omliggende matrix — een patroon dat bulktesten samenvoegen en verdoezelen.
Hoe COL4A6 groei en verspreiding aanjaagt
Om te testen hoe door CAF’s geproduceerde COL4A6 tumoren beïnvloedt, kweekte het team maagkankercellen samen met fibroblastcultures die zodanig waren gemodificeerd dat ze meer of minder COL4A6 produceerden. Wanneer fibroblasten te veel COL4A6 aanmaakten, werden naburige kankercellen mobieler en invasiever, en schakelden ze over op een agressievere, van vorm veranderende toestand bekend als epitheliaal‑mesenchymale transitie. In muismodellen vormden tumoren met COL4A6‑rijke fibroblasten grotere gezwellen, hadden ze dichtere collageenafzettingen en toonden ze sterke COL4A6‑signalen verweven door het stroma. Tegelijk leek COL4A6 ook op de fibroblasten zelf terug te werken, hun interne skelet te reorganiseren tot dikke stressvezels en klassieke activatiemarkers te verhogen. In wezen hielp COL4A6 fibroblasten om te zetten in krachtige remodelleurs die het weefsel verstevigen, fysieke barrières opbouwen en een niche creëren die tumorinvasie en medicijnresistentie ondersteunt.
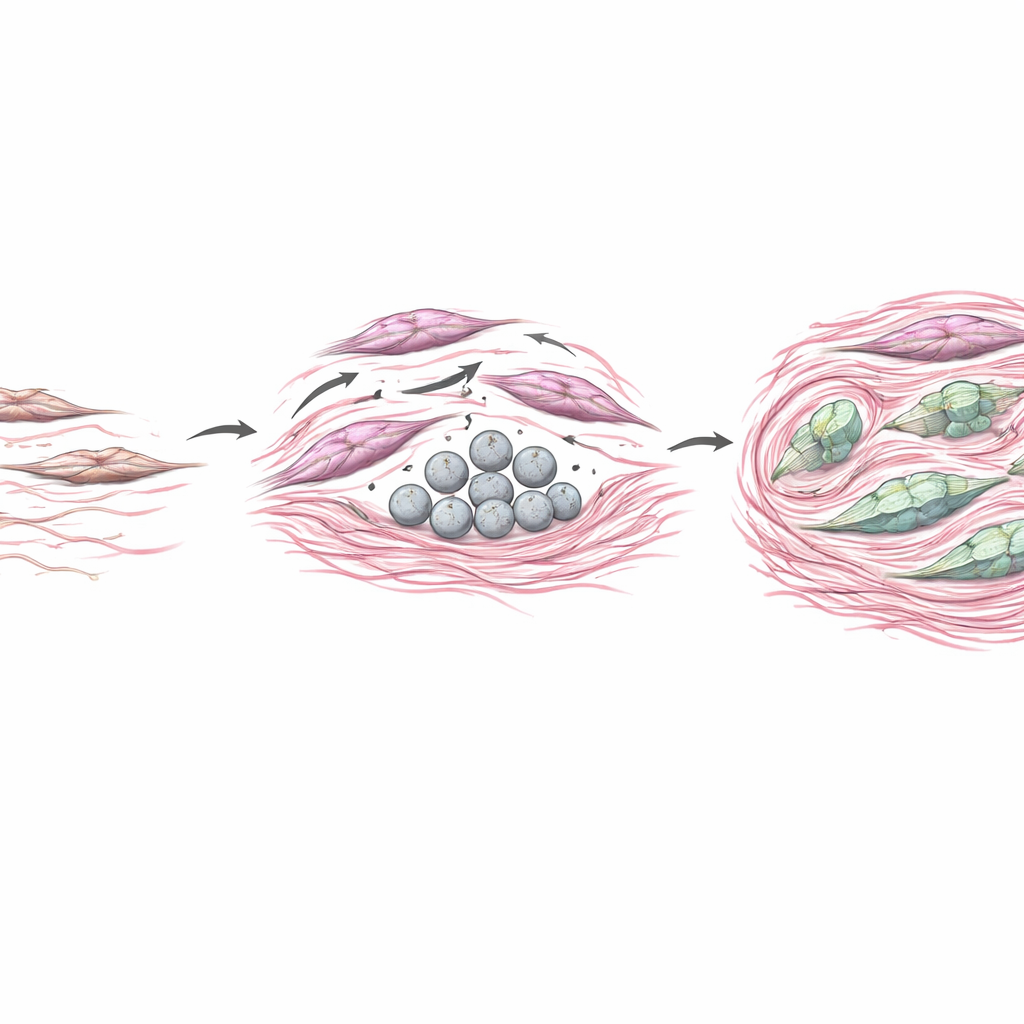
Wat dit betekent voor patiënten
Voor niet‑specialisten is de kernboodschap dat hetzelfde molecuul behulpzaam of schadelijk kan lijken, afhankelijk van hoe en waar het wordt gemeten. COL4A6 kan “beschermend” lijken wanneer het over alle cellen in een tumor wordt gemiddeld, maar wanneer het in het juiste compartiment wordt bekeken, blijkt het een belangrijke bevorderaar van ziekte te zijn — geproduceerd door geactiveerde fibroblasten die een dichte, vijandige omgeving opbouwen. Door matrixgebaseerde tumortypes te definiëren en deze CAF–COL4A6‑as bloot te leggen als aanjager van immuunontwijking en chemotherapie‑resistentie, suggereert de studie nieuwe manieren om maagkankerpatiënten te stratificeren en benadrukt het tumorstroma als een veelbelovend doelwit. Therapieën die COL4A6 in fibroblasten verstoren of de omliggende matrix verzachten, zouden op termijn kunnen helpen om koude, therapieresistente maagtumoren om te zetten in tumoren die beter reageren op medicijnen en immunotherapie.
Bronvermelding: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Trefwoorden: maagkanker, tumormicro‑omgeving, kanker-geassocieerde fibroblasten, extracellulaire matrix, COL4A6