Clear Sky Science · zh
边界引导的细胞排列驱动小鼠上胚层成熟
组织如何找到形状
在小鼠胚胎出现任何可识别形态之前,其细胞首先必须决定如何排列以及在哪里开凿第一个内部腔。本文探讨了一个看似简单但意义重大的问题:一个无明显特征的细胞球体如何自组织成一个有序结构,随后能够构建器官和体轴?通过三维观察早期小鼠胚胎并将生物学与物理学相结合,作者揭示了组织边缘如何悄然编排这一转变。
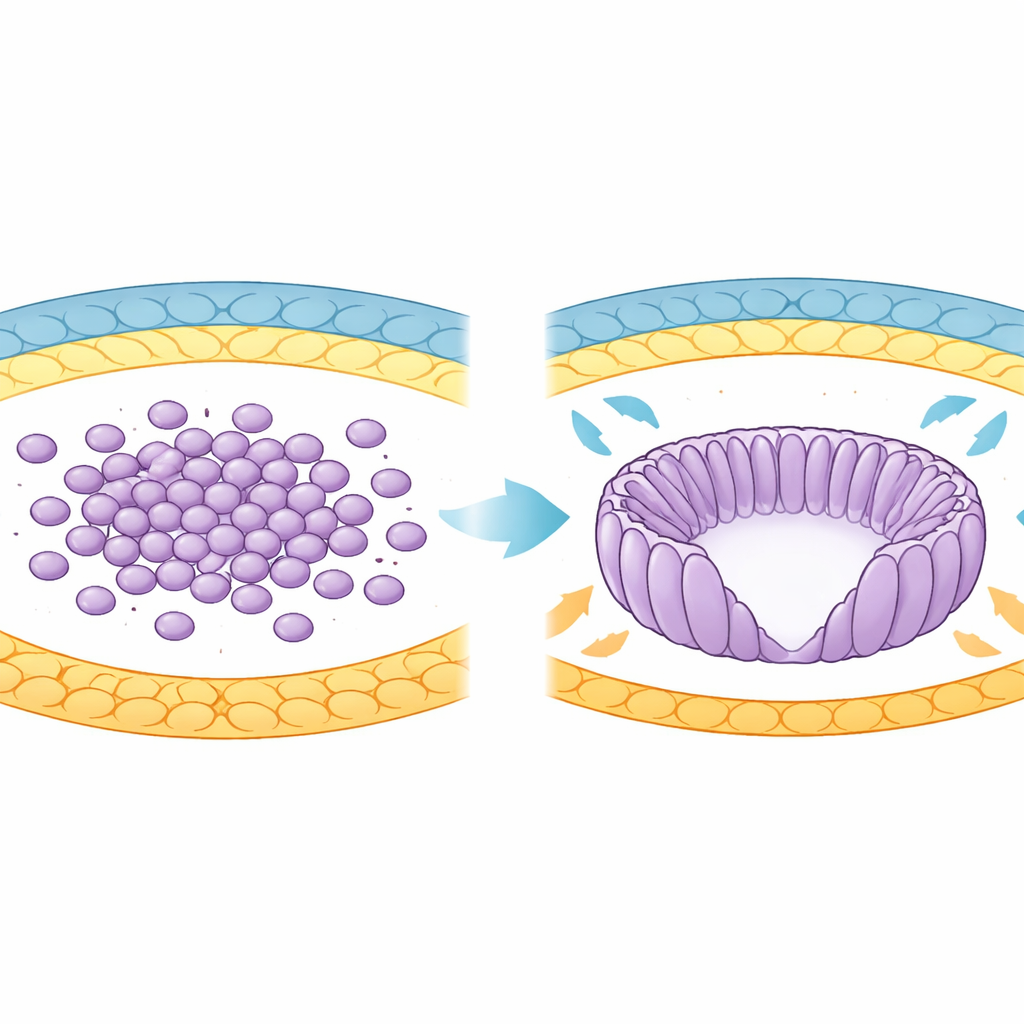
从细胞团到有序杯状结构
在早期发育中,小鼠未来的身体来源于一组称为上胚层的细胞。起初这些细胞在囊胚内呈圆形且松散排列。当胚胎植入子宫时,上胚层重塑为一种称为卵圆柱的杯状结构。在这一转变过程中,细胞拉伸成细长形态,像车轮的辐条一样排列,并包围一个称为原羊膜腔的中心腔。作者使用先进的三维成像和计算分析,追踪了特定发育天数之间数千个细胞随形状变化的过程,发现相邻细胞取向相似度逐步增加。
边缘与分界面的力量
上胚层并非孤立存在。它被两种不同的组织包裹,形成明确的边界:下方将成为内胚层脏层,和上方将成为额外胚外胚层。研究显示,上胚层细胞逐渐在接触内胚层脏层的一侧时取向垂直,而在接触额外胚外胚层的一侧时取向则平行。这意味着当上胚层接触不同邻居时,细胞会采用不同的优选方向。当研究者绘制整个胚胎的细胞取向图时,发现对齐在这些边界附近总是最强,而在中心较弱。该模式表明,组织的边缘像导轨一样引导细胞指向,最终塑造整体结构。
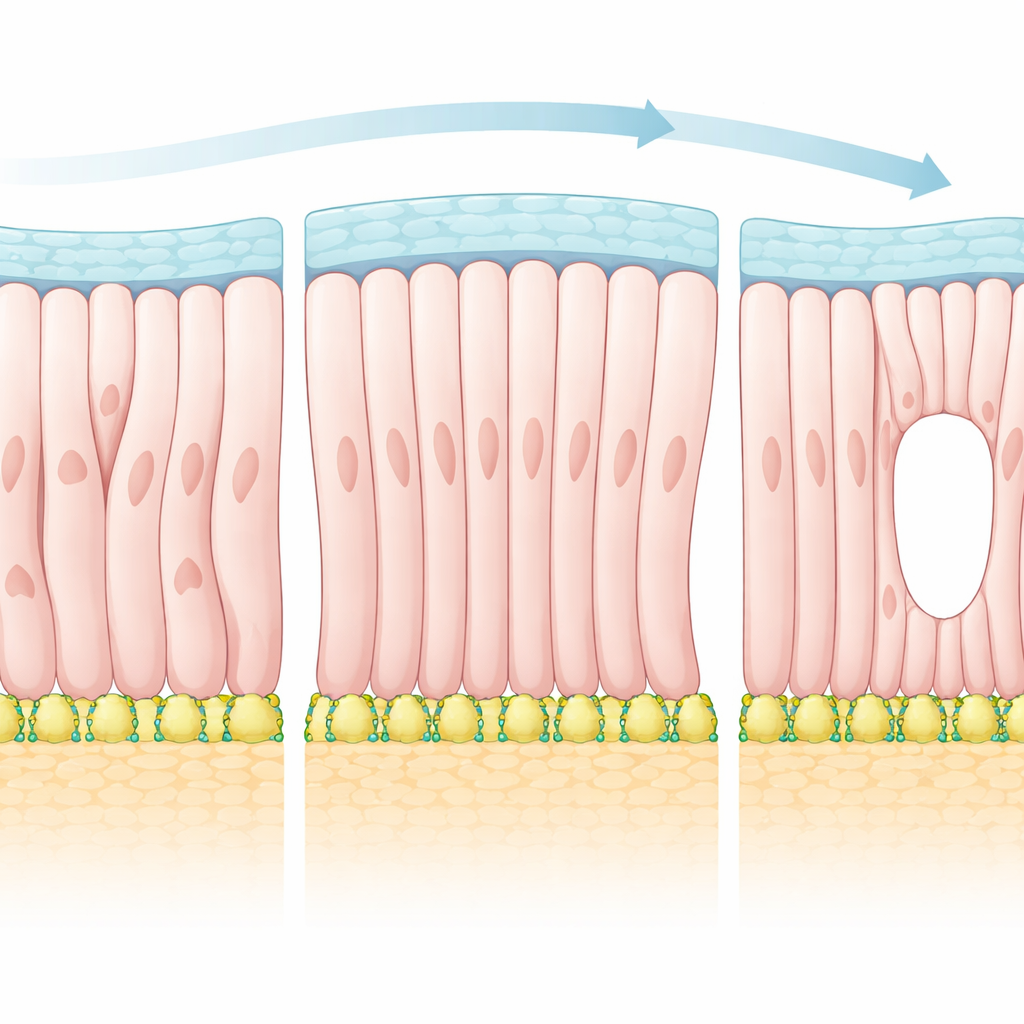
借鉴液晶的理念
为了解释这些观察结果,作者转向了更常用于描述显示器中液晶的框架。在此类材料中,杆状分子往往相互排列,但其确切模式可以受到限制它们的表面的强烈影响。团队将上胚层细胞视为极性“粒子”,它们既倾向与邻居对齐,也倾向与周围边界强加的方向一致。利用该理论,作者预测随着边界影响增强,组织应发生向更有序状态的转变,并在排列场中产生特殊的扰动点——所谓的拓扑缺陷。在胚胎中,这些缺陷对应于细胞顶端趋于汇聚之处,也是未来腔首次打开的位置。
底部边缘的分子锚点
在分子层面,是什么赋予内胚层脏层边界如此强的影响力?作者结合单细胞基因数据和蛋白染色显示,下方的这个边界富集了特定的细胞外基质成分,尤其是层粘连蛋白(laminin),以及其细胞表面配对分子的活性形式整合素β1。二者共同像微小的分子锚点一样附着在上胚层细胞的基底面。随着时间推移,在该边界处层粘连蛋白—整合素粘附增强,细胞排列变得更为显著并形成稳健的模式。在计算机模拟中,削弱这种锚定会抹去有序模式,暗示这些分子对于组织“感知”并响应其边缘至关重要。
当锚点失效时,形状与信号都受损
为直接检验这一点,研究者分析了缺失层粘连蛋白γ1或整合素β1的胚胎。在这些突变体中,上胚层细胞不再垂直指向内胚层脏层边界,而是像在上部边界附近那样呈切向排列。组织失去了典型的放射状对齐,顶端表面的花簇状集群未能正常形成,腔启动位置被扰乱。然而细胞伸长的总体程度仍然增加,表明主要缺陷在于细胞的取向而非其伸展能力。在另一种处理下,酶学方法削弱下方基质会降低ERK信号通路的活性——该通路对细胞生长与分化很重要——这表明正确的组织图案化有助于触发驱动上胚层成熟的分子程序。
这对构建体轴有何意义
简而言之,这项研究表明早期胚胎细胞的排列并非随机;它由边界差异引导,尤其是内胚层脏层侧的层粘连蛋白—整合素粘附。这种由边界引导的对齐足以解释第一个腔体出现的位置,以及ERK等信号如何被激活以推动胚胎发育。对非专业读者来说,关键信息是边缘并非被动的分界:它们是积极的组织者,帮助一团无形状的细胞变成有序的、功能性的组织,为身体其余部分铺设蓝图。
引用: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
关键词: 胚胎发育, 细胞排列, 细胞外基质, 组织图案化, 腔形成