Clear Sky Science · es
La alineación celular guiada por límites impulsa la maduración del epiblasto en ratón
Cómo los tejidos encuentran su forma
Antes de que un embrión de ratón adquiera una forma reconocible, sus células deben decidir primero cómo alinearse y dónde tallar la primera cavidad interna. Este artículo explora una pregunta aparentemente sencilla con grandes implicaciones: ¿cómo se autoorganiza una bola de células aparentemente sin rasgos en una estructura bien ordenada capaz luego de construir órganos y ejes corporales? Al observar embriones de ratón tempranos en tres dimensiones y combinar biología con física, los autores desvelan cómo los bordes de un tejido coreografían silenciosamente esta transformación.
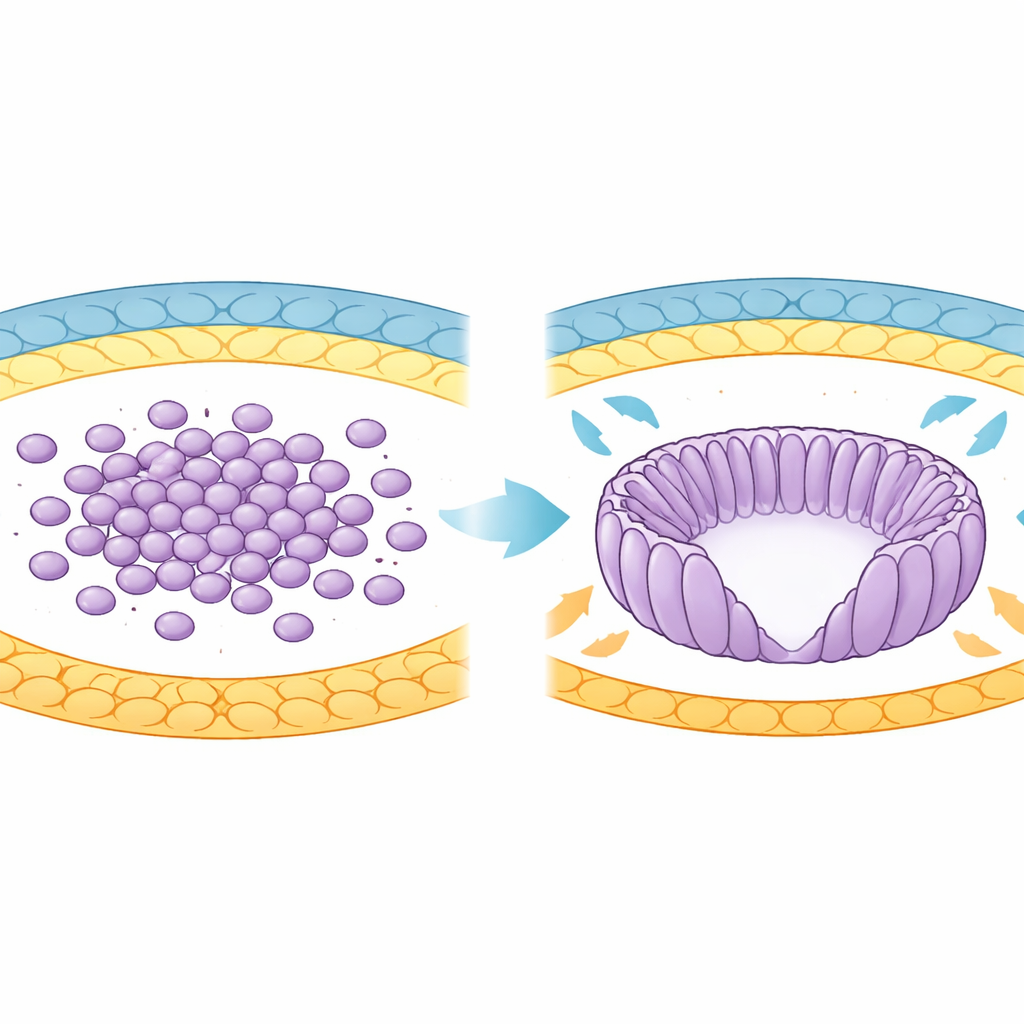
Del racimo celular a la copa organizada
En el desarrollo temprano, el futuro cuerpo del ratón procede de un grupo de células llamado epiblasto. Inicialmente estas células son redondas y están poco organizadas dentro del blastocisto. Cuando el embrión se implanta en el útero, el epiblasto se remodela en una estructura en forma de copa llamada cilindro embrionario. Durante esta transición, las células se estiran hasta adoptar formas alargadas, se alinean como radios de una rueda y rodean una cavidad central conocida como cavidad proamniótica. Los autores utilizaron imágenes 3D avanzadas y análisis computacionales para seguir miles de células mientras este cambio de forma se producía entre días de desarrollo específicos, revelando un aumento progresivo en la concordancia de orientación entre células vecinas.
El poder de los bordes y las fronteras
El epiblasto no existe de forma aislada. Está envuelto por dos tejidos diferentes que forman fronteras distintas: uno que se convertirá en el endodermo visceral por debajo y otro que dará lugar al ectodermo extraembrionario por encima. El estudio muestra que las células del epiblasto gradualmente se orientan perpendiculares al lado del endodermo visceral pero paralelas al lado extraembrionario. Esto significa que donde el epiblasto toca diferentes vecinos, las células adoptan direcciones preferentes distintas. Cuando los investigadores cartografiaron las orientaciones celulares en embriones enteros, hallaron que la alineación era siempre más fuerte cerca de estas fronteras y más débil en el centro. Este patrón sugiere que los bordes del tejido actúan como raíles guía, indicando a las células hacia dónde apuntar y, en última instancia, moldeando toda la estructura.
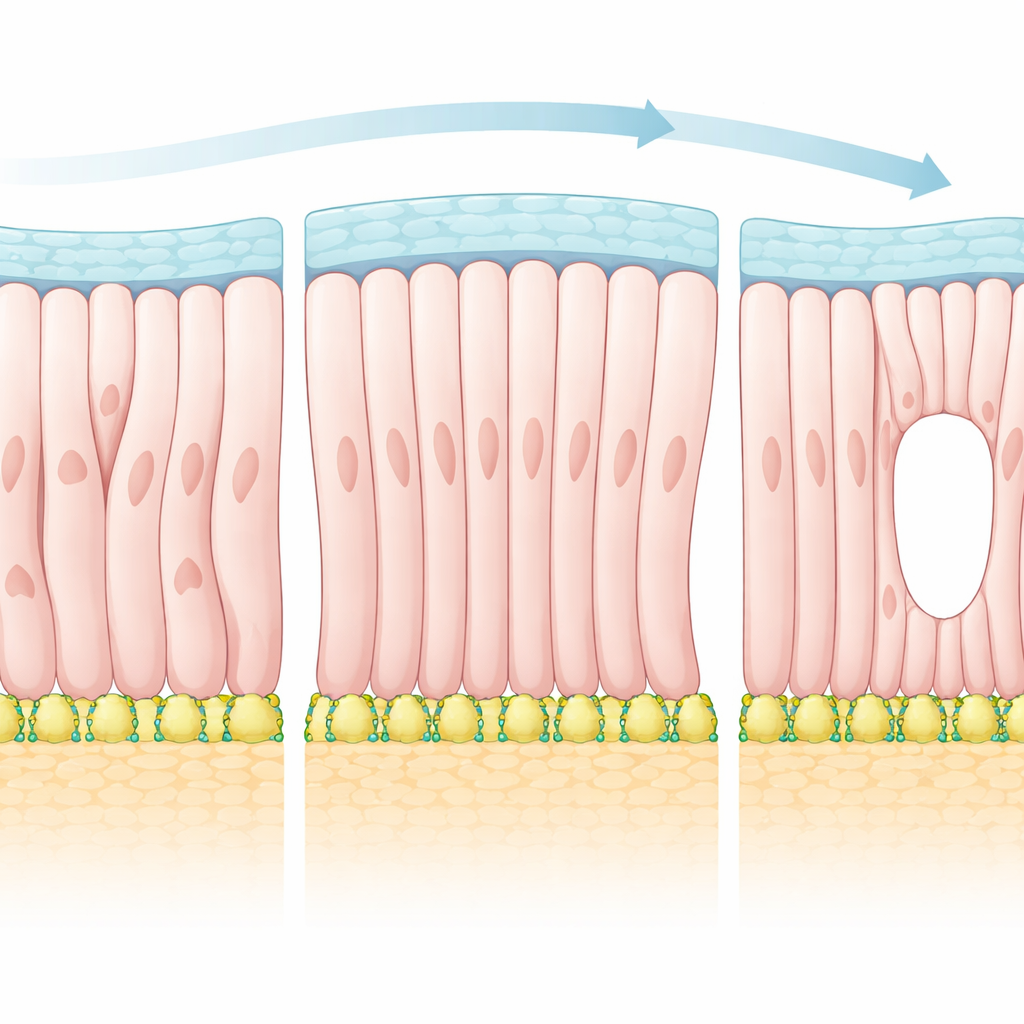
Tomando ideas de los cristales líquidos
Para explicar estas observaciones, los autores recurrieron a un marco teórico más usado para describir cristales líquidos en pantallas. En esos materiales, las moléculas en forma de varilla tienden a alinearse entre sí, pero su patrón exacto puede verse fuertemente influido por las superficies que las confinan. El equipo trató a las células del epiblasto como “partículas” polares que prefieren alinearse tanto con sus vecinas como con las direcciones impuestas por los límites circundantes. Usando esta teoría, predijeron que a medida que la influencia de los bordes se fortalece, el tejido debería sufrir una transición hacia un estado más ordenado que contenga puntos especiales de interrupción del campo de alineación—los llamados defectos topológicos. En el embrión, estos defectos corresponden a lugares donde convergen los lados apicales de las células y donde la futura cavidad se abre por primera vez.
Anclas moleculares en el borde inferior
¿Qué, a nivel molecular, confiere al límite del endodermo visceral su fuerte influencia? Los autores combinaron datos genéticos a nivel de célula única y tinción proteica para mostrar que este límite inferior se enriquece en componentes específicos de la matriz extracelular, sobre todo laminina, y en la forma activa de su pareja en la superficie celular, la integrina β1. Juntas, estas actúan como pequeñas anclas moleculares para el lado basal de las células del epiblasto. A medida que la adhesión laminina–integrina se intensifica con el tiempo en este límite, la alineación celular se hace más pronunciada y emerge un patrón robusto. En simulaciones por ordenador, debilitar este anclaje borraba el patrón ordenado, lo que sugiere que estas moléculas son esenciales para que el tejido «sienta» y responda a su borde.
Cuando las anclas fallan, la forma y las señales flaquean
Para probar esto directamente, los investigadores examinaron embriones carentes de laminina γ1 o de integrina β1. En estos mutantes, las células del epiblasto ya no apuntaban perpendicularmente hacia el límite del endodermo visceral, sino que yacían de forma tangencial, como ocurre cerca del límite superior. El tejido perdió su característica alineación radial, los racimos en forma de roseta de superficies apicales no se formaron correctamente y los sitios de iniciación de la luz se vieron alterados. Sin embargo, la magnitud básica del alargamiento celular siguió aumentando, lo que indica que el defecto principal residía en cómo se orientaban las células más que en su capacidad de estirarse. En una manipulación separada, debilitar enzimáticamente la matriz en el borde inferior redujo la actividad de ERK, una vía de señalización importante para el crecimiento y la diferenciación celular, lo que sugiere que el patrónado tisular correcto ayuda a desencadenar los programas moleculares que impulsan la maduración del epiblasto.
Por qué esto importa para construir cuerpos
En términos simples, el estudio muestra que la forma en que las células embrionarias tempranas se alinean no es aleatoria; está dirigida por diferencias en sus fronteras, especialmente por la adhesión laminina–integrina en el lado del endodermo visceral. Esta alineación guiada por límites bastaría para explicar dónde aparece la primera cavidad y cómo se activan señales como ERK para avanzar el embrión en el desarrollo. Para un lector general, el mensaje clave es que los bordes no son meras fronteras pasivas: son organizadores activos que ayudan a que un amasijo informe de células se convierta en un tejido ordenado y funcional, trazando el plano para el resto del organismo.
Cita: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Palabras clave: desarrollo embrionario, alineación celular, matriz extracelular, patronización tisular, formación de luz