Clear Sky Science · fr
L’alignement cellulaire guidé par les bords pilote la maturation de l’épiblaste chez la souris
Comment les tissus trouvent leur forme
Avant qu’un embryon de souris n’adopte une forme reconnaissable, ses cellules doivent d’abord décider comment s’aligner et où creuser la toute première cavité interne. Cet article explore une question apparemment simple mais aux grandes implications : comment une boule de cellules sans caractéristiques apparentes s’auto-organise-t-elle en une structure ordonnée capable, ensuite, de construire des organes et des axes corporels ? En observant des embryons de souris précoces en trois dimensions et en mêlant biologie et physique, les auteurs révèlent comment les bords d’un tissu orchestrent discrètement cette transformation.
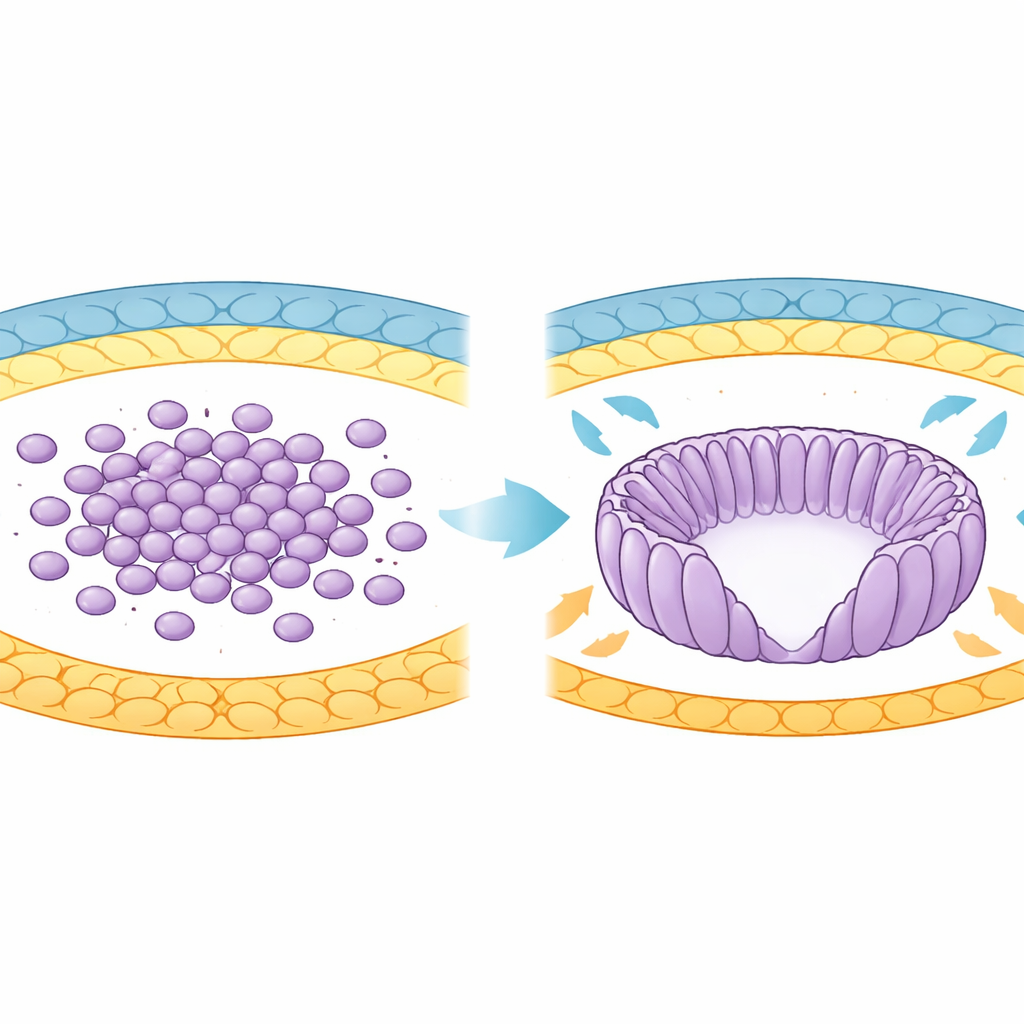
D’un amas cellulaire à une coupe organisée
Au tout début du développement, le futur corps de la souris provient d’un groupe de cellules appelé épiblaste. À l’origine, ces cellules sont rondes et faiblement organisées à l’intérieur du blastocyste. Lors de l’implantation dans l’utérus, l’épiblaste se remodele en une structure en forme de coupe appelée cylindre embryonnaire. Pendant cette transition, les cellules s’allongent, se disposent en forme de rayon, et entourent une cavité centrale connue sous le nom de cavité proamniotique. Les auteurs ont utilisé des imageries 3D avancées et des analyses computationnelles pour suivre des milliers de cellules pendant ce changement de forme entre des stades de développement précis, révélant une augmentation progressive de la similitude d’orientation entre cellules voisines.
La puissance des bords et des frontières
L’épiblaste n’existe pas isolément. Il est entouré par deux tissus différents qui forment des frontières distinctes : l’un qui deviendra l’endoderme viscéral en dessous, et l’autre qui deviendra l’ectoderme extraembryonnaire au-dessus. L’étude montre que les cellules de l’épiblaste s’orientent progressivement perpendiculairement du côté de l’endoderme viscéral mais parallèlement du côté extraembryonnaire. Autrement dit, là où l’épiblaste touche des voisins différents, les cellules adoptent des directions préférentielles différentes. Lorsque les chercheurs ont cartographié les orientations cellulaires à l’échelle entière des embryons, ils ont trouvé que l’alignement était toujours le plus fort près de ces frontières et plus faible au centre. Ce schéma suggère que les bords du tissu agissent comme des rails guides, indiquant aux cellules dans quelle direction se tourner et finissant par façonner l’ensemble de la structure.
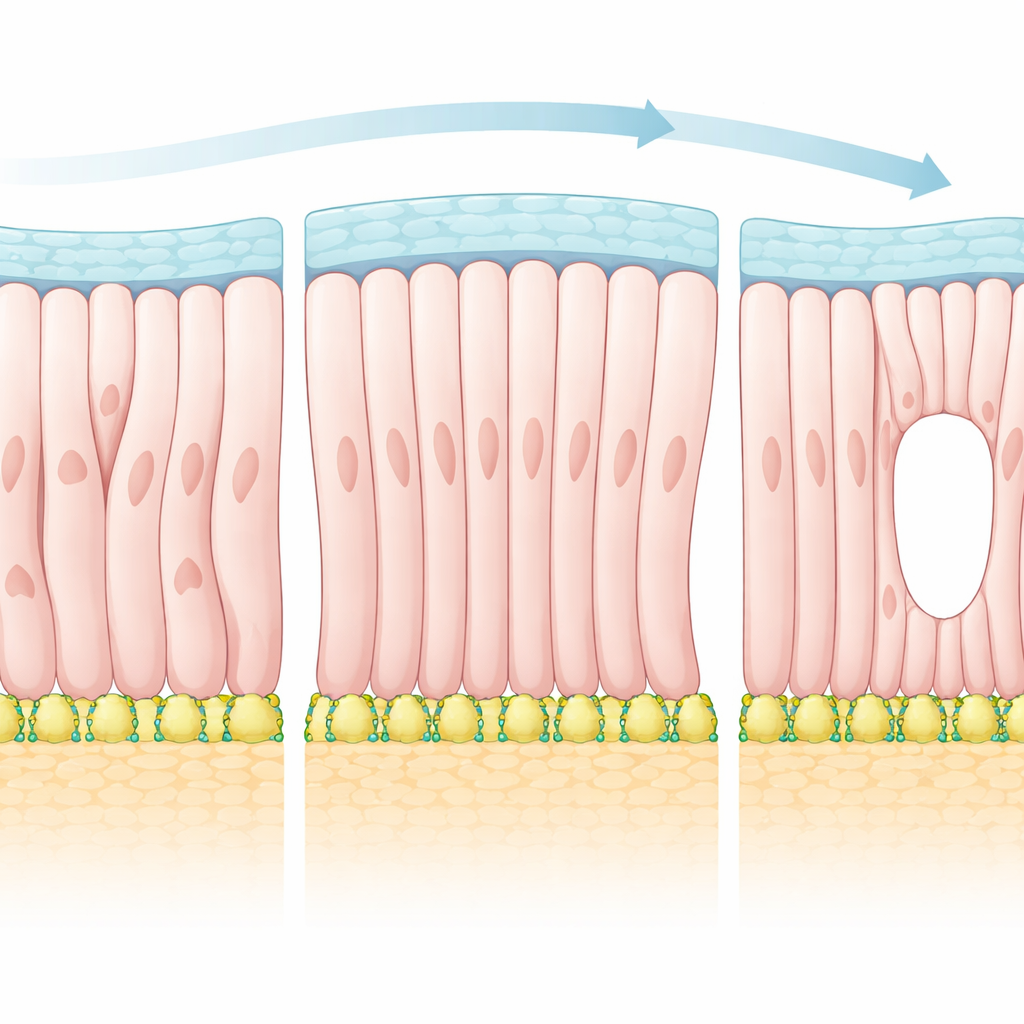
Emprunter des idées aux cristaux liquides
Pour expliquer ces observations, les auteurs se sont tournés vers un cadre théorique plus couramment utilisé pour décrire les cristaux liquides dans les écrans. Dans ces matériaux, des molécules en forme de tige tendent à s’aligner entre elles, mais leur motif exact peut être fortement influencé par les surfaces qui les confinent. L’équipe a traité les cellules de l’épiblaste comme des « particules » polaires qui préfèrent s’aligner à la fois avec leurs voisines et avec des directions imposées par les frontières environnantes. À partir de cette théorie, ils ont prédit que lorsque l’influence des frontières s’intensifie, le tissu devrait subir une transition vers un état plus ordonné contenant des points particuliers de perturbation du champ d’alignement — des soi‑disant défauts topologiques. Dans l’embryon, ces défauts correspondent à des endroits où les faces apicales des cellules convergent et où la future cavité s’ouvre en premier.
Ancrages moléculaires au bord inférieur
Qu’est‑ce qui, au niveau moléculaire, confère au bord de l’endoderme viscéral son influence marquée ? Les auteurs ont combiné des données transcriptionnelles unicellulaires et des marquages protéiques pour montrer que cette frontière inférieure devient enrichie en composants spécifiques de la matrice extracellulaire, en particulier la laminine, et en forme active de son partenaire membranaire, l’intégrine β1. Ensemble, ils agissent comme de minuscules ancrages moléculaires pour le côté basal des cellules de l’épiblaste. À mesure que l’adhésion laminine–intégrine s’intensifie au fil du temps à cette frontière, l’alignement des cellules se renforce et un motif robuste émerge. Dans des simulations numériques, affaiblir cet ancrage effaçait le motif ordonné, suggérant que ces molécules sont essentielles pour que le tissu « sente » et réponde à son bord.
Quand les ancrages cèdent, forme et signalisation faiblissent
Pour tester cela directement, les chercheurs ont examiné des embryons dépourvus de laminine γ1 ou d’intégrine β1. Chez ces mutants, les cellules de l’épiblaste ne se tournaient plus perpendiculairement vers le bord de l’endoderme viscéral mais restaient tangentiellement orientées, comme près de la frontière supérieure. Le tissu perdit son alignement radial caractéristique, les amas en rosette des surfaces apicales ne se formèrent plus correctement, et les sites d’initiation de la lumière furent perturbés. Pourtant, l’étendue générale de l’allongement cellulaire augmentait toujours, indiquant que le défaut principal concernait l’orientation des cellules plutôt que leur capacité à s’étirer. Dans une manipulation distincte, l’affaiblissement enzymatique de la matrice au bord inférieur réduisit l’activité d’ERK, une voie de signalisation importante pour la croissance et la différenciation cellulaires, suggérant que le bon façonnage du tissu aide à déclencher les programmes moléculaires qui propulsent la maturation de l’épiblaste.
Pourquoi cela importe pour la construction des organismes
En termes simples, l’étude montre que la façon dont les cellules embryonnaires précoces s’alignent n’est pas aléatoire ; elle est dirigée par des différences à leurs frontières, en particulier par l’adhésion laminine–intégrine du côté de l’endoderme viscéral. Cet alignement guidé par la frontière suffit à expliquer où la première cavité apparaît et comment des signaux comme ERK sont activés pour faire progresser le développement de l’embryon. Pour un lecteur non spécialiste, le message clé est que les bords ne sont pas de simples limites passives : ce sont des organisateurs actifs qui aident une masse informe de cellules à devenir un tissu ordonné et fonctionnel, posant la feuille de route pour le reste du corps.
Citation: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Mots-clés: développement embryonnaire, alignement cellulaire, matrice extracellulaire, mise en forme des tissus, formation de la lumière