Clear Sky Science · pt
Alinhamento celular guiado por bordas impulsiona a maturação do epiblasto de camundongo
Como os Tecidos Encontram Sua Forma
Antes que um embrião de camundongo assuma qualquer forma reconhecível, suas células precisam primeiro decidir como se alinhar e onde esculpir a primeira cavidade interna. Este artigo explora uma questão aparentemente simples, com grandes implicações: como uma bola de células aparentemente sem características se autoorganiza em uma estrutura bem ordenada que depois pode construir órgãos e eixos do corpo? Ao observar embriões de camundongo em estágio inicial em três dimensões e combinar biologia com física, os autores revelam como as bordas de um tecido coreografam silenciosamente essa transformação.
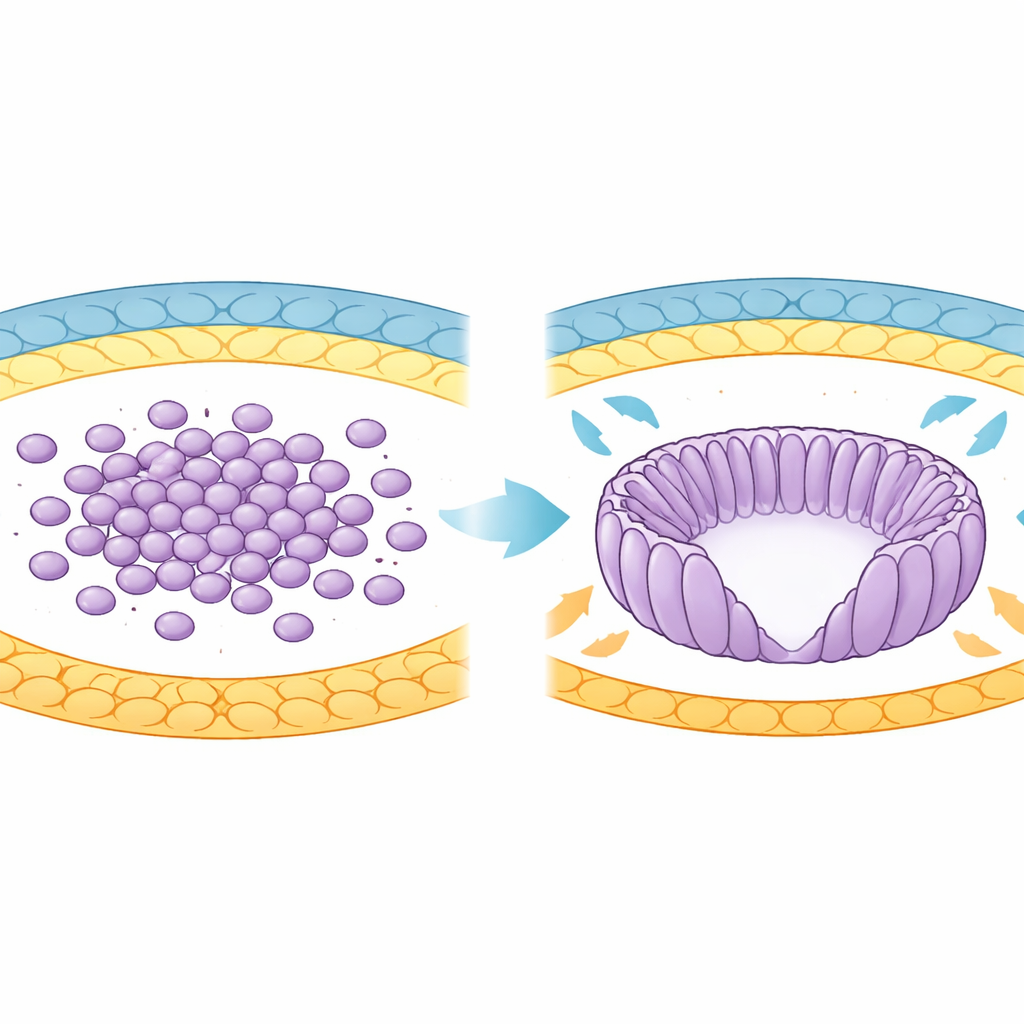
Do Agregado Celular ao Cálice Organizado
No início do desenvolvimento, o futuro corpo do camundongo provém de um grupo de células chamado epiblasto. Inicialmente essas células são arredondadas e frouxamente organizadas dentro do blastocisto. À medida que o embrião se implanta no útero, o epiblasto se remodela em uma estrutura em forma de cálice chamada cilindro embrionário. Durante essa transição, as células se alongam em formas elípticas, se alinham como raios em uma roda e circundam uma cavidade central conhecida como cavidade proamniótica. Os autores usaram imageamento 3D avançado e análise computacional para rastrear milhares de células enquanto essa mudança de forma ocorria entre dias específicos do desenvolvimento, revelando um aumento progressivo na similaridade de orientação entre células vizinhas.
O Poder das Bordas e Fronteiras
O epiblasto não existe isoladamente. Ele é envolvido por dois tecidos diferentes que formam fronteiras distintas: um que se tornará o endoderma visceral abaixo, e outro que se tornará o ectoderma extraembrionário acima. O estudo mostra que as células do epiblasto gradualmente se orientam perpendicularmente ao lado do endoderma visceral, mas paralelamente ao lado extraembrionário. Isso significa que, onde o epiblasto toca vizinhos diferentes, as células adotam direções preferenciais distintas. Quando os pesquisadores mapearam as orientações celulares por todo o embrião, descobriram que o alinhamento era sempre mais forte perto dessas fronteiras e mais fraco no centro. Esse padrão sugeriu que as bordas do tecido atuam como trilhos orientadores, indicando às células para que lado apontar e, em última instância, moldando toda a estrutura.
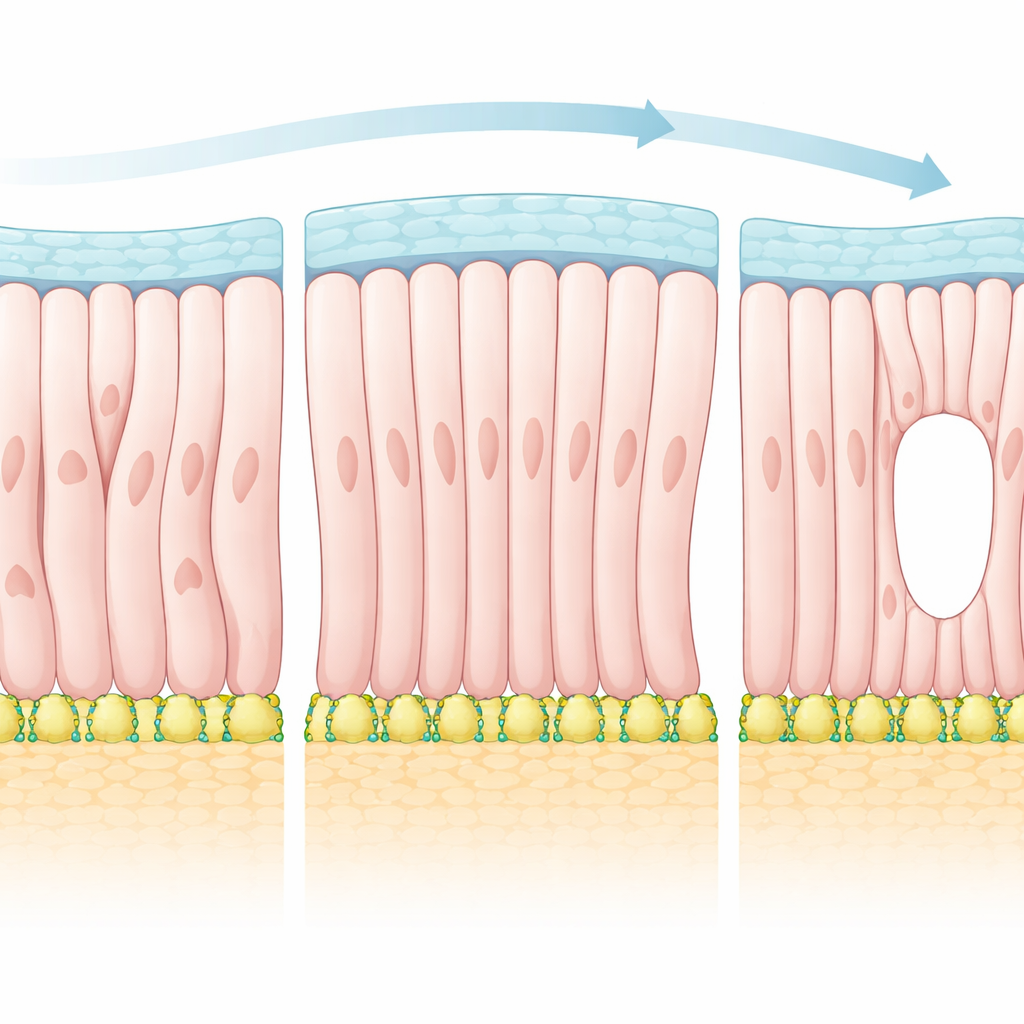
Tomando Emprestado Conceitos de Cristais Líquidos
Para explicar essas observações, os autores recorreram a um arcabouço mais comumente usado para descrever cristais líquidos em displays. Nesses materiais, moléculas em forma de bastão tendem a se alinhar umas com as outras, mas seu padrão exato pode ser fortemente influenciado pelas superfícies que as confinam. A equipe tratou as células do epiblasto como “partículas” polares que preferem se alinhar tanto com suas vizinhas quanto com direções impostas pelas fronteiras circundantes. Usando essa teoria, eles previram que, à medida que a influência das fronteiras se fortalece, o tecido deveria sofrer uma transição para um estado mais ordenado que contém pontos especiais de ruptura no campo de alinhamento — os chamados defeitos topológicos. No embrião, esses defeitos correspondem a locais onde os lados apicais das células convergem e onde a cavidade futura se abre pela primeira vez.
Âncoras Moleculares na Borda Inferior
O que, ao nível molecular, confere ao limite do endoderma visceral sua forte influência? Os autores combinaram dados de expressão em célula única e marcação proteica para mostrar que essa fronteira inferior se torna enriquecida em componentes específicos da matriz extracelular, especialmente laminina, e na forma ativa de seu parceiro de superfície celular, a integrina β1. Juntos, esses elementos atuam como pequenas âncoras moleculares para o lado basal das células do epiblasto. À medida que a adesão laminina–integrina se intensifica ao longo do tempo nessa fronteira, o alinhamento celular se torna mais pronunciado e um padrão robusto emerge. Em simulações computacionais, enfraquecer essa ancoragem apagou o padrão ordenado, sugerindo que essas moléculas são essenciais para o tecido “sentir” e responder à sua borda.
Quando as Âncoras Falham, Forma e Sinais Fraquejam
Para testar isso diretamente, os pesquisadores examinaram embriões que careciam de laminina γ1 ou integrina β1. Nesses mutantes, as células do epiblasto deixaram de apontar perpendicularmente para a fronteira do endoderma visceral e, em vez disso, ficaram tangenciais, como ocorrem perto da fronteira superior. O tecido perdeu seu alinhamento radial característico, aglomerados em forma de rosácea de superfícies apicais deixaram de se formar adequadamente, e os locais de iniciação do lúmen foram perturbados. Ainda assim, a extensão básica do alongamento celular continuou a aumentar, indicando que o defeito principal estava em como as células eram orientadas, e não na sua capacidade de se alongar. Em uma manipulação separada, o enfraquecimento enzimático da matriz na fronteira inferior reduziu a atividade de ERK, uma via de sinalização importante para crescimento e diferenciação celular, sugerindo que o padrão correto do tecido ajuda a disparar os programas moleculares que dirigem a maturação do epiblasto.
Por Que Isso Importa para Construir Corpos
Em termos simples, o estudo mostra que a forma como as células embrionárias iniciais se alinham não é aleatória; ela é guiada por diferenças em suas fronteiras, especialmente pela adesão laminina–integrina no lado do endoderma visceral. Esse alinhamento guiado pela fronteira é suficiente para explicar onde a primeira cavidade surge e como sinais como ERK são ativados para levar o embrião adiante no desenvolvimento. Para um leitor leigo, a mensagem principal é que as bordas não são apenas fronteiras passivas: são organizadoras ativas que ajudam um amontoado informe de células a se tornar um tecido ordenado e funcional, traçando a planta para o restante do corpo.
Citação: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Palavras-chave: desenvolvimento embrionário, alinhamento celular, matriz extracelular, padronização tecidual, formação de lúmen