Clear Sky Science · sv
Kantstyrd cellinriktning driver musens epiblastermognad
Hur vävnader hittar sin form
Innan ett musembryo får någon igenkännbar form måste dess celler först bestämma hur de ska rada upp sig och var de ska skapa den allra första inre håligheten. Denna artikel undersöker en bedrägligt enkel fråga med stora följder: hur organiserar en till synes formlös cellklot sig själv till en välordnad struktur som senare kan bygga organ och kroppsaxlar? Genom att följa tidiga musembryon i tre dimensioner och förena biologi med fysik visar författarna hur vävnadens kanter tyst koreograferar denna omvandling.
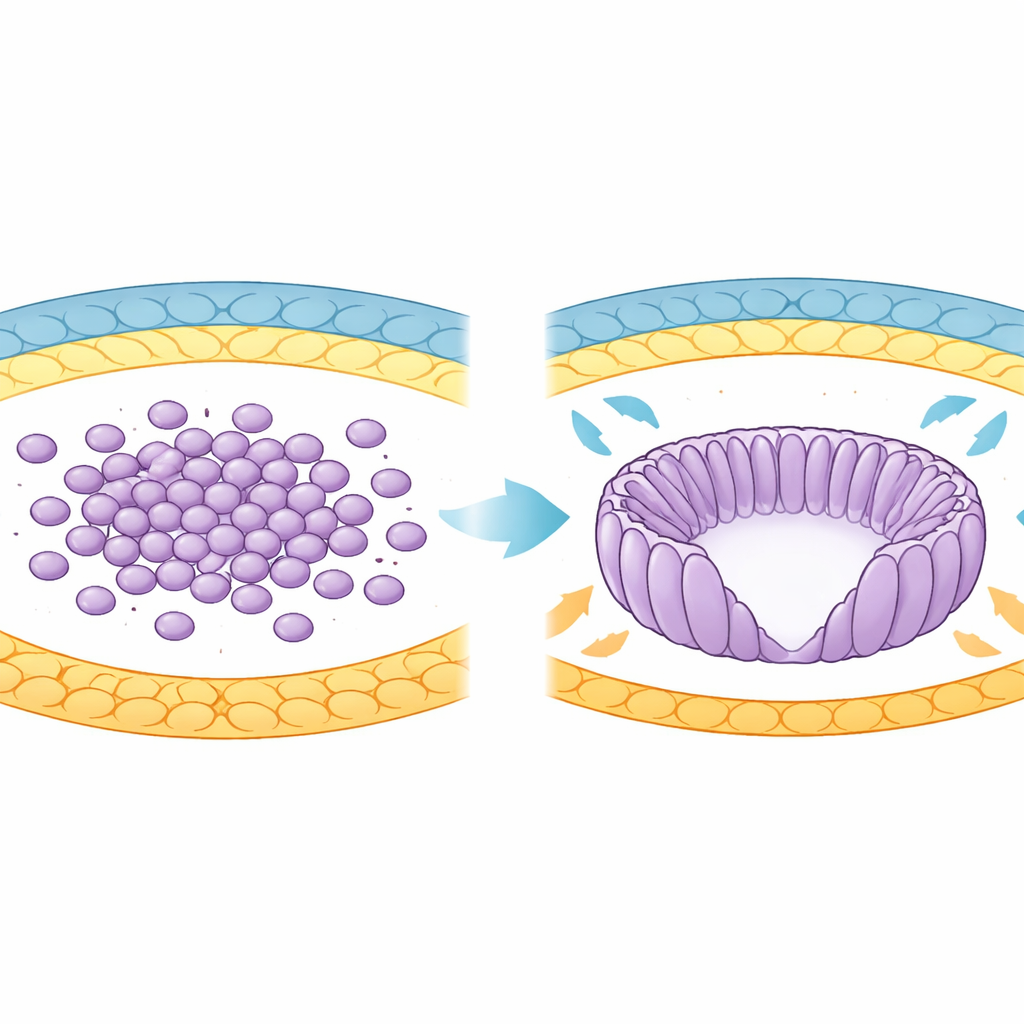
Från cellklunga till organiserad kopp
I tidig utveckling kommer musens framtida kropp från en cellgrupp som kallas epiblaster. Inledningsvis är dessa celler runda och löst organiserade inne i blastocysten. När embryot implanteras i livmodern omformar epiblaster sig till en koppformig struktur kallad äggcylinder. Under denna övergång sträcks cellerna ut till förlängda former, radas upp som ekrar i ett hjul och omger en central hålighet känd som proamniotiska håligheten. Författarna använde avancerad 3D-bildtagning och datoranalys för att följa tusentals celler medan denna formförändring skedde under specifika utvecklingsdagar, och avslöjade en gradvis ökning i hur lika grannceller var orienterade.
Kraften hos kanter och gränser
Epiblaster finns inte isolerade. De är omslutna av två olika vävnader som bildar distinkta gränser: en som blir visceral endoderm nedanför och en annan som blir extraembryonal ektoderm ovanför. Studien visar att epiblasterceller gradvis orienterar sig vinkelrätt mot visceral endoderm-sidan men parallellt med den extraembryonala sidan. Det betyder att där epiblaster möter olika grannar antar cellerna olika föredragna riktningar. När forskarna kartlade cellernas orientering över hela embryon fann de att inriktningen alltid var starkast nära dessa gränser och svagare i mitten. Detta mönster antyder att vävnadens kanter fungerar som styrskenor som talar om för cellerna åt vilket håll de ska peka och i slutändan formar hela strukturen.
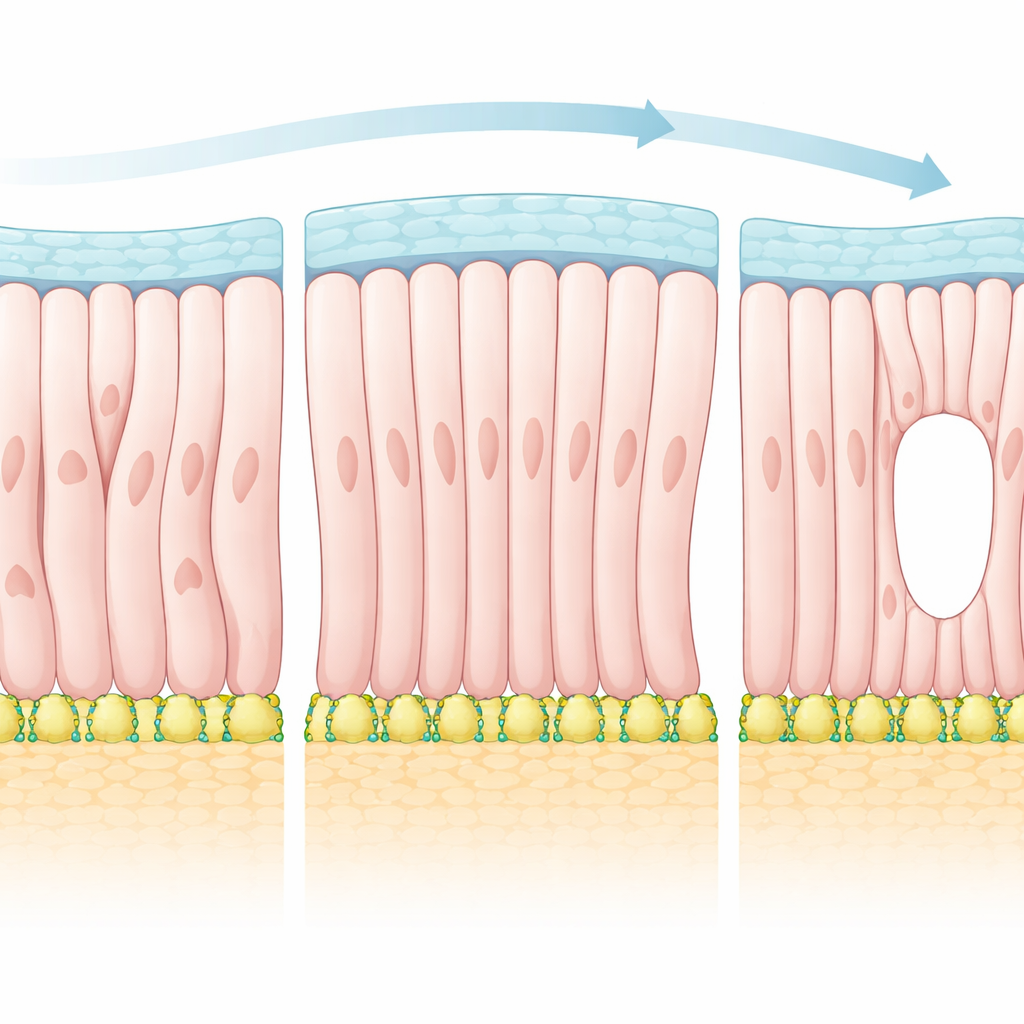
Lånar idéer från flytande kristaller
För att förklara dessa observationer använde författarna en ram som oftare används för att beskriva flytande kristaller i bildskärmar. I sådana material tenderar stavformade molekyler att rada upp sig med varandra, men deras exakta mönster kan starkt påverkas av de ytor som begränsar dem. Teamet behandlade epiblasterceller som polära "partiklar" som föredrar att anpassa sig både med sina grannar och med riktningar som påtvingas av kringliggande gränser. Med hjälp av denna teori förutsade de att när gränsernas inflytande stärks bör vävnaden genomgå en övergång till ett mer ordnat tillstånd som innehåller särskilda punkter av störning i inriktningsfältet — så kallade topologiska defekter. I embryot motsvarar dessa defekter platser där cellernas apikala sidor konvergerar och där den framtida håligheten först öppnas.
Molekylära ankare vid den nedre kanten
Vad är det på molekylär nivå som ger visceral endoderm-gränsen dess starka inflytande? Författarna kombinerade enkelcells-genuttrycksdata och proteinfärgning för att visa att denna nedre gräns blir berikad i specifika komponenter av den extracellulära matrisen, särskilt laminin, och i den aktiva formen av dess cellmembranpartner, integrin β1. Tillsammans fungerar dessa som små molekylära ankare för epiblastcellernas basala sida. När laminin–integrin-adhesionen intensifieras över tid vid denna gräns blir cellinriktningen mer uttalad och ett robust mönster uppstår. I datorsimuleringar raderade försvagning av detta förankrande det ordnade mönstret, vilket antyder att dessa molekyler är nödvändiga för att vävnaden ska kunna "känna" och reagera på sin kant.
När ankare sviker försämras form och signaler
För att testa detta direkt undersökte forskarna embryon som saknade laminin γ1 eller integrin β1. I dessa mutanter pekade epiblastceller inte längre vinkelrätt in mot visceral endoderm-gränsen utan låg i stället tangentiellt, som de gör nära den övre gränsen. Vävnaden förlorade sin karakteristiska radiella inriktning, rosettliknande kluster av apikala ytor bildades inte korrekt och lumeninitieringsplatser stördes. Ändå ökade cellernas grundläggande förlängning fortsatt, vilket indikerar att huvudfelet låg i hur cellerna var orienterade snarare än i deras förmåga att sträcka ut sig. I en separat manipulation minskade enzymatisk försvagning av matrisen vid den nedre gränsen aktiviteten i ERK, en signalväg viktig för celltillväxt och differentiering, vilket tyder på att korrekt vävnadsmönstring hjälper till att utlösa de molekylära program som driver epiblastmognad.
Varför detta spelar roll för att bygga kroppar
Enkelt uttryckt visar studien att sättet tidiga embryonceller radar upp sig inte är slumpmässigt; det styrs av skillnader vid deras gränser, särskilt av laminin–integrin-adhesion vid visceral endoderm-sidan. Denna kantstyrda inriktning räcker för att förklara var den första håligheten uppstår och hur signaler som ERK aktiveras för att föra embryot vidare i utvecklingen. För en lekmannaläsare är huvudbudskapet att kanter inte bara är passiva gränser: de är aktiva organisatörer som hjälper en formlös cellklump att bli en ordnad, funktionell vävnad och lägger grunden för resten av kroppen.
Citering: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Nyckelord: embryonal utveckling, cellinriktning, extracellulär matrix, vävnadsmönstring, lumenbildning