Clear Sky Science · it
L'allineamento cellulare guidato dai confini guida la maturazione dell'epiblasto del topo
Come i tessuti trovano la loro forma
Prima che un embrione di topo assuma una qualsiasi forma riconoscibile, le sue cellule devono innanzitutto decidere come disporsi e dove scavare la primissima cavità interna. Questo articolo esplora una domanda apparentemente semplice ma dalle grandi implicazioni: come una sfera di cellule priva di caratteristiche evidenti si auto-organizza in una struttura ordinata capace poi di costruire organi e assi corporei? Osservando embrioni di topo in tre dimensioni e combinando biologia e fisica, gli autori svelano come i margini di un tessuto orchestrino silenziosamente questa trasformazione.
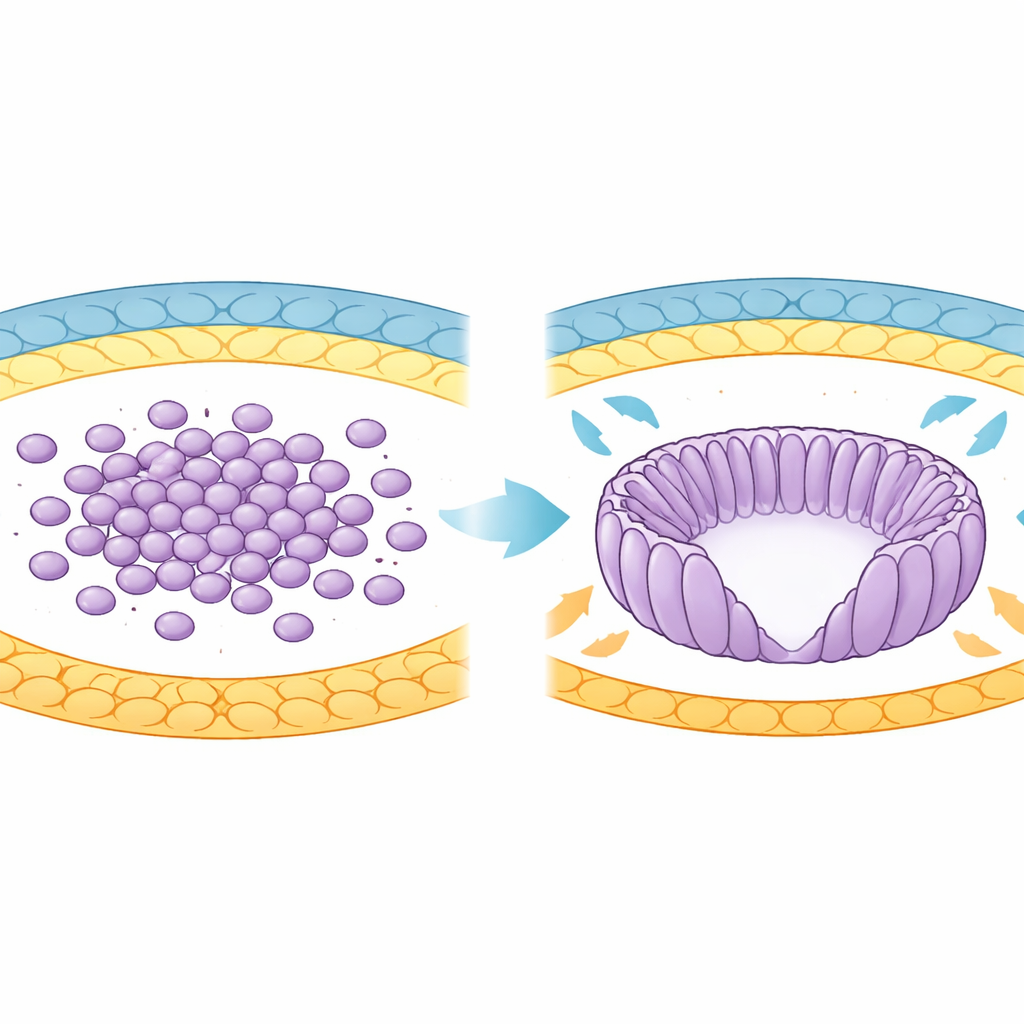
Da ammasso cellulare a coppa organizzata
Nello sviluppo precoce, il futuro corpo del topo deriva da un gruppo di cellule chiamato epiblasto. Inizialmente queste cellule sono rotonde e poco ordinate all'interno del blastocisto. Quando l'embrione si impianta nell'utero, l'epiblasto si rimodella in una struttura a forma di coppa chiamata cilindro embrionale. Durante questa transizione, le cellule si allungano, si dispongono come raggi di una ruota e circondano una cavità centrale nota come cavità proamniotica. Gli autori hanno utilizzato immagini 3D avanzate e analisi computazionali per tracciare migliaia di cellule mentre questo cambiamento di forma si svolgeva in giorni di sviluppo specifici, rivelando un aumento progressivo della similarità nell'orientamento tra cellule vicine.
Il potere dei bordi e delle frontiere
L'epiblasto non vive isolato. È avvolto da due tessuti diversi che formano confini distinti: uno che diventerà l'endoderma viscerale sotto e un altro che diventerà l'ectoderma extraembrionale sopra. Lo studio mostra che le cellule dell'epiblasto si orientano progressivamente perpendicolarmente rispetto al lato dell'endoderma viscerale ma parallelamente al lato extraembrionale. Questo significa che dove l'epiblasto tocca vicini diversi, le cellule adottano direzioni preferenziali diverse. Quando i ricercatori mappavano le orientazioni cellulari nell'intero embrione, hanno scoperto che l'allineamento era sempre più forte vicino a questi confini e più debole al centro. Questo schema suggerisce che i margini del tessuto agiscano come rotaie guida, indicando alle cellule in quale direzione puntare e modellando infine l'intera struttura.
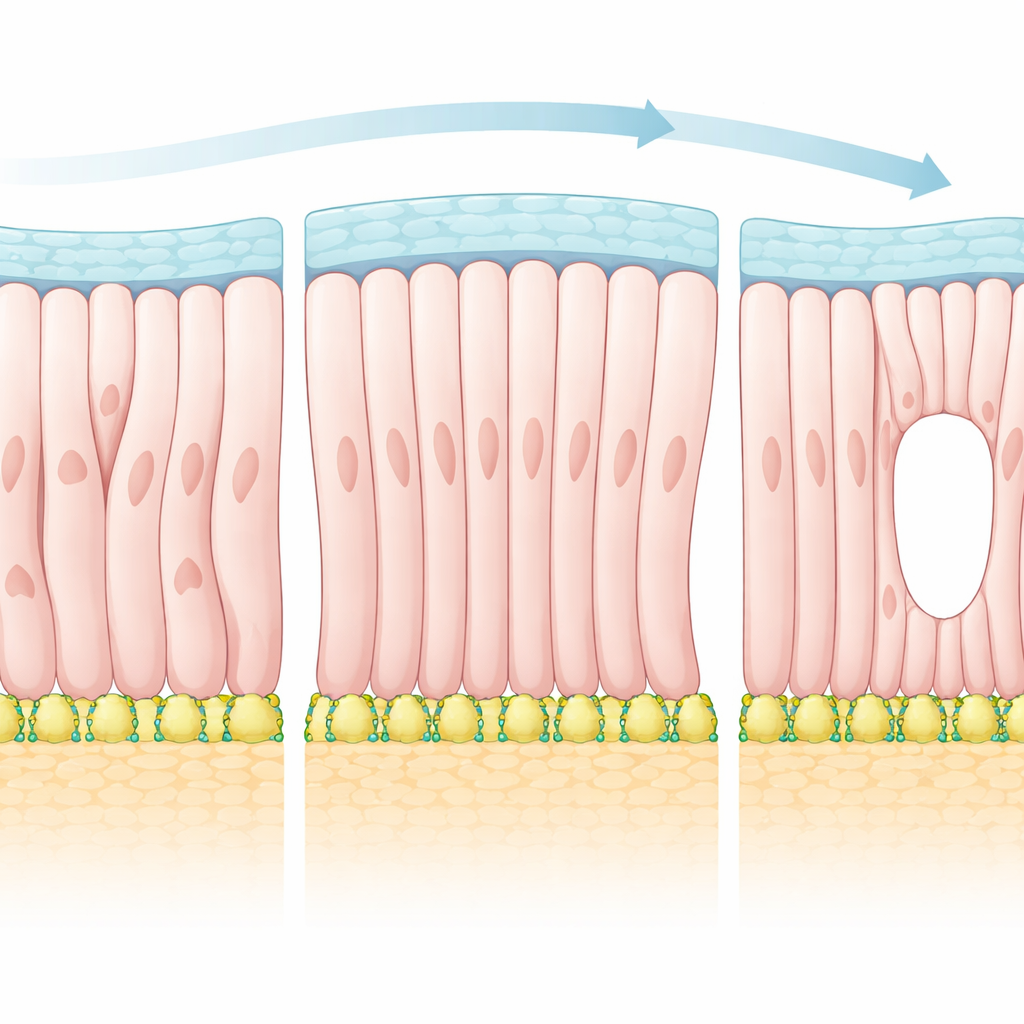
Prendendo in prestito idee dai cristalli liquidi
Per spiegare queste osservazioni, gli autori hanno fatto riferimento a un quadro teorico più comunemente usato per descrivere i cristalli liquidi nei display. In tali materiali, molecole a forma di asta tendono ad allinearsi tra loro, ma il loro pattern può essere fortemente influenzato dalle superfici che le confinano. Il team ha trattato le cellule dell'epiblasto come «particelle» polari che preferiscono allinearsi sia con i vicini sia con direzioni imposte dai confini circostanti. Usando questa teoria, hanno previsto che, man mano che l'influenza dei confini si rafforza, il tessuto dovrebbe subire una transizione verso uno stato più ordinato che contiene punti speciali di disturbo nel campo di allineamento — i cosiddetti difetti topologici. Nell'embrione, questi difetti corrispondono a luoghi dove i lati apicali delle cellule convergono e dove la futura cavità si apre per la prima volta.
Ancore molecolari al margine inferiore
Cosa, a livello molecolare, conferisce al confine dell'endoderma viscerale la sua forte influenza? Gli autori hanno combinato dati trascrizionali a singola cellula e colorazioni proteiche per mostrare che questo confine inferiore si arricchisce in componenti specifici della matrice extracellulare, in particolare laminina, e nella forma attiva del suo partner di superficie cellulare, l'integrina β1. Insieme, questi agiscono come piccole ancore molecolari per il lato basale delle cellule dell'epiblasto. All'aumentare dell'adesione laminina–integrina in questo confine, l'allineamento cellulare diventa più marcato e emerge un pattern robusto. Nelle simulazioni al computer, indebolire questa ancoraggio cancellava il pattern ordinato, suggerendo che queste molecole sono essenziali perché il tessuto «senta» e risponda al proprio margine.
Quando le ancore falliscono, forma e segnali vacillano
Per testare questo direttamente, i ricercatori hanno esaminato embrioni privi di laminina γ1 o integrina β1. In questi mutanti, le cellule dell'epiblasto non si orientavano più perpendicolarmente verso il confine dell'endoderma viscerale ma si disponevano invece tangenzialmente, come accade vicino al confine superiore. Il tessuto perdeva il caratteristico allineamento radiale, gli aggregati a rosetta delle superfici apicali non si formavano correttamente e i siti di inizio della cavità venivano perturbati. Tuttavia, l'entità complessiva dell'allungamento cellulare aumentava ancora, indicando che il difetto principale riguardava l'orientamento delle cellule più che la loro capacità di allungarsi. In una manipolazione separata, l'indebolimento enzimatico della matrice al confine inferiore riduceva l'attività di ERK, una via di segnalazione importante per la crescita e la differenziazione cellulare, suggerendo che un corretto patterning tissutale contribuisce ad attivare i programmi molecolari che guidano la maturazione dell'epiblasto.
Perché questo conta per la costruzione dei corpi
In breve, lo studio mostra che il modo in cui le cellule embrionali precoci si dispongono non è casuale; è guidato dalle differenze ai loro confini, in particolare dall'adesione laminina–integrina sul lato dell'endoderma viscerale. Questo allineamento guidato dai bordi è sufficiente a spiegare dove appare la prima cavità e come segnali come ERK vengano attivati per far progredire lo sviluppo dell'embrione. Per il lettore non specialistico, il messaggio chiave è che i margini non sono solo confini passivi: sono organizzatori attivi che aiutano un ammasso informe di cellule a diventare un tessuto ordinato e funzionale, tracciando il progetto per il resto del corpo.
Citazione: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Parole chiave: sviluppo embrionale, allineamento cellulare, matrice extracellulare, modellazione dei tessuti, formazione della cavità