Clear Sky Science · de
Randgeführte Zellorientierung treibt die Reifung des Maus‑Epiblasten voran
Wie Gewebe ihre Form finden
Bevor ein Maus‑Embryo eine erkennbare Gestalt annimmt, müssen seine Zellen zuerst entscheiden, wie sie sich ausrichten und wo sie die allererste innere Höhlung anlegen. Dieser Artikel untersucht eine auf den ersten Blick einfache Frage mit großen Folgen: Wie organisiert sich eine scheinbar strukturlose Zellkugel selbst zu einer geordneten Struktur, die später Organe und Körperachsen hervorbringen kann? Durch Beobachtung früher Maus‑Embryonen in drei Dimensionen und eine Verbindung von Biologie und Physik zeigen die Autoren, wie die Ränder eines Gewebes diese Umformung still dirigieren.
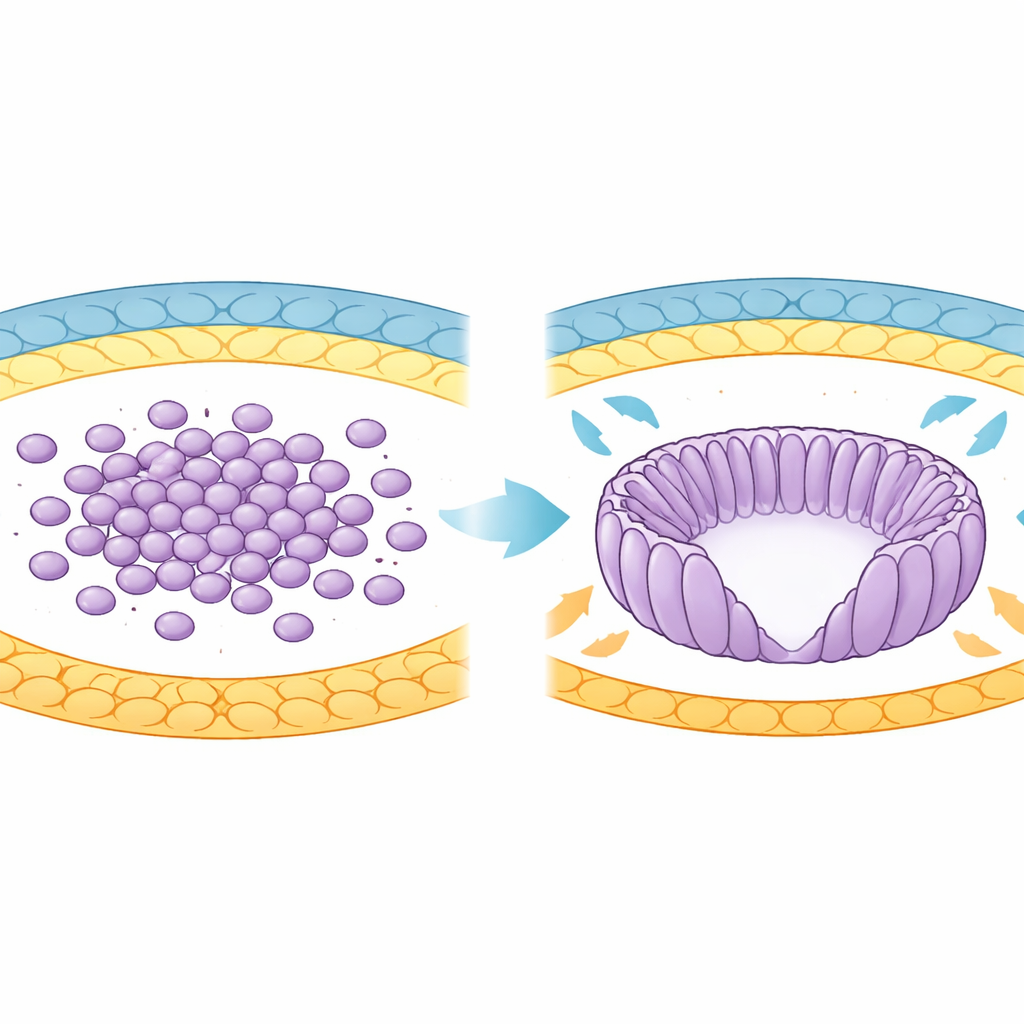
Vom Zellhaufen zur organisierten Schale
In der frühen Entwicklung stammt der zukünftige Körper der Maus aus einer Zellpopulation, dem Epiblasten. Zunächst sind diese Zellen rund und lose im Blastozysten angeordnet. Wenn der Embryo in die Gebärmutter implantiert, formt sich der Epiblast zu einer becherartigen Struktur, dem sogenannten Eizylinder. Während dieser Umwandlung strecken sich Zellen zu länglichen Formen, ordnen sich wie Speichen eines Rades und umschließen eine zentrale Höhlung, die Proamniotishöhle. Die Autoren nutzten fortgeschrittene 3D‑Bildgebung und computergestützte Analyse, um Tausende von Zellen über die relevanten Entwicklungstage hinweg zu verfolgen und zeigten so eine fortschreitende Zunahme der Ähnlichkeit in der Orientierung benachbarter Zellen.
Die Macht von Kanten und Grenzen
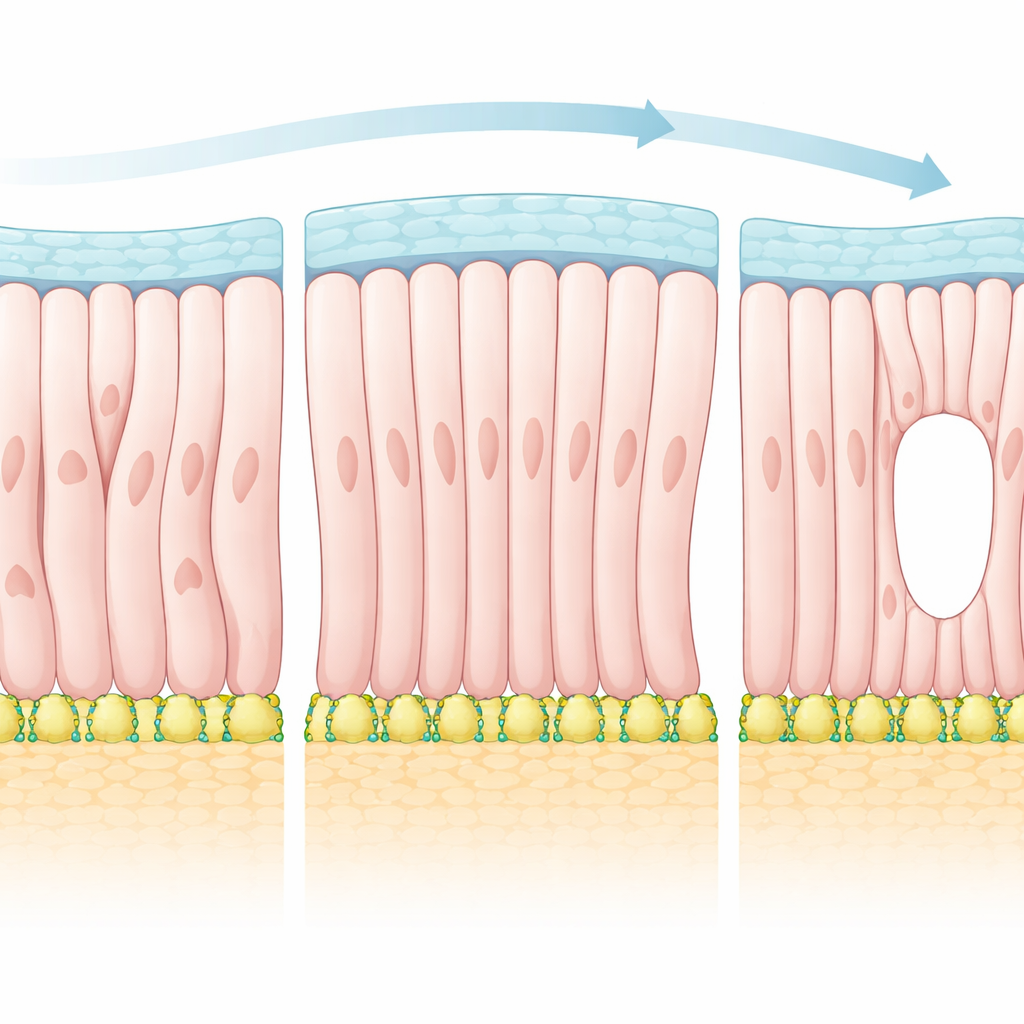
Der Epiblast existiert nicht isoliert. Er ist von zwei unterschiedlichen Geweben umgeben, die ausgeprägte Grenzen bilden: eines, das später das viszerale Endoderm unten wird, und ein anderes, das oberhalb das extraembryonale Ektoderm wird. Die Studie zeigt, dass sich Epiblastzellen schrittweise senkrecht zur Seite des viszeralen Endoderms, aber parallel zur extraembryonalen Seite ausrichten. Das bedeutet: Wo der Epiblast auf verschiedene Nachbargewebe trifft, nehmen Zellen unterschiedliche bevorzugte Richtungen ein. Als die Forscher die Zellorientierungen über ganze Embryonen kartierten, fanden sie, dass die Ausrichtung stets nahe diesen Grenzen am stärksten und in der Mitte schwächer war. Dieses Muster legt nahe, dass die Ränder des Gewebes als leitende Schienen wirken, die den Zellen sagen, wohin sie zeigen sollen, und so die gesamte Form prägen.
Ideen aus Flüssigkristallen
Um diese Beobachtungen zu erklären, griffen die Autoren auf ein Rahmenwerk zurück, das häufiger zur Beschreibung von Flüssigkristallen in Displays verwendet wird. In solchen Materialien neigen stäbchenförmige Moleküle dazu, sich gegenseitig auszurichten, wobei ihre genaue Anordnung stark von den sie begrenzenden Oberflächen beeinflusst werden kann. Das Team behandelte Epiblastzellen als polare „Partikel“, die sich sowohl mit ihren Nachbarn als auch entlang von von den umgebenden Grenzen vorgegebenen Richtungen ausrichten möchten. Mit dieser Theorie sagten sie voraus, dass mit zunehmendem Einfluss der Grenzen das Gewebe in einen geordneteren Zustand übergehen sollte, der spezielle Störpunkte im Orientierungsfeld enthält – sogenannte topologische Defekte. Im Embryo entsprechen diese Defekte Stellen, an denen die apikalen Seiten der Zellen zusammenlaufen und an denen sich die zukünftige Höhlung zuerst öffnet.
Molekulare Anker an der unteren Grenze
Was verleiht auf molekularer Ebene der Grenze zum viszeralen Endoderm ihren starken Einfluss? Die Autoren kombinierten Einzelzell‑Genexpressionsdaten und Proteinfärbung und zeigten, dass diese untere Grenze mit bestimmten Komponenten der extrazellulären Matrix, insbesondere Laminin, und mit der aktiven Form ihres zellulären Partners Integrin β1 angereichert wird. Zusammen wirken diese wie winzige molekulare Verankerungen für die basale Seite der Epiblastzellen. Wenn Laminin–Integrin‑Adhäsion an dieser Grenze im Laufe der Zeit zunimmt, wird die Zellorientierung ausgeprägter und ein robustes Muster entsteht. In Computersimulationen löschte eine Abschwächung dieser Verankerung das geordnete Muster, was darauf hindeutet, dass diese Moleküle wesentlich dafür sind, dass das Gewebe seine Kante „fühlt“ und darauf reagiert.
Wenn Anker versagen, leiden Form und Signale
Um dies direkt zu testen, untersuchten die Forscher Embryonen ohne Laminin γ1 oder Integrin β1. In diesen Mutanten zeigten Epiblastzellen nicht mehr die senkrechte Ausrichtung in Richtung der viszeralen Endodermgrenze, sondern lagen tangential, wie sie es in der Nähe der oberen Grenze tun. Das Gewebe verlor seine charakteristische radiale Ausrichtung, rosettenartige Cluster apikaler Flächen bildeten sich nicht richtig, und die Stellen, an denen das Lumen initiiert wird, waren gestört. Dennoch nahm das Ausmaß der Zellexpansion weiterhin zu, was darauf hindeutet, dass der Hauptfehler in der Orientierung der Zellen lag und weniger darin, ob sie sich strecken können. In einer separaten Manipulation reduzierte eine enzymatische Schwächung der Matrix an der unteren Grenze die Aktivität von ERK, einem Signalweg, der für Zellwachstum und Differenzierung wichtig ist. Das legt nahe, dass korrektes Gewebepatterning dazu beiträgt, die molekularen Programme zu starten, die die Reifung des Epiblasten vorantreiben.
Warum das für den Körperbau wichtig ist
Kurz gesagt zeigt die Studie, dass die Art und Weise, wie frühe embryonale Zellen sich ausrichten, nicht zufällig ist; sie wird durch Unterschiede an ihren Grenzen gesteuert, insbesondere durch Laminin–Integrin‑Adhäsion an der Seite zum viszeralen Endoderm. Diese randgeführte Ausrichtung erklärt, wo die erste Höhlung erscheint und wie Signale wie ERK aktiviert werden, um die Entwicklung des Embryos voranzutreiben. Für eine allgemeinere Leserschaft lautet die Kernbotschaft: Ränder sind nicht bloß passive Grenzen – sie sind aktive Organisatoren, die einem formlosen Zellklumpen helfen, zu einem geordneten, funktionellen Gewebe zu werden und damit das Fundament für den Rest des Körpers legen.
Zitation: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Schlüsselwörter: embryonale Entwicklung, Zellorientierung, extrazelluläre Matrix, Gewebe‑Patterning, Lumenbildung