Clear Sky Science · pl
Wytyczanie kształtu: wyrównanie komórek przy krawędzi napędza dojrzewanie epiblastu myszy
Jak tkanki znajdują swój kształt
Zanim embrion myszy przyjmie jakąkolwiek rozpoznawalną formę, jego komórki muszą zdecydować, jak się ustawić i gdzie wyciąć pierwszą wewnętrzną jamę. Artykuł bada na pozór prostą, lecz mającą dalekosiężne konsekwencje zagadkę: jak pozornie bezkształtna kula komórek samoorganizuje się w uporządkowaną strukturę, która później może zbudować organy i osie ciała? Obserwując wczesne embriony myszy w trzech wymiarach oraz łącząc podejścia biologiczne i fizyczne, autorzy odkrywają, jak brzegi tkanki dyskretnie kierują tę przemianą.
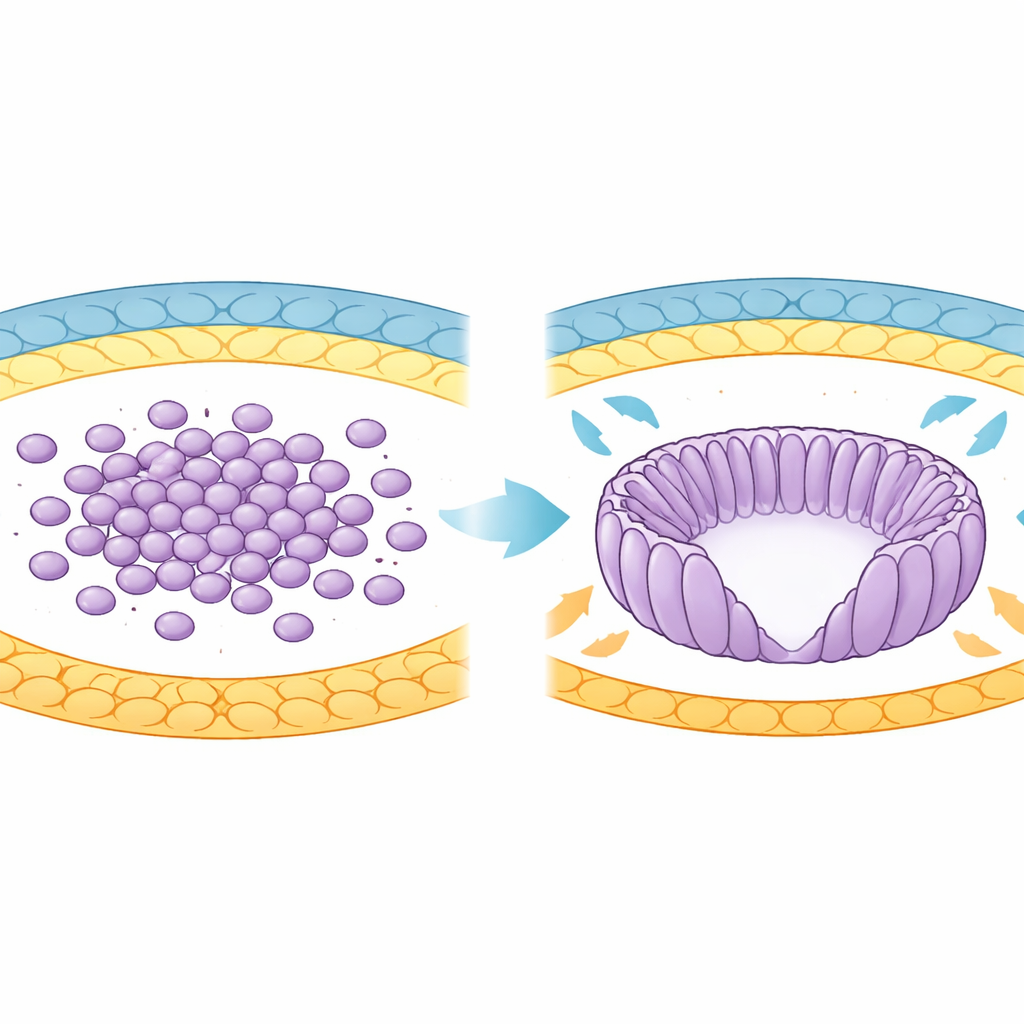
Z klastra komórek do zorganizowanej miseczki
We wczesnym rozwoju przyszłe ciało myszy wywodzi się z grupy komórek zwanych epiblastem. Początkowo komórki te są okrągłe i luźno zorganizowane wewnątrz blastocysty. W miarę jak embrion wszczepia się w macicę, epiblast przekształca się w strukturę przypominającą kielich, zwaną cylindrem zarodkowym. W trakcie tej przemiany komórki wydłużają się, ustawiają jak szprychy koła i otaczają centralną przestrzeń zwaną jamą proamnionową. Autorzy wykorzystali zaawansowane obrazowanie 3D i analizę komputerową, aby śledzić tysiące komórek podczas tej zmiany kształtu między określonymi dniami rozwoju, ujawniając stopniowy wzrost podobieństwa orientacji sąsiadujących komórek.
Siła krawędzi i granic
Epiblast nie istnieje w izolacji. Otacza go dwoje różnych tkanek tworzących wyraźne granice: jedna, która stanie się endodermą trzewną poniżej, i druga, która stanie się ektodermą pozazarodkową powyżej. Badanie pokazuje, że komórki epiblastu stopniowo ustawiają się prostopadle względem strony sąsiadującej z endodermą trzewną, ale równolegle do strony pozazarodkowej. Oznacza to, że tam, gdzie epiblast styka się z różnymi sąsiadami, komórki przyjmują odmienne preferowane kierunki. Gdy badacze odwzorowali orientacje komórek w całych embrionach, okazało się, że wyrównanie jest zawsze najsilniejsze przy tych granicach, a słabsze w centrum. Ten wzór sugeruje, że krawędzie tkanki działają jak prowadnice, wskazując komórkom, w którą stronę mają się ukierunkować, i ostatecznie kształtując całą strukturę.
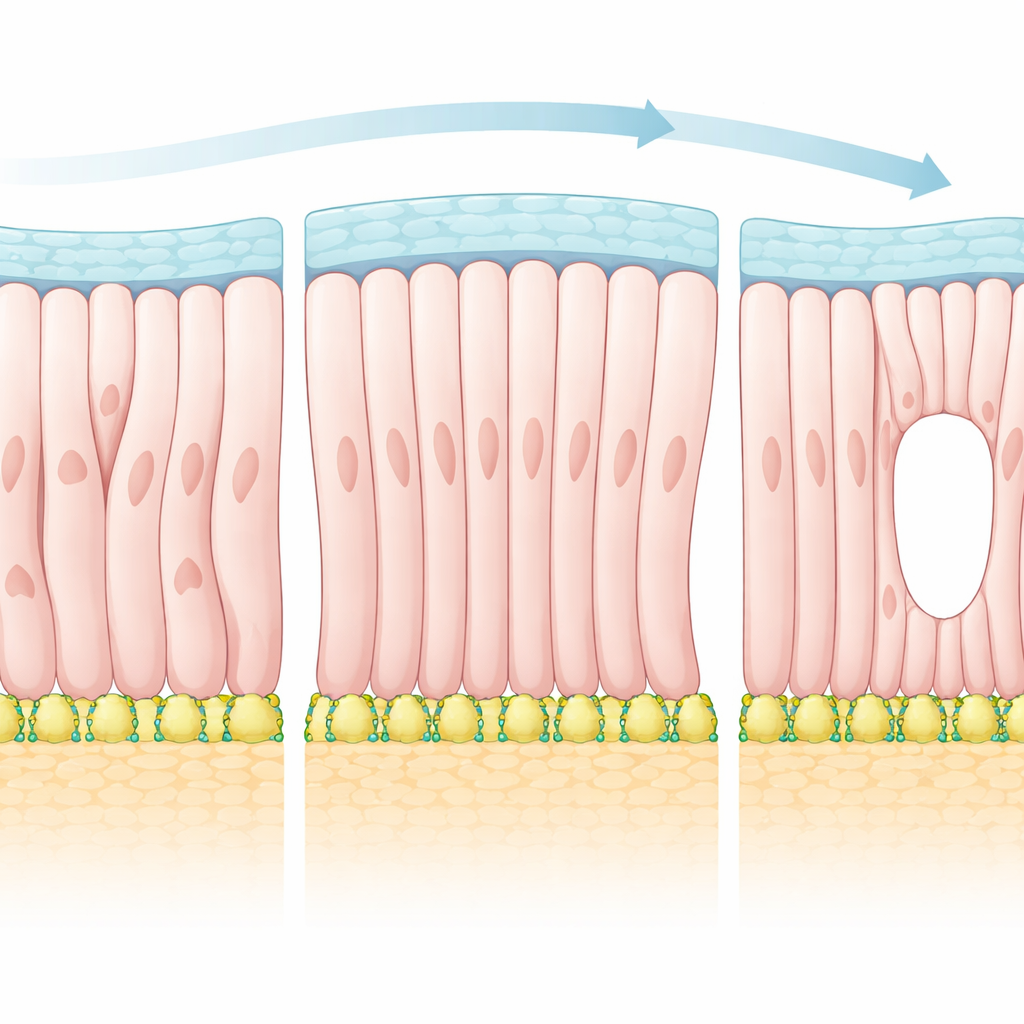
Zapożyczając pomysły z kryształów ciekłych
Aby wyjaśnić obserwacje, autorzy sięgnęli po ramy teoretyczne częściej używane do opisu kryształów ciekłych w ekranach. W takich materiałach cząsteczki o kształcie pręcików mają tendencję do wzajemnego wyrównywania się, ale ich wzór może być mocno zależny od powierzchni, które je ograniczają. Zespół potraktował komórki epiblastu jak spolaryzowane „cząstki”, które preferują wyrównanie zarówno z sąsiadami, jak i z kierunkami narzucanymi przez otaczające granice. Korzystając z tej teorii, przewidzieli, że w miarę jak wpływ granic się wzmacnia, tkanka powinna przejść w bardziej uporządkowany stan zawierający szczególne punkty zaburzenia pola orientacji — tzw. defekty topologiczne. W embrionie te defekty odpowiadają miejscom, gdzie zbiega się powierzchnia apikальная komórek i gdzie po raz pierwszy otwiera się przyszła jama.
Molekularne kotwice przy dolnej krawędzi
Co na poziomie molekularnym nadaje granicy endodermy trzewnej jej silny wpływ? Autorzy połączyli dane z pojedynczych komórek i barwienia białek, aby wykazać, że ta dolna granica staje się wzbogacona w określone składniki macierzy zewnątrzkomórkowej, zwłaszcza lamininę, oraz w aktywną formę jej receptorowego partnera na powierzchni komórkowej, integrynę β1. Razem działają one jak drobne molekularne kotwice dla strony bazalnej komórek epiblastu. W miarę jak adhezja laminina–integryna nasila się w czasie przy tej granicy, wyrównanie komórek staje się bardziej wyraźne i pojawia się stabilny wzór. W symulacjach komputerowych osłabienie tego zakotwiczenia usuwało uporządkowany wzór, co sugeruje, że te cząsteczki są niezbędne, aby tkanka „czuła” i reagowała na swoją krawędź.
Gdy kotwice zawodzą, kształt i sygnalizacja są zaburzone
Aby przetestować to bezpośrednio, badacze zbadali embriony pozbawione lamininy γ1 lub integryny β1. W tych mutantach komórki epiblastu nie sterczały już prostopadle w stronę granicy z endodermą trzewną, lecz układały się stycznie, tak jak w pobliżu górnej granicy. Tkanka straciła charakterystyczne radialne wyrównanie, skupiska powierzchni apikálních uformowane w układy typu rozet nie powstały prawidłowo, a miejsca inicjacji jam zostały zaburzone. Jednak podstawowy zakres wydłużenia komórek nadal się zwiększał, co wskazuje, że główny defekt dotyczył orientacji komórek, a nie zdolności do wydłużania się. W osobnym eksperymencie enzymatyczne osłabienie macierzy przy dolnej granicy zmniejszyło aktywność ERK — szlaku sygnałowego ważnego dla wzrostu i różnicowania komórek — co sugeruje, że prawidłowe patternowanie tkanki pomaga uruchomić molekularne programy napędzające dojrzewanie epiblastu.
Dlaczego to ma znaczenie przy budowie ciała
Mówiąc wprost, badanie pokazuje, że sposób, w jaki wczesne komórki embrionalne się ustawiają, nie jest przypadkowy; jest kierowany przez różnice na ich granicach, w szczególności przez adhezję laminina–integryna po stronie endodermy trzewnej. To wyrównanie prowadzone przez granice wystarcza, by wyjaśnić, gdzie pojawia się pierwsza jama i jak sygnały takie jak ERK są aktywowane, aby popchnąć embrion do przodu w rozwoju. Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że brzegi nie są tylko biernymi granicami: są aktywnymi organizatorami, które pomagają bezkształtnej grudce komórek stać się uporządkowaną, funkcjonalną tkanką, kładąc fundamenty dla reszty ciała.
Cytowanie: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Słowa kluczowe: rozwój embrionalny, wyrównanie komórek, macierz zewnątrzkomórkowa, patternowanie tkanki, powstawanie światła