Clear Sky Science · nl
Rand-gebaseerde celuitlijning stuurt rijping van de muis-epiblast
Hoe weefsels hun vorm vinden
Voordat een muisembryo enige herkenbare vorm aanneemt, moeten de cellen eerst beslissen hoe ze zich organiseren en waar ze de allereerste interne holte uitsnijden. Dit artikel onderzoekt een schijnbaar eenvoudige vraag met grote implicaties: hoe ordent een ogenschijnlijk vormloze bol cellen zichzelf tot een goed geordende structuur die later organen en lichaamsassen kan aanleggen? Door vroege muisembryo’s driedimensionaal te volgen en biologie met fysica te combineren, onthullen de auteurs hoe de randen van een weefsel deze transformatie subtiel choreograferen.
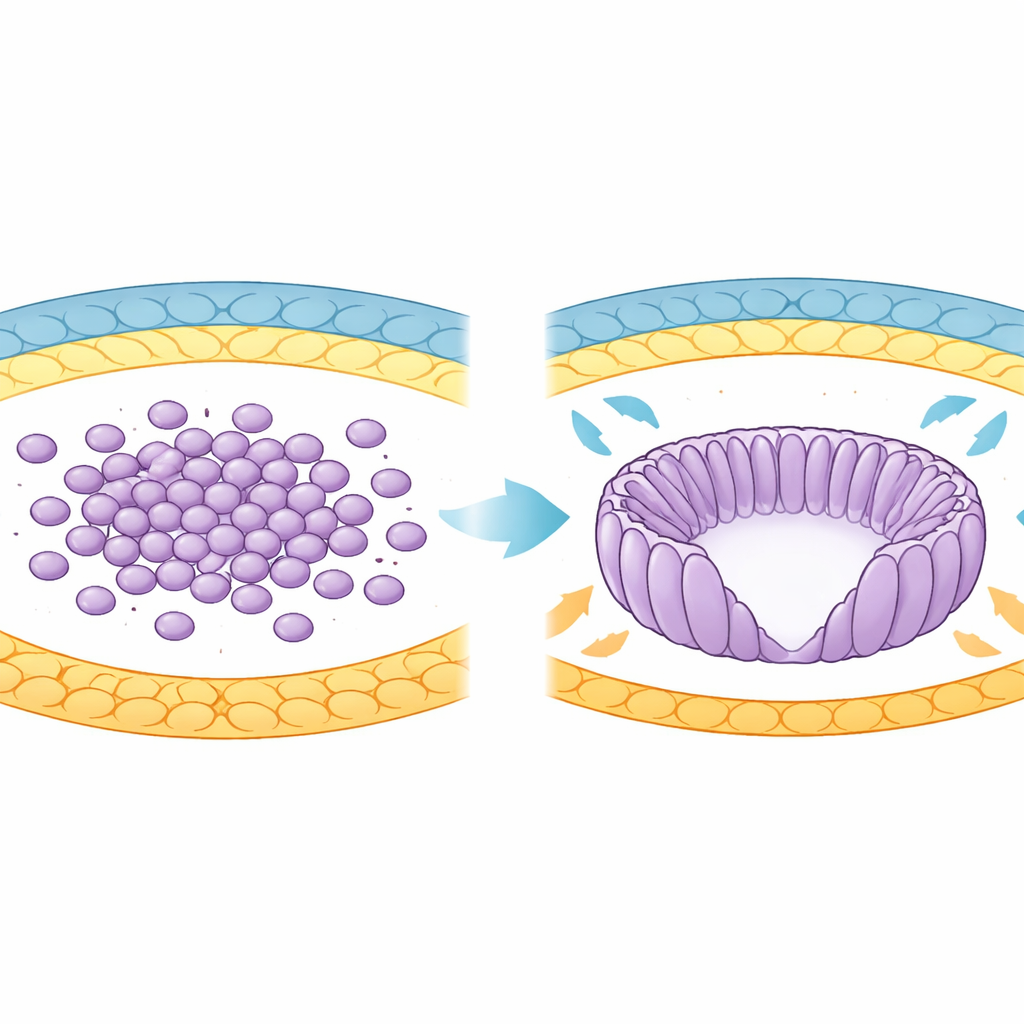
Van celcluster naar georganiseerde kom
In de vroege ontwikkeling ontstaat het toekomstige lichaam van de muis uit een groep cellen die de epiblast wordt genoemd. Aanvankelijk zijn deze cellen rond en los georganiseerd in de blastocyst. Wanneer het embryo in de baarmoeder innestelt, vormt de epiblast zich om tot een komachtige structuur die de eicilinder wordt genoemd. Tijdens deze overgang rekken cellen uit tot langgerekte vormen, lijnen zich op als spaken in een wiel en omringen een centrale holte, de proamniotische holte. De auteurs gebruikten geavanceerde 3D-beelden en computationele analyse om duizenden cellen te volgen terwijl deze vormverandering plaatsvond tussen specifieke ontwikkelingsdagen, en toonden een geleidelijke toename in overeenstemming van oriëntatie tussen naburige cellen.
De invloed van randen en grenzen
De epiblast bestaat niet geïsoleerd. Hij wordt omhuld door twee verschillende weefsels die duidelijke grenzen vormen: één die onderaan de viscerale endoderm zal worden en een andere die bovenaan extra-embryonaal ectoderm wordt. De studie laat zien dat epiblastcellen zich geleidelijk loodrecht oriënteren ten opzichte van de zijde met de viscerale endoderm, maar parallel aan de extra-embryonale zijde. Dit betekent dat waar de epiblast verschillende buren raakt, cellen verschillende voorkeursrichtingen aannemen. Toen de onderzoekers de celoriëntaties over hele embryo’s in kaart brachten, vonden ze dat de uitlijning altijd het sterkst was nabij deze grenzen en zwakker in het midden. Dit patroon suggereerde dat de randen van het weefsel als geleide rails fungeren, cellen aanwijzen welke kant ze op moeten wijzen en uiteindelijk de gehele structuur vormgeven.
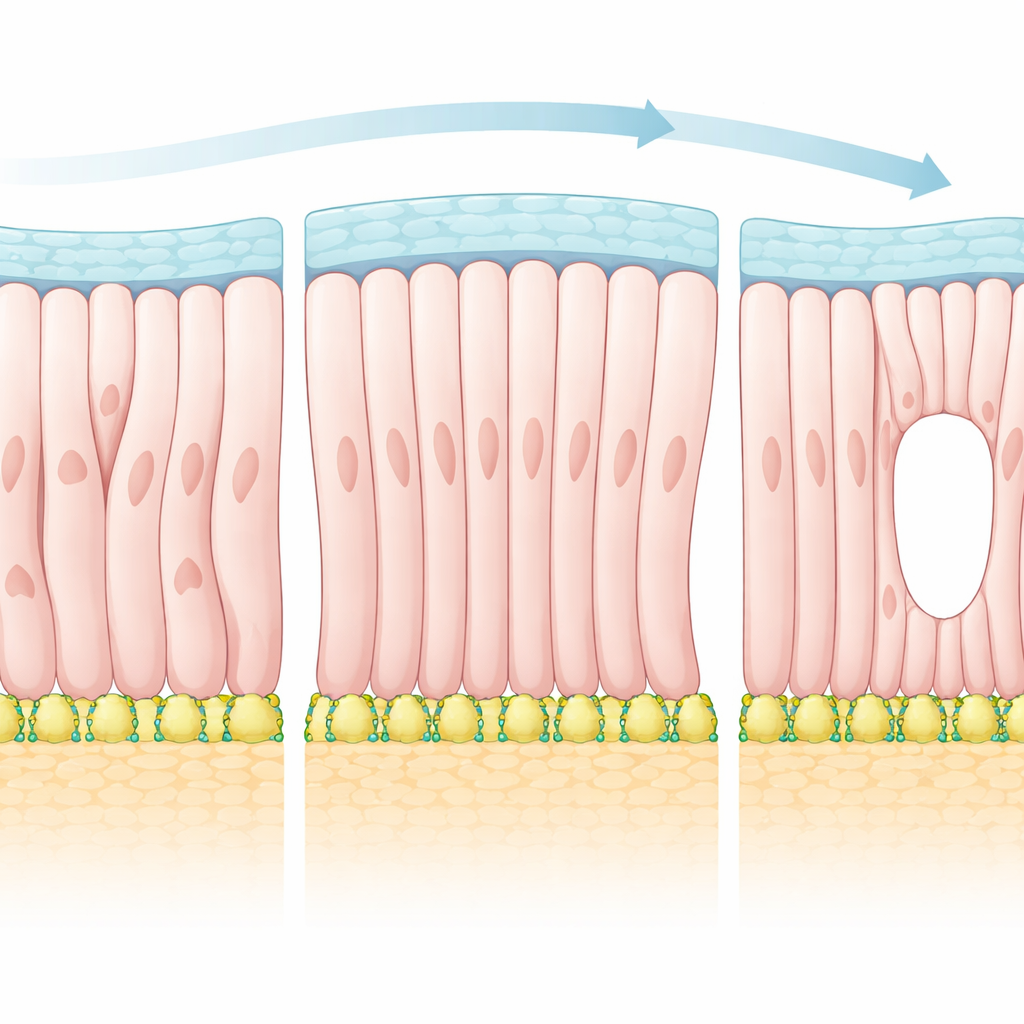
Ideeën geleend van vloeibare kristallen
Om deze waarnemingen te verklaren grepen de auteurs naar een raamwerk dat vaker wordt gebruikt om vloeibare kristallen in schermen te beschrijven. In dergelijke materialen hebben staafvormige moleculen de neiging om zich parallel aan elkaar te scharen, maar hun precieze patroon kan sterk worden beïnvloed door de oppervlakken die hen begrenzen. Het team behandelde epiblastcellen als polaire “deeltjes” die de voorkeur geven aan uitlijning zowel met hun buren als met richtingen die door de omliggende grenzen worden opgelegd. Met deze theorie voorspelden ze dat naarmate de invloed van de randen sterker wordt, het weefsel een overgang zal ondergaan naar een meer geordende toestand met speciale verstoringspunten in het uitlijningsveld — zogenaamde topologische defecten. In het embryo komen deze defecten overeen met plekken waar de apicale zijden van cellen samenkomen en waar de toekomstige holte het eerst opent.
Moleculaire ankers aan de onderrand
Wat zorgt op moleculair niveau voor de sterke invloed van de grens met de viscerale endoderm? De auteurs combineerden single-cell genexpressiegegevens en eiwitkleuringen om te laten zien dat deze onderste grens verrijkt raakt met specifieke componenten van de extracellulaire matrix, met name laminine, en met de actieve vorm van zijn celoppervlaktepartner, integrine β1. Samen functioneren deze als kleine moleculaire ankers voor de basale zijde van epiblastcellen. Naarmate laminine–integrine-adhesie in de tijd aanzwelt aan deze grens, wordt celuitlijning duidelijker en ontstaat een robuust patroon. In computersimulaties wist het verzwakken van deze verankering het geordende patroon uit, wat suggereert dat deze moleculen essentieel zijn zodat het weefsel zijn rand kan ‘voelen’ en erop kan reageren.
Als ankers falen, haperen vorm en signalen
Om dit direct te testen onderzochten de onderzoekers embryo’s die geen laminine γ1 of integrine β1 hadden. In deze mutanten wezen epiblastcellen niet langer loodrecht naar de grens met de viscerale endoderm maar lagen ze in plaats daarvan tangentieel, zoals ze dat ook doen nabij de bovenste grens. Het weefsel verloor zijn karakteristieke radiale uitlijning, rozetachtige clusters van apicale oppervlakken vormden zich niet goed en de initiatieplaatsen voor de lumen werden verstoord. Toch nam de algemene mate van celuitrekking nog steeds toe, wat aangeeft dat het belangrijkste defect lag in de oriëntatie van cellen en niet in hun vermogen om uit te rekken. In een aparte manipulatie verminderde het enzymatisch verzwakken van de matrix aan de onderrand de activiteit van ERK, een signaalroute die belangrijk is voor celgroei en differentiatie, wat suggereert dat correcte weefselpatterning bijdraagt aan het activeren van de moleculaire programma’s die de rijping van de epiblast aandrijven.
Waarom dit belangrijk is voor het bouwen van lichamen
Simpel gezegd toont de studie aan dat de manier waarop vroege embryonale cellen zich uitlijnen niet willekeurig is; ze wordt gestuurd door verschillen aan hun grenzen, vooral door laminine–integrine-adhesie aan de zijde van de viscerale endoderm. Deze rand-geleide uitlijning verklaart waar de eerste holte verschijnt en hoe signalen zoals ERK worden geactiveerd om het embryo verder in de ontwikkeling te brengen. Voor een lezer zonder specialistische kennis is de kernboodschap dat randen niet slechts passieve grenzen zijn: ze zijn actieve organisatoren die helpen een vormeloze klomp cellen te veranderen in een geordend, functioneel weefsel en daarmee het blauwdruk voor de rest van het lichaam uitzetten.
Bronvermelding: Ichikawa, T., Guruciaga, P.C., Hu, S. et al. Boundary-guided cell alignment drives mouse epiblast maturation. Nat. Phys. 22, 461–473 (2026). https://doi.org/10.1038/s41567-026-03176-9
Trefwoorden: embryonale ontwikkeling, celuitlijning, extracellulaire matrix, weefselpatronering, lumenvorming