Clear Sky Science · zh
通过双受体敲除消除CAR T细胞中前列腺素E2信号提升实体肿瘤治疗效果
这项研究对未来癌症治疗为何重要
许多人听说过CAR T细胞疗法,这是一种个性化免疫治疗,能够根除某些血液癌症。然而,同样策略在胰腺癌或结直肠癌等实体肿瘤中效果不佳。本研究探讨了实体肿瘤内部一个被忽视的化学制动——由一种称为前列腺素E2的脂类分子介导——并展示了如何通过精确编辑治疗性T细胞上的两个结合位点,大幅增强其效力,同时不干扰机体其他部位的功能。
对“活体癌症药物”的智能升级
CAR T细胞是从患者体内提取的普通免疫细胞,重新编程以识别癌细胞上的特定标志。在血液恶性肿瘤中,它们可大规模扩增、发动攻击,有时单次输注即可治愈疾病。实体肿瘤则不同:它们被一种称为肿瘤微环境的敌对环境包围,充斥着使T细胞耗竭或瘫痪的物质。其中影响最大的物质之一是前列腺素E2(PGE2),这是一种由许多肿瘤大量产生的脂类信号分子,通常与不良预后相关。与其在全身范围内阻断PGE2——一种在以往药物试验中导致严重副作用的策略——作者们提出了一个问题:能否让CAR T细胞对这一信号“充耳不闻”而不是试图抑制它在体内的所有存在?
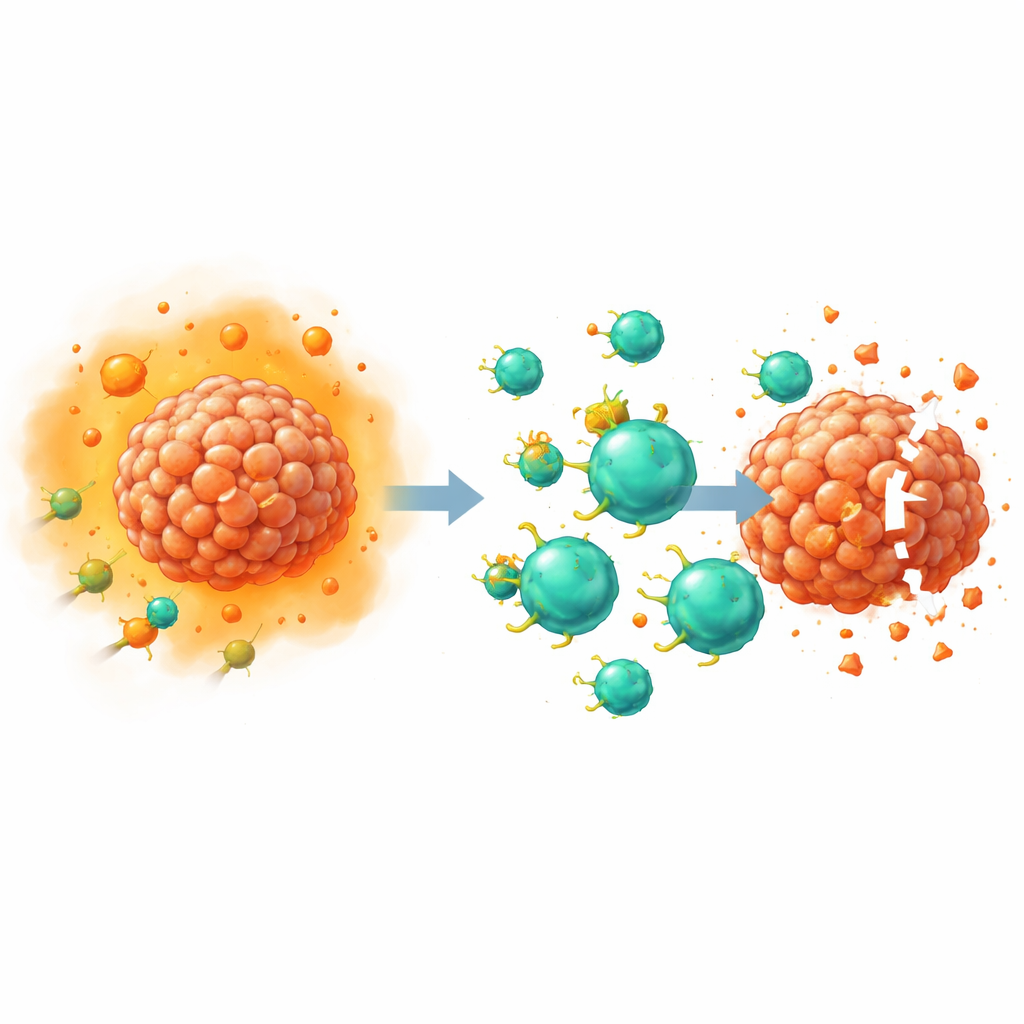
解除一条关键抑制信号
PGE2通过结合细胞表面的四种受体(EP1至EP4)发挥作用。之前该团队及其他研究组的工作表明,T细胞上的EP2和EP4受体对削弱抗肿瘤免疫尤为重要,主要通过干扰细胞对生长因子白细胞介素-2的响应来实现。在这项研究中,研究者使用CRISPR–Cas9基因编辑有选择地从被工程化为CAR T细胞的T细胞中删除了EP2和EP4。由于这些受体用常规实验室抗体难以直接检测,团队通过间接手段验证了编辑效果:在加入高剂量PGE2后,测量下游化学信使(如信号分子cAMP和蛋白质CREB的活化形式)。双重编辑的细胞显示出几乎完全丧失的PGE2信号传导,证实了受体已被有效禁用。
从体外培养到小鼠与患者肿瘤样本
团队首先在细胞培养中测试了他们编辑过的CAR T细胞。当常规CAR T细胞预先暴露于PGE2时,它们的增殖能力和清除癌细胞的效率显著下降,尽管在被激活后每个细胞仍具备杀伤能力。相反,缺失EP2和EP4的CAR T细胞在PGE2存在下仍保持扩增并完全清除肿瘤细胞。这种模式在使用与胰腺癌及其他实体肿瘤相关靶点的小鼠和人体系中均成立。关键差异并非编辑细胞单个更具攻击性,而是更多细胞在抑制性环境中存活并分裂。
在体模型中更强且更持久的应答
随后,研究者将实验推进到动物模型。在携带高PGE2肿瘤的小鼠中,缺失EP2和EP4的T细胞或CAR T细胞在肿瘤内的积累远高于未编辑细胞,而在淋巴结和血液中的数量相似。肿瘤生长减慢、生存期延长,且部分小鼠出现肿瘤完全清除——这是常规CAR T细胞在实体瘤中很少见的结局。使用生物发光报告的成像研究证实,编辑后的CAR T细胞在肿瘤内的扩增更为显著,随后随着肿瘤复生而下降,将肿瘤控制直接与T细胞持久性联系起来。最后,在由结直肠癌、胰腺癌和神经内分泌肿瘤患者肿瘤样本构建的三维培养体系中,双重编辑的CAR T细胞持续比标准CAR T细胞杀死更多肿瘤细胞,强调了该方法的临床相关性。
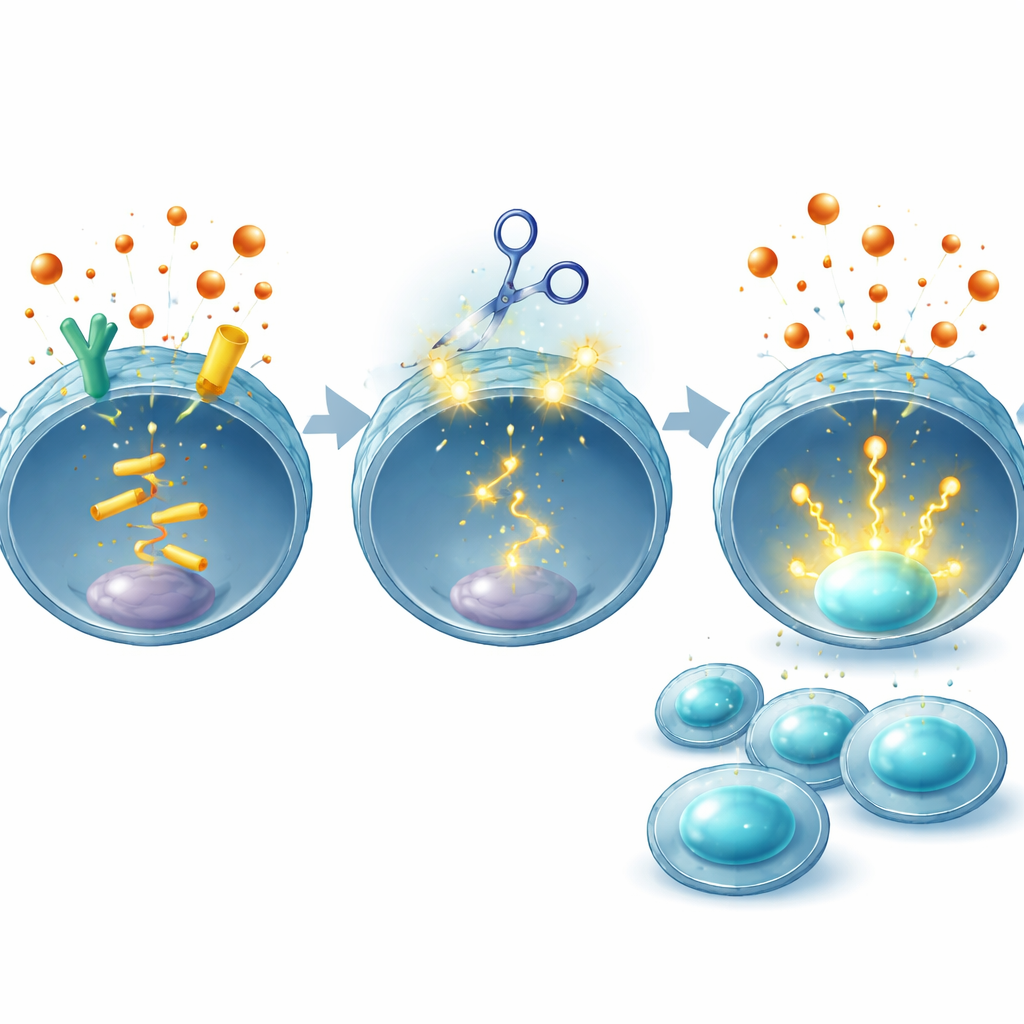
权衡效能与安全性
任何基因编辑策略都带来意外DNA变化的担忧,团队因此进行了广泛检查。利用计算工具和全基因组测序,他们在所检验的供体人源CAR T细胞中搜索脱靶编辑,除预期的EP2和EP4基因外未发现其他编辑。他们还指出,CRISPR编辑的CAR T细胞已在针对其他靶点的患者中开展测试,并未显现明显额外毒性。重要的是,通过只改变T细胞而不在全身范围内阻断PGE2的产生,该策略旨在保留该激素在肠道和肾脏等组织中的正常功能,从而避免困扰系统性药物的副作用。
这对患者可能意味着什么
简单来说,这项工作表明,许多CAR T细胞在实体肿瘤中失败并非因为无法识别靶标,而是因为肿瘤用一种化学“雾”包围它们,使其无法增殖。通过从治疗性细胞上移除两个该“雾”的微小停靠位点——EP2和EP4——科学家可以让这些细胞即便在敌对环境中也继续分裂和发挥作用。该研究为升级CAR T细胞提供了蓝图,使其选择性地对癌症的一种关键沉默信号“充耳不闻”,有望在尽量减少对机体其他部位伤害的同时,提高细胞疗法对某些最致命实体肿瘤的疗效。
引用: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
关键词: CAR T细胞疗法, 实体肿瘤, 前列腺素E2, CRISPR基因编辑, 肿瘤微环境