Clear Sky Science · nl
Uitschakeling van prostaglandine E2-signaal via dubbele receptor-knockout in CAR-T-cellen verbetert therapeutische werkzaamheid bij solide tumoren
Waarom dit onderzoek belangrijk is voor toekomstige kankerbehandelingen
Veel mensen hebben gehoord van CAR-T-celtherapie, een vorm van gepersonaliseerde immunotherapie die bepaalde bloedkankers kan uitroeien. Toch heeft dezelfde strategie moeite gehad bij solide tumoren zoals pancreaskanker of colorectale kanker. Deze studie onderzoekt een verborgen chemische rem binnen solide tumoren — bemiddeld door een vetachtige molecuul genaamd prostaglandine E2 — en laat zien hoe het doelgericht bewerken van twee van diens aanhechtingsplaatsen op therapeutische T-cellen hun werkzaamheid aanzienlijk kan vergroten zonder de rest van het lichaam te verstoren.
Een slimme upgrade voor levende kankergeneesmiddelen
CAR-T-cellen zijn gewone immuuncellen die bij een patiënt worden verzameld en zodanig geherprogrammeerd dat ze een specifiek merkteken op kankercellen herkennen. Bij bloedkankers kunnen ze zich krachtig vermenigvuldigen, aanvallen en soms genezing bewerkstelligen na slechts één infusie. Solide tumoren zijn anders. Ze worden omgeven door een vijandige omgeving, bekend als de tumormicro-omgeving, die vol zit met stoffen die T-cellen uitputten of verlammen. Een van de meest invloedrijke daarvan is prostaglandine E2, of PGE2, een lipide-signaal dat door veel tumoren in hoge hoeveelheden wordt geproduceerd en geassocieerd is met slechte uitkomsten. In plaats van te proberen PGE2 overal in het lichaam te blokkeren — een strategie die in eerdere geneesmiddelproeven ernstige bijwerkingen veroorzaakte — vroegen de auteurs zich af of ze CAR-T-cellen simpelweg ongevoelig konden maken voor dit signaal.
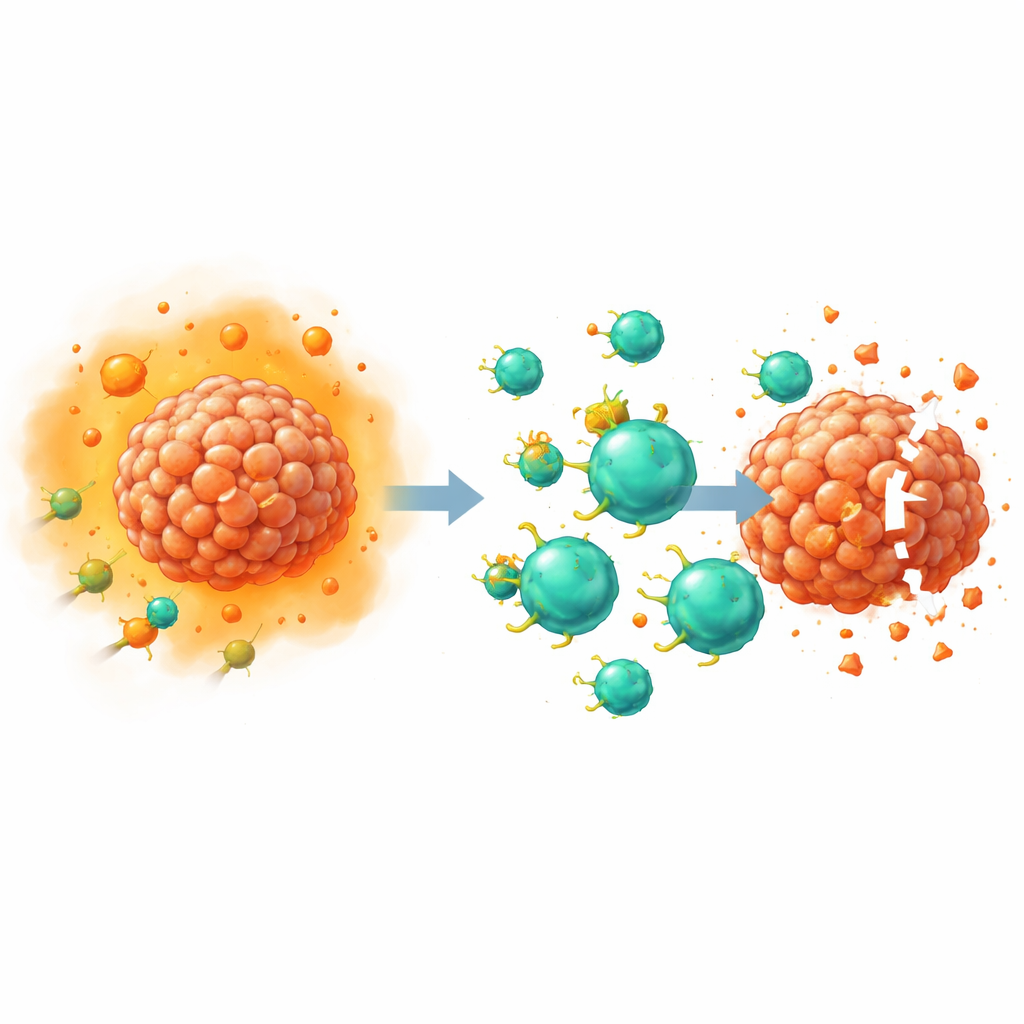
Het neutraliseren van een belangrijk onderdrukkend signaal
PGE2 werkt door te binden aan vier receptoren op celoppervlakken, genaamd EP1 tot en met EP4. Eerder werk van deze en andere groepen toonde aan dat de EP2- en EP4-receptoren op T-cellen bijzonder belangrijk zijn voor het verzwakken van antitumorimmuniteit, grotendeels door het vermogen van cellen om te reageren op de groeifactor interleukine-2 te verstoren. In deze studie gebruikten de onderzoekers CRISPR–Cas9-genbewerking om EP2 en EP4 specifiek uit T-cellen te verwijderen die als CAR-T-cellen waren ontworpen. Omdat deze receptoren moeilijk te detecteren zijn met standaard laboratoriumantistoffen, valideerde het team de bewerkingen indirect: ze maten downstream chemische boodschappers, zoals het signaalmolecuul cAMP en de geactiveerde vorm van een eiwit genaamd CREB, nadat ze hoge doses PGE2 toevoegden. Dubbel bewerkte cellen toonden een bijna volledig verlies van PGE2-signaaltransductie, wat bevestigde dat de receptoren effectief waren uitgeschakeld.
Van petrischaal naar muizen en patiëntentumoren
Het team testte eerst hun bewerkte CAR-T-cellen in celculturen. Wanneer gewone CAR-T-cellen vooraf werden blootgesteld aan PGE2, nam hun vermogen om te vermenigvuldigen en kankercellen te verwijderen sterk af, ook al bleef elke cel in staat om te doden zodra ze geactiveerd waren. Daarentegen bleven CAR-T-cellen zonder zowel EP2 als EP4 zich uitbreiden en elimineerden ze tumorcellen volledig ondanks de aanwezigheid van PGE2. Dit patroon was zowel in muis- als in menselijke systemen zichtbaar bij doelwitten die relevant zijn voor pancreaskanker en andere solide tumoren. Het belangrijkste verschil was niet dat de bewerkte cellen per cel agressiever waren, maar dat er meer van hen overleefden en zich deelden onder onderdrukkende omstandigheden.
Krachtigere en langduriger responsen in levende modellen
Vervolgens gingen de onderzoekers over naar diermodellen. In muizen met PGE2-rijke tumoren stapelden T-cellen of CAR-T-cellen zonder EP2 en EP4 zich in veel grotere aantallen op in de tumoren dan hun onbewerkte tegenhangers, terwijl aantallen in lymfeklieren en bloed vergelijkbaar bleven. Tumorgroei vertraagde, overleving verbeterde en een subset van muizen ervoer volledige tumoruitroei — een uitkomst die zelden wordt gezien met conventionele CAR-T-cellen bij solide kankers. Beeldvormingsstudies met een bioluminescente reporter bevestigden dat bewerkte CAR-T-cellen zich robuuster uitbreidden binnen tumoren voordat ze uiteindelijk afnamen toen tumoren weer teruggroeiden, waarmee tumorcontrole direct werd gekoppeld aan T-celpersistentie. Ten slotte doodden dubbel bewerkte CAR-T-cellen in driedimensionale culturen gemaakt van patiënttumormonsters van colorectale, pancreatische en neuro-endocriene kankers consequent meer tumorcellen dan standaard CAR-T-cellen, wat de klinische relevantie van de benadering onderstreept.
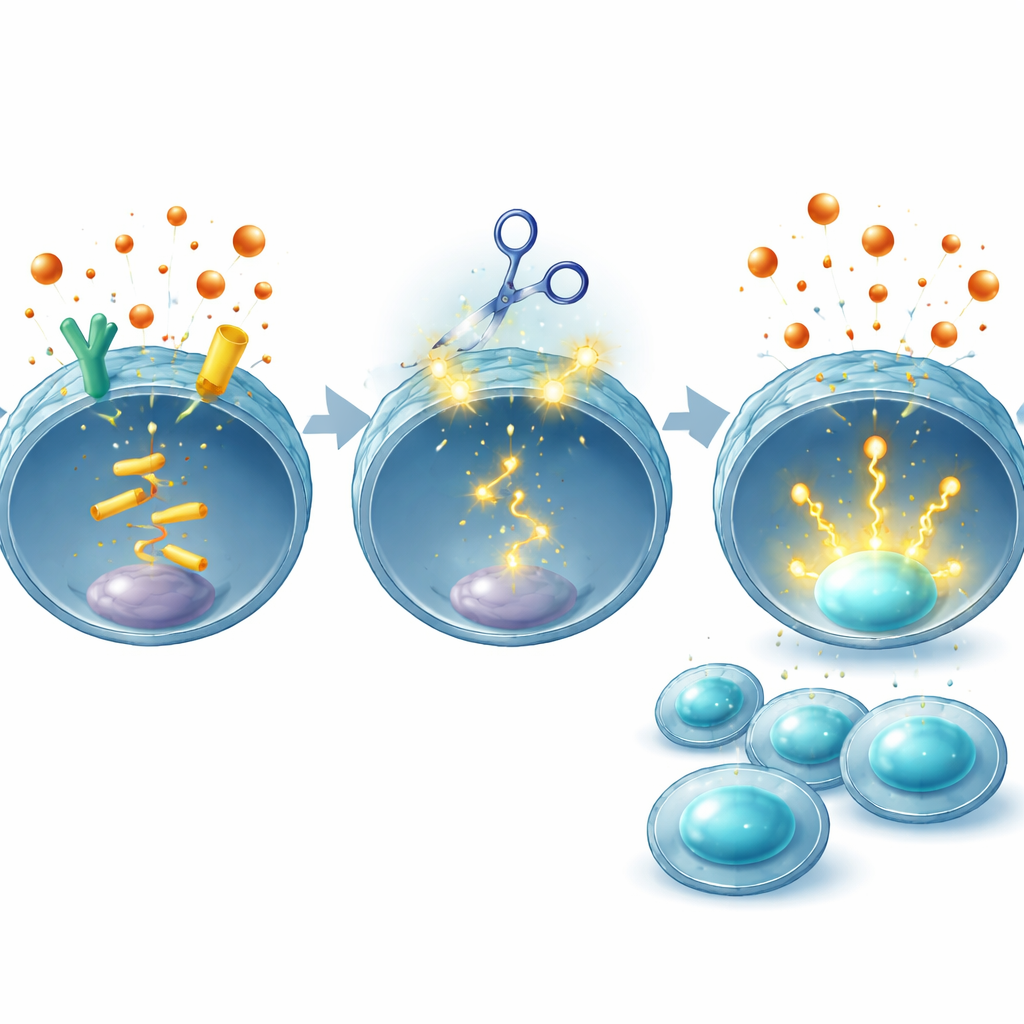
Het balanceren van kracht en veiligheid
Aangezien elke genbewerkingsstrategie zorgen oproept over ongewenste DNA-veranderingen, voerde het team uitgebreide controles uit. Met behulp van computationele tools en whole-genome sequencing zochten ze naar off-target-bewerkingen in humane CAR-T-cellen en vonden ze geen veranderingen buiten de beoogde EP2- en EP4-genen in de donor die ze onderzochten. Ze merkten ook op dat CRISPR-bewerkte CAR-T-cellen al bij patiënten voor andere doelwitten worden getest zonder tot nu toe duidelijke extra toxiciteit. Belangrijk is dat door alleen de T-cellen te veranderen en niet de PGE2-productie in het hele lichaam te blokkeren, deze strategie erop gericht is de normale rollen van het hormoon in weefsels zoals de darm en de nieren te behouden, waardoor bijwerkingen die systemische geneesmiddelen teisterden worden vermeden.
Wat dit voor patiënten zou kunnen betekenen
In eenvoudige bewoordingen laat dit werk zien dat veel CAR-T-cellen falen in solide tumoren niet omdat ze hun doelwitten niet kunnen herkennen, maar omdat de tumor hen in een chemische mist onderdompelt die hen verhindert zich te vermenigvuldigen. Door twee kleine aanhechtingsplaatsen voor die mist — EP2 en EP4 — uit de therapeutische cellen te verwijderen, kunnen wetenschappers hen laten blijven delen en functioneren, zelfs in een vijandige omgeving. De studie biedt een blauwdruk om CAR-T-cellen zodanig te upgraden dat ze selectief ongevoelig zijn voor een van de belangrijkste stiltezenders van kanker, wat mogelijk celtherapieën effectiever maakt tegen enkele van de dodelijkste solide tumoren en tegelijkertijd de schade aan de rest van het lichaam minimaliseert.
Bronvermelding: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Trefwoorden: CAR-T-celtherapie, solide tumoren, prostaglandine E2, CRISPR-genbewerking, tumormicro-omgeving