Clear Sky Science · es
Eliminación de la señalización de prostaglandina E2 mediante doble supresión de receptores en células CAR T mejora la eficacia terapéutica en tumores sólidos
Por qué esta investigación importa para los tratamientos futuros contra el cáncer
Muchos han oído hablar de la terapia con células CAR T, una forma de inmunoterapia personalizada capaz de erradicar ciertos cánceres hematológicos. Sin embargo, la misma estrategia ha fracasado en tumores sólidos como el de páncreas o el colorrectal. Este estudio explora un freno químico oculto dentro de los tumores sólidos—mediado por una molécula lipídica llamada prostaglandina E2—y demuestra cómo editar con precisión dos de sus puntos de unión en las células T terapéuticas puede aumentar notablemente su eficacia sin alterar el resto del organismo.
Una mejora inteligente para fármacos vivos
Las células CAR T son células inmunitarias ordinarias tomadas del paciente y reprogramadas para reconocer un marcador específico en las células cancerosas. En los cánceres de la sangre, pueden expandirse vigorosamente, atacar y, en ocasiones, curar la enfermedad tras una sola infusión. Los tumores sólidos son distintos. Están rodeados por un vecindario hostil, conocido como microambiente tumoral, lleno de sustancias que agotan o paralizan a las células T. Una de las más influyentes es la prostaglandina E2, o PGE2, una señal lipídica producida en gran cantidad por muchos tumores y asociada a malos pronósticos. En lugar de intentar bloquear la PGE2 en todo el cuerpo—una estrategia que ha provocado efectos secundarios graves en ensayos farmacológicos previos—los autores investigaron si podían hacer que las células CAR T simplemente ignoraran esa señal.
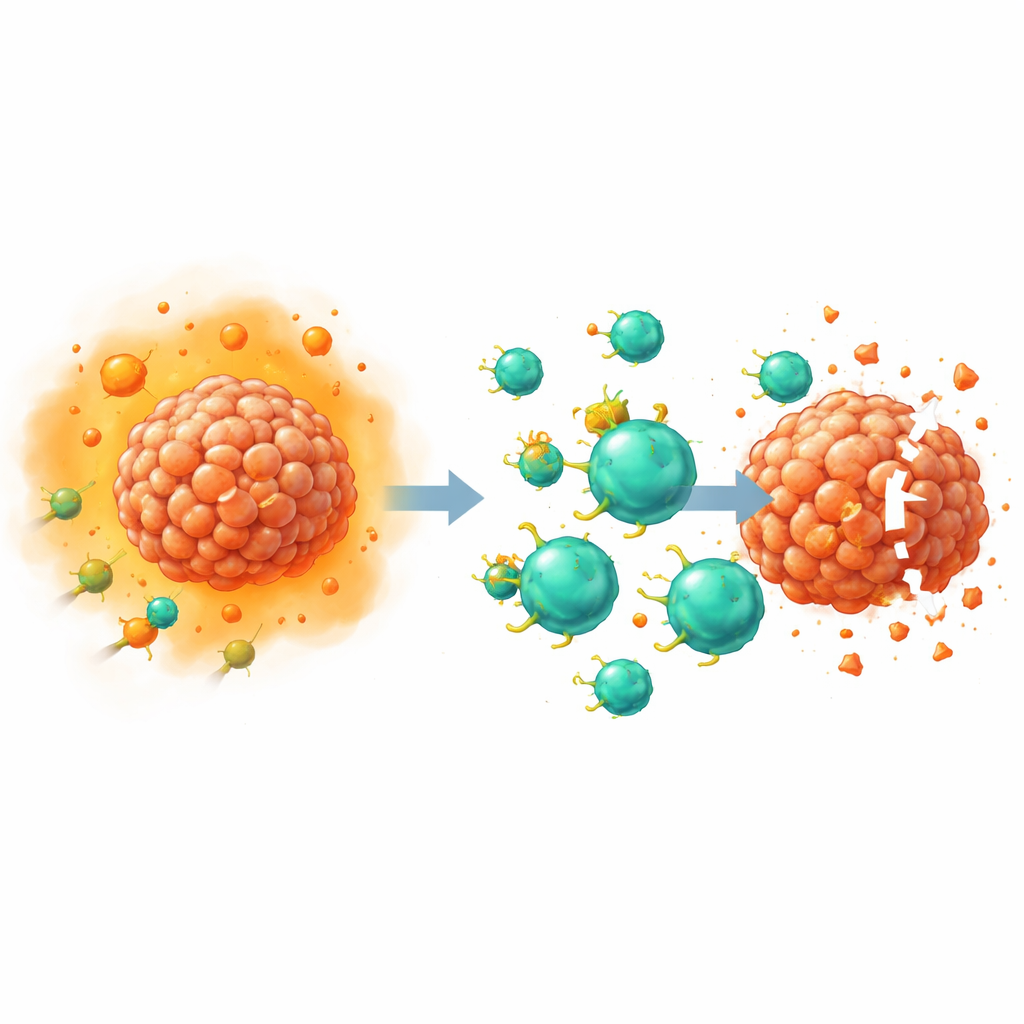
Desarmando una señal supresora clave
La PGE2 actúa uniéndose a cuatro receptores en la superficie celular, denominados EP1 a EP4. Trabajos previos de este y otros grupos mostraron que los receptores EP2 y EP4 en las células T son particularmente importantes para debilitar la inmunidad antitumoral, en gran parte al interrumpir la capacidad de las células para responder al factor de crecimiento interleucina-2. En este estudio, los investigadores usaron edición genética CRISPR–Cas9 para eliminar EP2 y EP4 específicamente de las células T que habían sido modificadas como CAR T. Dado que estos receptores son difíciles de detectar con los anticuerpos de laboratorio estándar, el equipo validó las modificaciones de forma indirecta: midieron mensajeros químicos aguas abajo, como la molécula de señalización cAMP y la forma activada de una proteína llamada CREB, tras añadir dosis altas de PGE2. Las células editadas doblemente mostraron una pérdida casi completa de la señalización por PGE2, confirmando que los receptores habían sido desactivados de forma efectiva.
De las placas de laboratorio a ratones y tumores humanos
El equipo probó primero sus células CAR T editadas en cultivos celulares. Cuando las células CAR T habituales se expusieron previamente a PGE2, su capacidad para multiplicarse y eliminar células cancerosas se redujo drásticamente, aunque cada célula seguía siendo capaz de matar una vez activada. En contraste, las células CAR T que carecían tanto de EP2 como de EP4 continuaron expandiéndose y eliminaron por completo las células tumorales a pesar de la presencia de PGE2. Este patrón se mantuvo tanto en sistemas murinos como humanos usando dianas relevantes para el cáncer de páncreas y otros tumores sólidos. La diferencia clave no fue que las células editadas fueran más agresivas por célula, sino que un mayor número de ellas sobrevivió y se dividió en condiciones supresoras.
Respuestas más fuertes y duraderas en modelos vivos
A continuación, los investigadores pasaron a modelos animales. En ratones con tumores ricos en PGE2, las células T o CAR T sin EP2 y EP4 se acumularon en los tumores en números mucho mayores que sus homólogas no editadas, mientras que los recuentos en ganglios linfáticos y sangre permanecieron similares. El crecimiento tumoral se ralentizó, la supervivencia mejoró y un subconjunto de ratones experimentó la eliminación completa del tumor—un resultado raramente visto con las CAR T convencionales en tumores sólidos. Estudios de imagen usando un reportero bioluminiscente confirmaron que las CAR T editadas se expandieron con mayor fuerza dentro de los tumores antes de disminuir finalmente a medida que los tumores volvían a crecer, vinculando directamente el control tumoral con la persistencia de las células T. Finalmente, en cultivos tridimensionales hechos a partir de muestras tumorales de pacientes con cáncer colorrectal, pancreático y neuroendocrino, las CAR T con doble edición mataron consistentemente más células tumorales que las CAR T estándar, subrayando la relevancia clínica del enfoque.
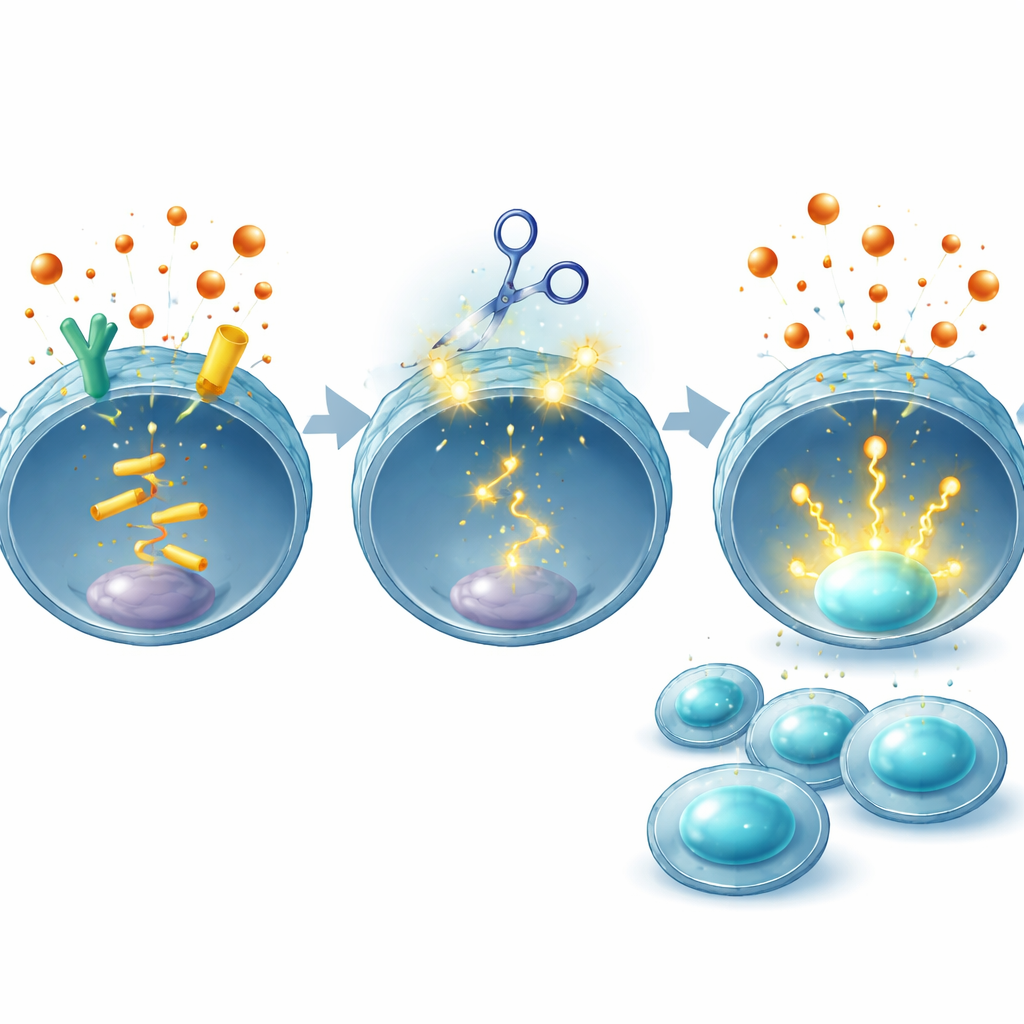
Equilibrando potencia y seguridad
Como cualquier estrategia de edición genética plantea preocupaciones sobre cambios no intencionados en el ADN, el equipo realizó controles extensos. Usando herramientas computacionales y secuenciación del genoma completo, buscaron ediciones fuera de objetivo en células CAR T humanas y no encontraron ninguna más allá de los genes EP2 y EP4 previstos en el donante examinado. También señalaron que las CAR T editadas con CRISPR ya se están probando en pacientes para otros objetivos sin toxicidad adicional clara hasta ahora. De manera importante, al cambiar solo las células T y no bloquear la producción de PGE2 en todo el organismo, esta estrategia pretende preservar los roles normales de esta hormona en tejidos como el intestino y los riñones, evitando los efectos secundarios que han afectado a los fármacos sistémicos.
Qué podría significar esto para los pacientes
En términos sencillos, este trabajo muestra que muchas células CAR T fallan en tumores sólidos no porque no puedan reconocer sus dianas, sino porque el tumor las baña en una niebla química que les impide multiplicarse. Al eliminar dos diminutos puntos de unión para esa niebla—EP2 y EP4—de las células terapéuticas, los científicos pueden permitir que sigan dividiéndose y funcionando incluso en un entorno hostil. El estudio ofrece un plan para mejorar las CAR T de modo que sean selectivamente sordas a una de las señales clave de silenciamiento del cáncer, lo que podría hacer las terapias celulares más eficaces contra algunos de los tumores sólidos más letales, al tiempo que minimiza el daño al resto del organismo.
Cita: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Palabras clave: Terapia con células CAR T, tumores sólidos, prostaglandina E2, edición genética CRISPR, microambiente tumoral