Clear Sky Science · pl
Usunięcie sygnalizacji prostaglandyny E2 przez podwójne zniesienie receptorów w komórkach CAR-T zwiększa skuteczność terapeutyczną w nowotworach litych
Dlaczego te badania mają znaczenie dla przyszłych terapii przeciwnowotworowych
Wielu słyszało o terapii CAR-T, formie spersonalizowanej immunoterapii, która potrafi wyeliminować niektóre nowotwory krwi. Ta sama strategia radzi sobie jednak znacznie gorzej w nowotworach litych, jak rak trzustki czy jelita grubego. W badaniu tym zbadano ukrytą chemiczną „hamulcową” w guzach litych — pośredniczoną przez lipidową cząsteczkę zwaną prostaglandyną E2 — i pokazano, że precyzyjne wyłączenie dwóch jej miejsc wiążących na terapeutycznych limfocytach T może znacząco wzmocnić ich działanie bez zaburzania reszty organizmu.
Sprytna poprawka dla żywych leków przeciwnowotworowych
Komórki CAR-T to zwykłe komórki odpornościowe pobrane od pacjenta i przeprogramowane tak, by rozpoznawały specyficzny marker na komórkach nowotworowych. W nowotworach krwi potrafią się szybko namnażać, atakować i czasem doprowadzić do wyleczenia po jednej infuzji. Nowotwory lite są inne. Otacza je wrogie otoczenie, zwane mikrośrodowiskiem guza, wypełnione substancjami, które wyczerpują lub paraliżują komórki T. Jedną z najsilniejszych z nich jest prostaglandyna E2 (PGE2), lipidowy sygnał produkowany w dużych ilościach przez wiele guzów i związany z gorszymi wynikami. Zamiast próbować blokować PGE2 w całym organizmie — strategii, która w przeszłości powodowała poważne skutki uboczne — autorzy zapytali, czy można sprawić, by komórki CAR-T po prostu ignorowały ten sygnał.
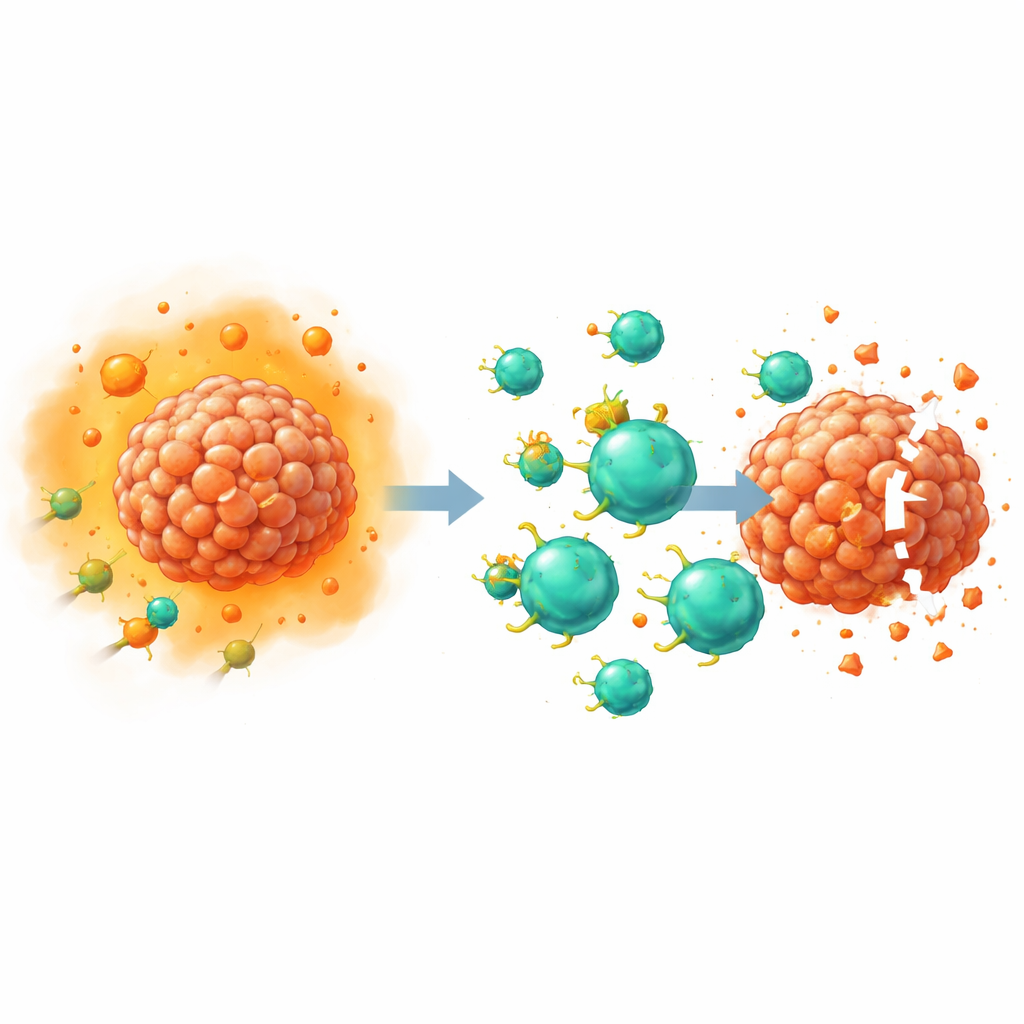
Rozbrajanie kluczowego sygnału supresyjnego
PGE2 działa przez wiązanie się z czterema receptorami na powierzchni komórek, nazwanymi EP1 do EP4. Wcześniejsze badania tej i innych grup wykazały, że receptory EP2 i EP4 na komórkach T są szczególnie ważne dla osłabiania odpowiedzi przeciwnowotworowej, w dużej mierze przez zakłócanie zdolności komórek do reagowania na czynnik wzrostu interleukinę-2. W tym badaniu naukowcy użyli edycji genów CRISPR–Cas9, aby usunąć EP2 i EP4 specyficznie z komórek T zaprojektowanych jako CAR-T. Ponieważ te receptory są trudne do wykrycia standardowymi przeciwciałami laboratoryjnymi, zespół zweryfikował edycje pośrednio: zmierzył stężenia wtórnych przekaźników, takich jak cząsteczka sygnałowa cAMP oraz aktywowana forma białka CREB, po podaniu wysokich dawek PGE2. Komórki z podwójną edycją wykazały prawie całkowitą utratę sygnalizacji PGE2, co potwierdziło skuteczne unieszkodliwienie receptorów.
Z naczyń laboratoryjnych do myszy i guzów pacjentów
Zespół najpierw przetestował edytowane komórki CAR-T w hodowlach komórkowych. Gdy zwykłe komórki CAR-T były uprzednio narażone na PGE2, ich zdolność do namnażania się i eliminowania komórek nowotworowych gwałtownie się zmniejszała, chociaż każda komórka nadal potrafiła zabić, gdy została aktywowana. W przeciwieństwie do tego, komórki CAR-T pozbawione zarówno EP2, jak i EP4 nadal się namnażały i całkowicie eliminowały komórki nowotworowe pomimo obecności PGE2. Schemat ten utrzymywał się zarówno w systemach mysich, jak i ludzkich, przy użyciu celów istotnych dla raka trzustki i innych nowotworów litych. Kluczowa różnica polegała nie na tym, że edytowane komórki były bardziej agresywne pojedynczo, lecz że więcej z nich przeżywało i dzieliło się w warunkach supresyjnych.
Mocniejsze i dłużej utrzymujące się odpowiedzi w modelach żywych
Następnie badacze przeszli do modeli zwierzęcych. U myszy z guzami bogatymi w PGE2, komórki T lub CAR-T pozbawione EP2 i EP4 gromadziły się w guzach w znacznie większych liczbach niż ich nieedytowane odpowiedniki, podczas gdy liczebność w węzłach chłonnych i krwi pozostawała podobna. Tempo wzrostu guza spowolniło, przeżywalność poprawiła się, a u części myszy stwierdzono całkowite oczyszczenie guza — wynik rzadko obserwowany przy konwencjonalnych komórkach CAR-T w nowotworach litych. Badania obrazowe z użyciem bioluminescencyjnego markera potwierdziły, że edytowane komórki CAR-T rozmnażały się bardziej intensywnie wewnątrz guzów, zanim ostatecznie ich liczba spadła w miarę odrastania guza, co bezpośrednio łączy kontrolę guza z utrzymaniem się komórek T. Wreszcie, w trójwymiarowych hodowlach przygotowanych z próbek guzów pacjentów z rakiem jelita grubego, trzustki i nowotworami neuroendokrynnymi, komórki CAR-T z podwójną edycją konsekwentnie zabijały więcej komórek nowotworowych niż standardowe CAR-T, podkreślając kliniczne znaczenie podejścia.
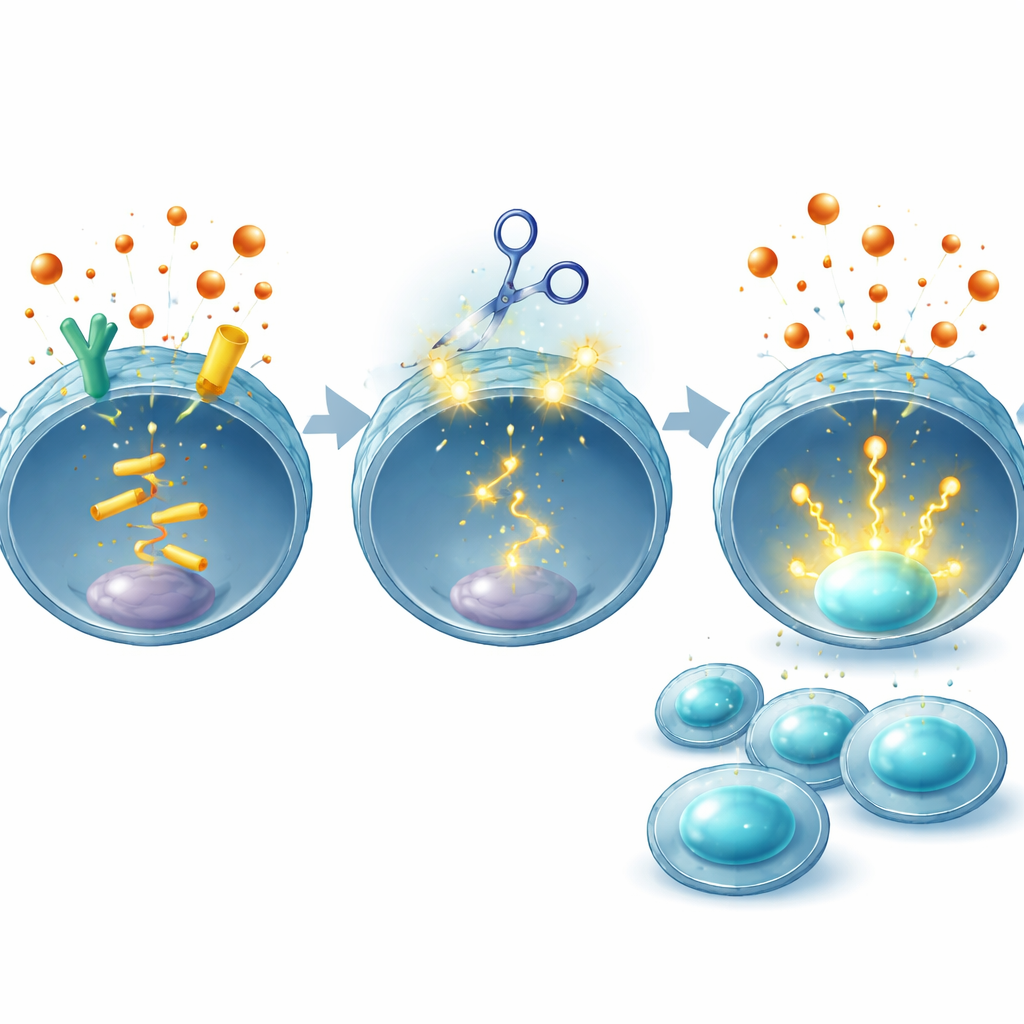
Równoważenie siły i bezpieczeństwa
Ponieważ każda strategia edycji genów budzi obawy o niezamierzone zmiany DNA, zespół przeprowadził obszerne kontrole. Przy użyciu narzędzi obliczeniowych i sekwencjonowania całego genomu poszukiwali niezamierzonych edycji w ludzkich komórkach CAR-T i nie znaleźli ich poza zamierzonymi genami EP2 i EP4 u badanego dawcy. Zauważyli również, że komórki CAR-T edytowane metodą CRISPR są już testowane u pacjentów w kontekście innych celów bez wyraźnego wzrostu toksyczności jak dotąd. Co ważne, zmieniając jedynie same komórki T, a nie blokując produkcji PGE2 w całym organizmie, strategia ta ma na celu zachowanie fizjologicznych ról tej hormonu w tkankach takich jak jelito czy nerki, unikając skutków ubocznych, które nękały leki działające systemowo.
Co to może znaczyć dla pacjentów
Mówiąc prosto, praca ta pokazuje, że wiele komórek CAR-T nie radzi sobie w nowotworach litych nie dlatego, że nie rozpoznają swoich celów, lecz dlatego, że guz kąpie je w chemicznej mgle, która przestaje je mnożyć. Poprzez usunięcie dwóch niewielkich miejsc przyłączania dla tej mgły — EP2 i EP4 — z komórek terapeutycznych, naukowcy pozwalają im nadal się dzielić i działać nawet w wrogim środowisku. Badanie dostarcza planu poprawy komórek CAR-T, dzięki czemu stają się selektywnie głuche na jeden z kluczowych sygnałów wyciszających raka, co potencjalnie może uczynić terapie komórkowe bardziej skutecznymi wobec niektórych z najbardziej śmiercionośnych nowotworów litych przy jednoczesnym zminimalizowaniu szkód dla reszty organizmu.
Cytowanie: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Słowa kluczowe: terapia komórkami CAR-T, nowotwory lite, prostaglandyna E2, edytowanie genów CRISPR, mikrośrodowisko guza