Clear Sky Science · ru
Устранение сигнализации простагландина E2 через двойной нокаут рецепторов в CAR‑T клетках повышает терапевтическую эффективность при солидных опухолях
Почему это исследование важно для будущих методов лечения рака
Многие слышали о терапии CAR‑T клетками — виде персонализированной иммунотерапии, который способен уничтожать некоторые кровяные раки. Однако тот же подход сталкивается с трудностями при лечении солидных опухолей, таких как рак поджелудочной железы или колоректальный рак. В этом исследовании изучается скрытый химический «тормоз» внутри солидных опухолей — опосредованный жироподобной молекулой простагландином E2 — и показано, что точечное удаление двух её сайтов связывания на терапевтических T‑клетках может значительно усилить их эффективность, не нарушая функций всего организма.
Разумное улучшение «живых» противораковых препаратов
CAR‑T клетки — это обычные иммунные клетки, взятые у пациента и перепрограммированные для распознавания специфического маркера на раковых клетках. При кровяных злокачественных новообразованиях они могут интенсивно разрастаться, атаковать и иногда излечивать болезнь после одной инфузии. Солидные опухоли иные: они окружены враждебным микроокружением, наполненным веществами, которые истощают или парализуют T‑клетки. Одним из самых влиятельных факторов здесь является простагландин E2, или PGE2 — липидный сигнал, вырабатываемый во многих опухолях в больших количествах и связанный с плохим прогнозом. Вместо того чтобы блокировать PGE2 по всему организму — стратегия, вызывавшая серьёзные побочные эффекты в предыдущих клинических испытаниях — авторы задали вопрос, можно ли сделать так, чтобы CAR‑T клетки просто игнорировали этот сигнал.
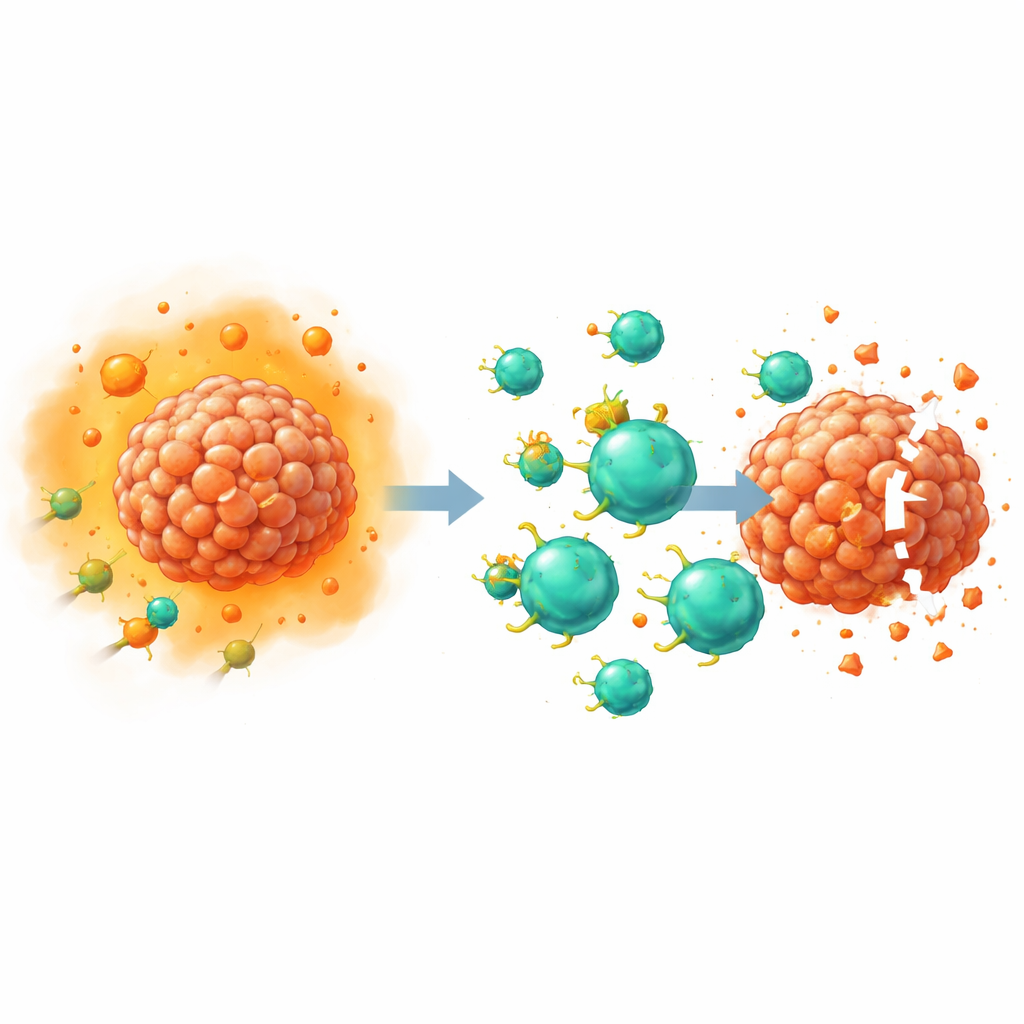
Обезвреживание ключевого супрессивного сигнала
PGE2 действует, связываясь с четырьмя рецепторами на поверхности клеток, называемыми EP1–EP4. Ранее проведённые исследования, в том числе авторами этой работы, показали, что рецепторы EP2 и EP4 на T‑клетках особенно важны для ослабления противоопухолевого иммунитета, главным образом через нарушение способности клеток отвечать на ростовой фактор интерлейкин‑2. В данном исследовании учёные использовали редактирование CRISPR–Cas9, чтобы удалить EP2 и EP4 непосредственно в T‑клетках, переработанных в CAR‑T. Поскольку эти рецепторы трудно обнаружить стандартными лабораторными антителами, команда валидации провела косвенные проверки: измеряли уровни внутриклеточных вторичных посредников, таких как сигнал cAMP и активная форма белка CREB, после добавления высоких доз PGE2. Двойная модификация приводила к почти полному исчезновению PGE2‑сигнализации, что подтверждало эффективное выключение рецепторов.
От чашек Петри до мышей и опухолей пациентов
Сначала команда протестировала отредактированные CAR‑T клетки в культурах клеток. Когда обычные CAR‑T клетки предварительно подвергали воздействию PGE2, их способность размножаться и устранять раковые клетки резко падала, хотя каждая клетка по‑прежнему могла убивать после активации. Напротив, CAR‑T клетки без EP2 и EP4 продолжали расширяться и полностью уничтожали опухолевые клетки, несмотря на присутствие PGE2. Этот эффект наблюдался в как мышиных, так и человеческих системах с мишенями, релевантными для рака поджелудочной железы и других солидных опухолей. Главное отличие заключалось не в том, что отредактированные клетки были «агрессивнее» на одну клетку, а в том, что их больше выживало и делилось в условиях супрессии.
Более сильные и длительные ответы в живых моделях
Далее исследователи перешли к животным моделям. У мышей с опухолями, богатыми PGE2, T‑клетки или CAR‑T клетки без EP2 и EP4 значительно в большей степени накапливались в опухолях по сравнению с немодифицированными аналогами, тогда как их число в лимфоузлах и крови оставалось сопоставимым. Рост опухолей замедлялся, выживаемость улучшалась, и у части животных наблюдалось полное очищение опухоли — результат, редко достигаемый при использовании обычных CAR‑T клеток против солидных опухолей. Исследования с биолюминесцентным репортером подтвердили, что отредактированные CAR‑T клетки внутри опухолей размножаются более активно, прежде чем их число со временем снижается по мере возвращения опухолей, что напрямую связывает контроль опухоли с устойчивостью T‑клеток. Наконец, в трёхмерных культурах, полученных из образцов опухолей пациентов с колоректальным, поджелудочно‑кишечным и нейроэндокринным раком, двойная модификация CAR‑T клеток последовательно приводила к более высокому уничтожению опухолевых клеток по сравнению со стандартными CAR‑T, подчёркивая клиническую значимость подхода.
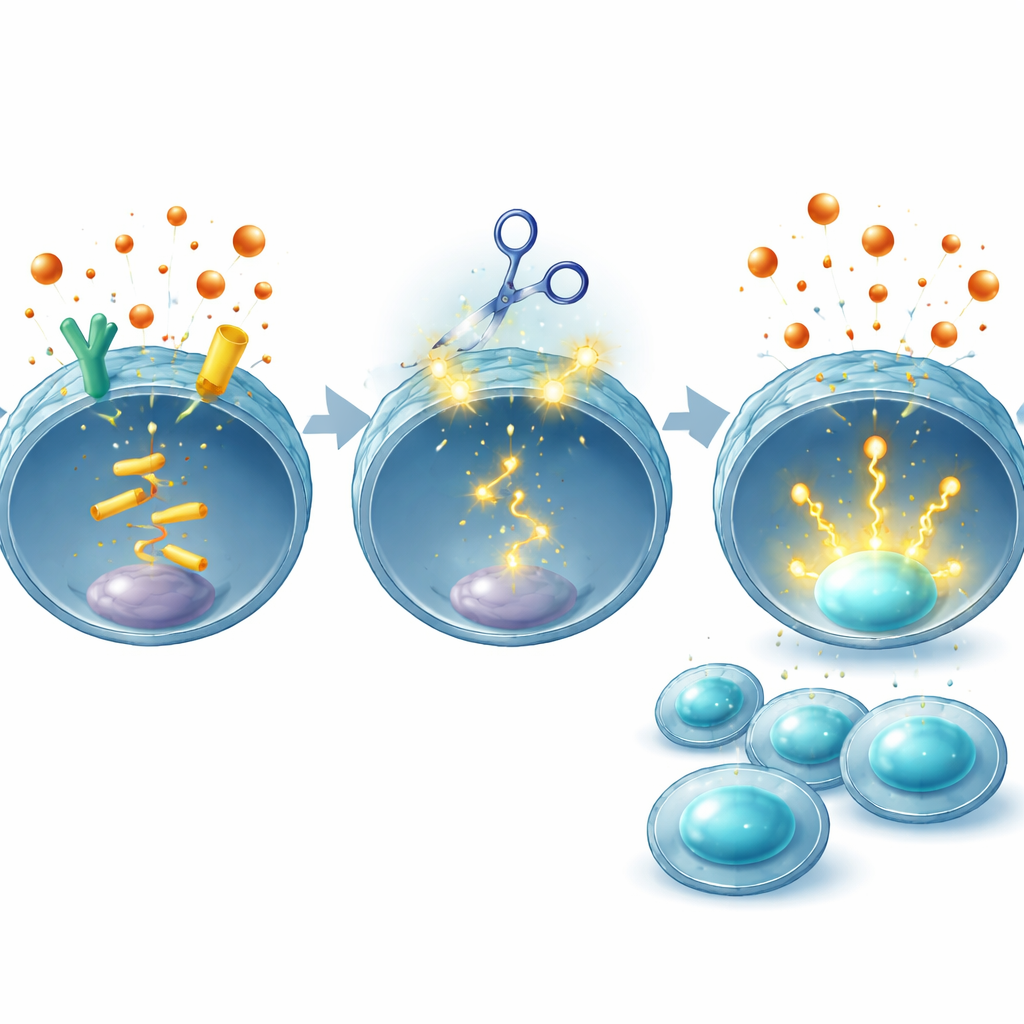
Баланс силы и безопасности
Поскольку любая стратегия редактирования генов вызывает опасения по поводу непреднамеренных изменений ДНК, команда провела обширные проверки. С помощью вычислительных инструментов и секвенирования всего генома они искали побочные правки в человеческих CAR‑T клетках и не обнаружили таковых за пределами целевых генов EP2 и EP4 в доноре, которого они анализировали. Они также отметили, что CRISPR‑отредактированные CAR‑T клетки уже тестируются у пациентов для других мишеней без явного дополнительного токсического эффекта на текущем этапе. Важно, что модифицируя только сами T‑клетки, а не блокируя производство PGE2 по всему организму, этот подход нацелен на сохранение нормальных функций гормона в тканях, таких как кишечник и почки, что помогает избегать побочных эффектов, сопровождавших системные препараты.
Что это может значить для пациентов
Проще говоря, работа показывает: многие CAR‑T клетки терпят неудачу в солидных опухолях не потому, что не распознают свои мишени, а потому что опухоль окутывает их химическим «туманом», который останавливает их размножение. Удалив два крошечных сайта связывания этого «тумана» — EP2 и EP4 — из терапевтических клеток, учёные дают им возможность продолжать делиться и работать даже в враждебной среде. Исследование предлагает план обновления CAR‑T клеток, делая их селективно нечувствительными к одному из ключевых подавляющих сигналов рака, что потенциально может повысить эффективность клеточных терапий против некоторых из самых смертоносных солидных опухолей при минимизации вреда для остального организма.
Цитирование: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Ключевые слова: терапия CAR‑T клетками, солидные опухоли, простагландин E2, редактирование генов CRISPR, микроокружение опухоли