Clear Sky Science · sv
Avlägsnande av prostaglandin E2‑signalering genom dubbel receptor‑knockout i CAR‑T‑celler förbättrar terapeutisk effektivitet i solida tumörer
Varför denna forskning spelar roll för framtida cancerbehandlingar
Många har hört talas om CAR‑T‑cellterapi, en form av personaliserad immunterapi som kan utrota vissa blodcancerformer. Samma strategi har dock haft svårt att lyckas mot solida tumörer som bukspottkörtel‑ eller kolorektalcancer. Denna studie undersöker en dold kemisk broms inne i solida tumörer — medierad av en fettsyra‑liknande molekyl kallad prostaglandin E2 — och visar hur noggrann borttagning av två av dess bindningsställen på terapeutiska T‑celler markant kan öka deras kraft utan att rubba resten av kroppen.
En smart uppgradering av levande cancermediciner
CAR‑T‑celler är vanliga immunceller som tas från en patient och omprogrammeras för att känna igen en specifik markör på cancerceller. I blodcancer kan de expandera kraftigt, attackera och ibland bota sjukdomen efter bara en infusion. Solida tumörer är annorlunda. De omges av ett fientligt kvarter, känt som tumörmikromiljön, som är fyllt med ämnen som uttröttar eller paralyserar T‑celler. En av de mest inflytelserika av dessa är prostaglandin E2, eller PGE2, en lipid‑signal som produceras i höga mängder av många tumörer och som är kopplad till sämre prognos. Istället för att försöka blockera PGE2 överallt i kroppen — en strategi som tidigare läkemedelsprövningar visat allvarliga biverkningar med — frågade författarna om de kunde få CAR‑T‑celler att helt enkelt ignorera denna signal.
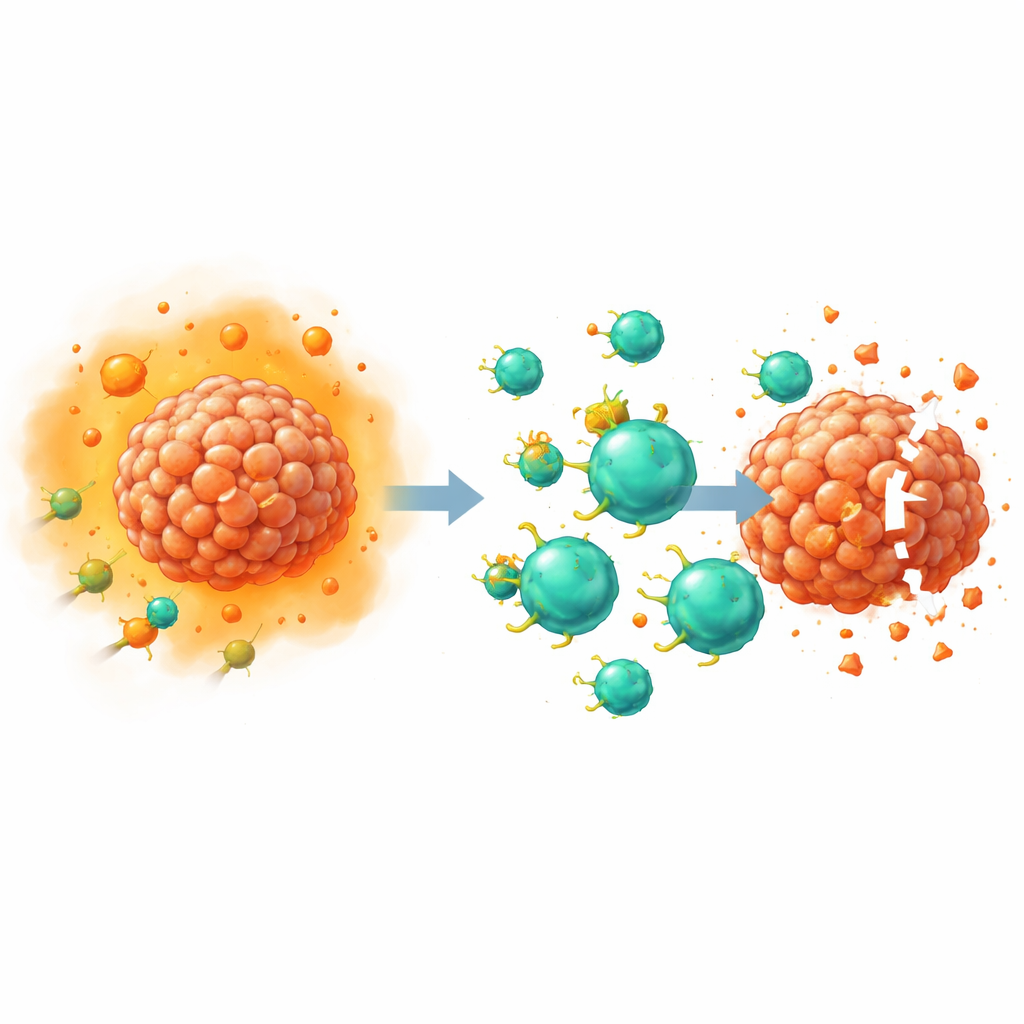
Avväpna en nyckelsuppressiv signal
PGE2 verkar genom att binda till fyra receptorer på cellytan, kallade EP1 till EP4. Tidigare arbete från denna och andra grupper visade att EP2‑ och EP4‑receptorerna på T‑celler är särskilt viktiga för att försvaga antitumoral immunitet, främst genom att störa cellernas förmåga att svara på tillväxtfaktorn interleukin‑2. I denna studie använde forskarna CRISPR–Cas9‑gennedskärning för att ta bort EP2 och EP4 specifikt från T‑celler som hade konstruerats till CAR‑T‑celler. Eftersom dessa receptorer är svåra att upptäcka med vanliga laboratorieantikroppar validerade teamet förändringarna indirekt: de mätte nedströms kemiska budbärare, såsom signalmolekylen cAMP och den aktiverade formen av proteinet CREB, efter tillsats av höga doser PGE2. Dubbelredigerade celler visade en nästan total förlust av PGE2‑signalering, vilket bekräftade att receptorerna effektivt hade inaktiverats.
Från odlingsskålar till möss och patienttumörer
Teamet testade först sina redigerade CAR‑T‑celler i cellodlingar. När vanliga CAR‑T‑celler förbehandlades med PGE2 minskade deras förmåga att multiplicera och rensa bort cancerceller kraftigt, även om varje enskild cell fortfarande kunde döda när den aktiverades. I kontrast fortsatte CAR‑T‑celler utan både EP2 och EP4 att expandera och eliminerade fullt ut tumörceller trots närvaro av PGE2. Detta mönster gällde i både mus‑ och mänskliga system med mål relevanta för bukspottkörtelcancer och andra solida tumörer. Den avgörande skillnaden var inte att de redigerade cellerna var mer aggressiva per cell, utan att fler av dem överlevde och delade sig under suppressiva förhållanden.
Starkare och mer långvariga svar i levande modeller
Sedan gick forskarna vidare till djurmodeller. Hos möss med PGE2‑rika tumörer ackumulerades T‑celler eller CAR‑T‑celler utan EP2 och EP4 i tumörer i mycket högre antal än deras oredigerade motsvarigheter, medan antalet i lymfknutor och blod förblev liknande. Tumörtillväxten försenades, överlevnaden förbättrades, och en delmängd av mössen upplevde komplett tumörrensning — ett utfall som sällan ses med konventionella CAR‑T‑celler i solida cancerformer. Avbildningsstudier med en bioluminescent reporter bekräftade att de redigerade CAR‑T‑cellerna expanderade mer robust inne i tumörer innan de så småningom avtog när tumörerna växte tillbaka, vilket direkt kopplade tumörkontroll till T‑cellspersistens. Slutligen, i tredimensionella odlingar gjorda av patienttumörprover från kolorektal, pankreas‑ och neuroendokrina cancerformer, dödade dubbelredigerade CAR‑T‑celler konsekvent fler tumörceller än standard CAR‑T‑celler, vilket understryker metodens kliniska relevans.
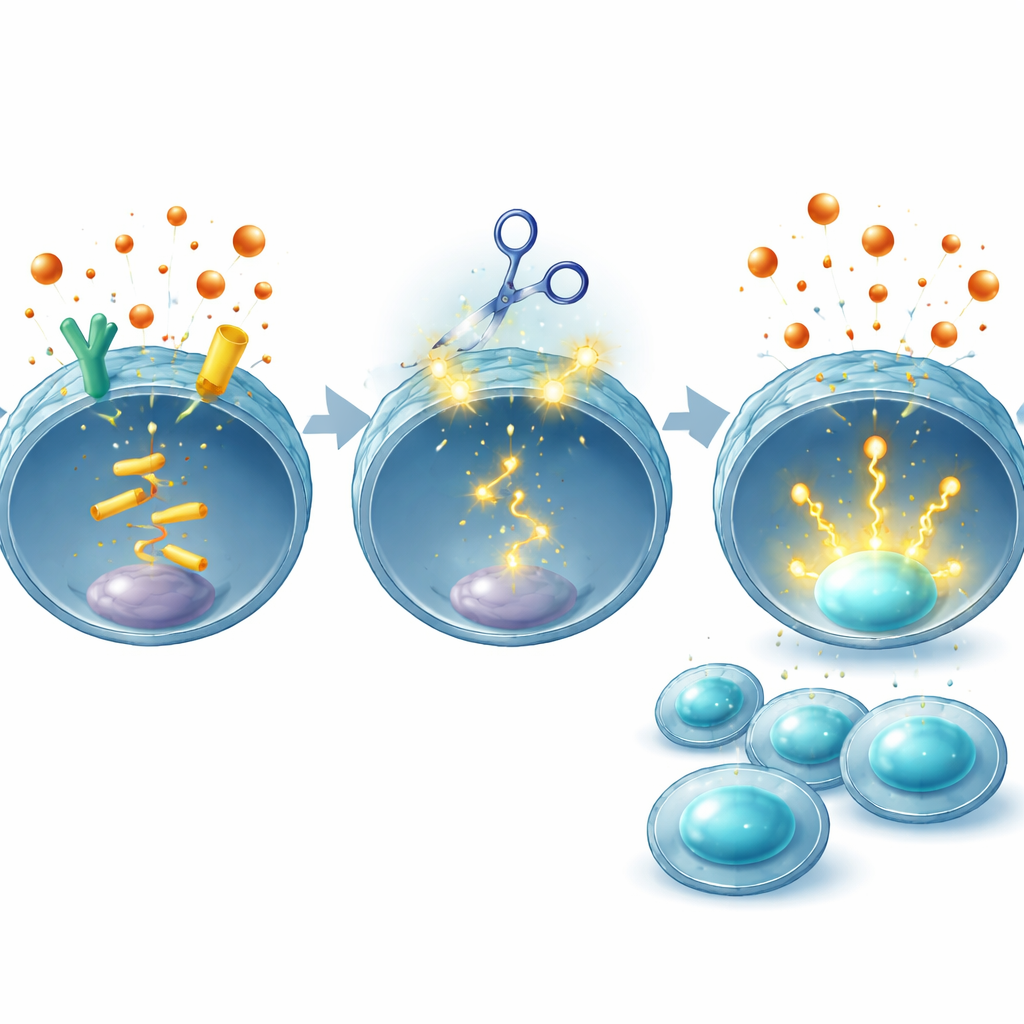
Balans mellan kraft och säkerhet
Eftersom varje genterapistrategi väcker oro för oavsiktliga DNA‑förändringar utförde teamet omfattande kontroller. Med hjälp av beräkningsverktyg och helgenomsekvensering sökte de efter off‑target‑redigeringar i mänskliga CAR‑T‑celler och fann inga utöver de avsedda EP2‑ och EP4‑generna i den givare de undersökte. De noterade också att CRISPR‑redigerade CAR‑T‑celler redan testas i patienter för andra mål utan tydligt tillagd toxicitet hittills. Viktigt är att genom att bara förändra T‑cellerna och inte blockera PGE2‑produktionen i hela kroppen, syftar denna strategi till att bevara hormonets normala roller i vävnader som tarm och njure och undvika biverkningar som plågat systemiska läkemedel.
Vad detta kan betyda för patienter
Enkelt uttryckt visar detta arbete att många CAR‑T‑celler misslyckas i solida tumörer inte för att de inte kan känna igen sina mål, utan för att tumören badar dem i en kemisk dimma som hindrar dem från att multiplicera. Genom att ta bort två små bindningsställen för den dimman — EP2 och EP4 — från de terapeutiska cellerna kan forskare låta dem fortsätta dela sig och fungera även i en fientlig omgivning. Studien ger en ritning för att uppgradera CAR‑T‑celler så att de selektivt är döva för en av cancerns viktiga tystnadssignaler, vilket potentiellt kan göra cellterapier mer effektiva mot några av de farligaste solida tumörerna samtidigt som skador på resten av kroppen minimeras.
Citering: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Nyckelord: CAR‑T‑cellbehandling, solida tumörer, prostaglandin E2, CRISPR‑genterapi, tumörmikromiljö