Clear Sky Science · fr
Élimination de la signalisation de la prostaglandine E2 par suppression double des récepteurs dans les cellules CAR T améliore l’efficacité thérapeutique contre les tumeurs solides
Pourquoi cette recherche compte pour les traitements du cancer à venir
Beaucoup de gens ont entendu parler de la thérapie par cellules CAR T, une forme d’immunothérapie personnalisée capable d’éradiquer certains cancers du sang. Pourtant, la même stratégie a rencontré des difficultés dans les tumeurs solides comme le cancer du pancréas ou colorectal. Cette étude explore un frein chimique caché au sein des tumeurs solides — médié par une molécule lipidique appelée prostaglandine E2 — et montre comment l’édition ciblée de deux de ses sites d’accrochage sur les cellules T thérapeutiques peut considérablement renforcer leur efficacité sans perturber le reste de l’organisme.
Une mise à niveau intelligente des médicaments vivants contre le cancer
Les cellules CAR T sont des cellules immunitaires ordinaires prélevées chez un patient et reprogrammées pour reconnaître un marqueur spécifique des cellules cancéreuses. Dans les cancers du sang, elles peuvent s’amplifier vigoureusement, attaquer et parfois guérir la maladie après une seule perfusion. Les tumeurs solides diffèrent. Elles sont entourées d’un environnement hostile, appelé microenvironnement tumoral, rempli de substances qui épuisent ou paralysent les cellules T. L’une des plus influentes est la prostaglandine E2, ou PGE2, un signal lipidique produit en grande quantité par de nombreuses tumeurs et associé à de mauvais pronostics. Plutôt que de tenter de bloquer la PGE2 dans tout le corps — une stratégie qui a entraîné de graves effets secondaires lors d’essais de médicaments antérieurs — les auteurs se sont demandé s’il était possible de rendre les cellules CAR T simplement insensibles à ce signal.
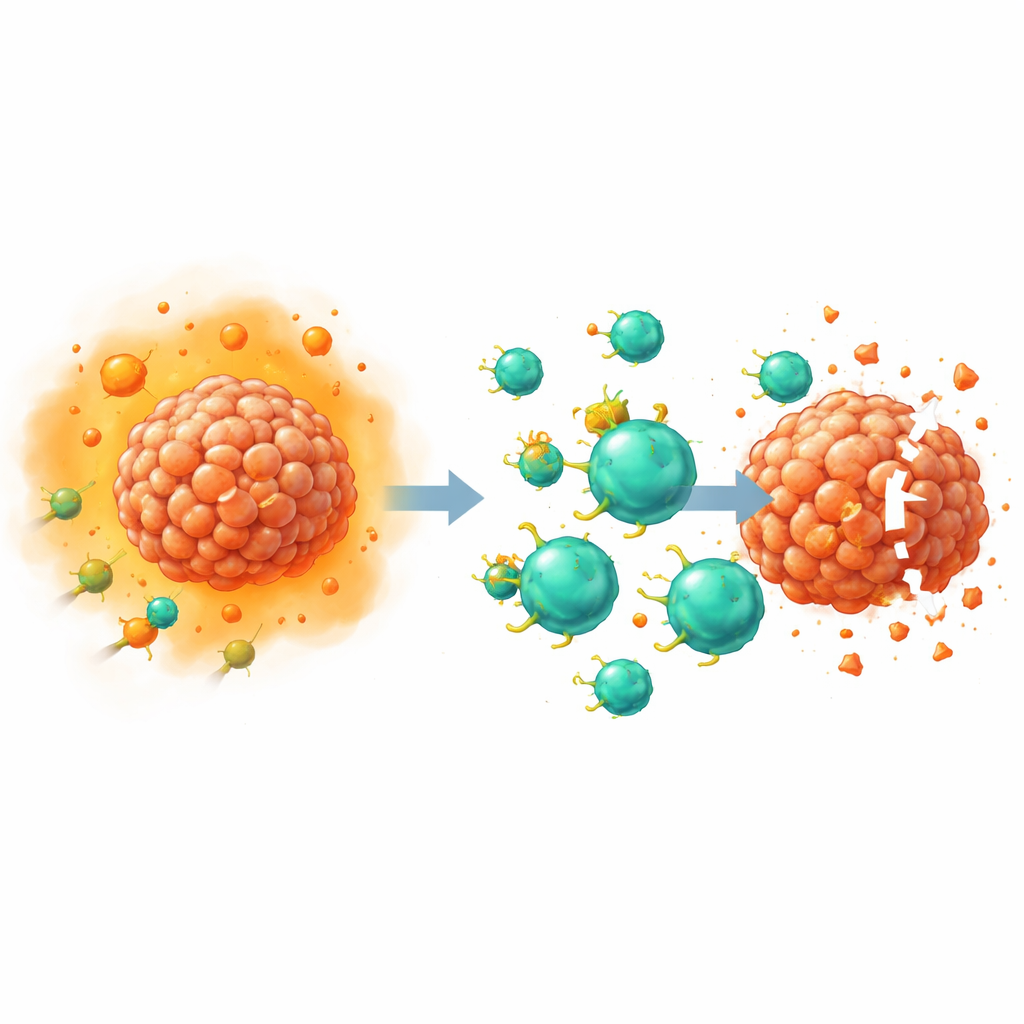
Désarmer un signal suppressif clé
La PGE2 agit en se liant à quatre récepteurs à la surface des cellules, nommés EP1 à EP4. Des travaux antérieurs de ce groupe et d’autres ont montré que les récepteurs EP2 et EP4 sur les cellules T sont particulièrement importants pour affaiblir l’immunité antitumorale, en perturbant notamment la capacité des cellules à répondre au facteur de croissance interleukine-2. Dans cette étude, les chercheurs ont utilisé l’édition génique CRISPR–Cas9 pour supprimer EP2 et EP4 spécifiquement dans des cellules T qui avaient été transformées en cellules CAR T. Parce que ces récepteurs sont difficiles à détecter avec des anticorps de laboratoire standard, l’équipe a validé les modifications de manière indirecte : elle a mesuré des messagers chimiques en aval, tels que la molécule de signalisation cAMP et la forme activée d’une protéine appelée CREB, après l’ajout de fortes doses de PGE2. Les cellules doublement éditées ont montré une perte quasi complète de la signalisation par la PGE2, confirmant que les récepteurs avaient été efficacement neutralisés.
Des boîtes de Pétri aux souris et aux tumeurs humaines
L’équipe a d’abord testé ses cellules CAR T éditées en cultures cellulaires. Lorsque des cellules CAR T ordinaires étaient pré-exposées à la PGE2, leur capacité à se multiplier et à éliminer les cellules cancéreuses diminuait fortement, même si chaque cellule restait capable de tuer une fois activée. En revanche, les cellules CAR T dépourvues à la fois d’EP2 et d’EP4 continuèrent de s’amplifier et éliminèrent complètement les cellules tumorales malgré la présence de PGE2. Ce schéma s’est vérifié tant dans des systèmes murins qu’humains utilisant des cibles pertinentes pour le cancer du pancréas et d’autres tumeurs solides. La différence clé n’était pas que les cellules éditées étaient plus agressives par cellule, mais que davantage d’entre elles survivaient et se divisaient dans des conditions suppressives.
Réponses plus fortes et plus durables dans des modèles vivants
Les chercheurs sont ensuite passés aux modèles animaux. Chez des souris porteuses de tumeurs riches en PGE2, les cellules T ou CAR T sans EP2 et EP4 s’accumulaient en bien plus grand nombre dans les tumeurs que leurs homologues non éditées, tandis que les effectifs dans les ganglions lymphatiques et le sang restaient similaires. La croissance tumorale ralentit, la survie s’améliora, et un sous-ensemble de souris connut une élimination complète de la tumeur — un résultat rarement observé avec des CAR T conventionnels dans les cancers solides. Des études d’imagerie utilisant un rapporteur bioluminescent confirmèrent que les cellules CAR T éditées s’amplifiaient de manière plus robuste à l’intérieur des tumeurs avant de décroître lorsque les tumeurs repoussaient, liant directement le contrôle tumoral à la persistance des cellules T. Enfin, dans des cultures tridimensionnelles issues d’échantillons tumoraux de patients atteints de cancers colorectaux, pancréatiques et neuroendocrines, les cellules CAR T doublement éditées tuèrent systématiquement plus de cellules tumorales que les CAR T standards, soulignant la pertinence clinique de l’approche.
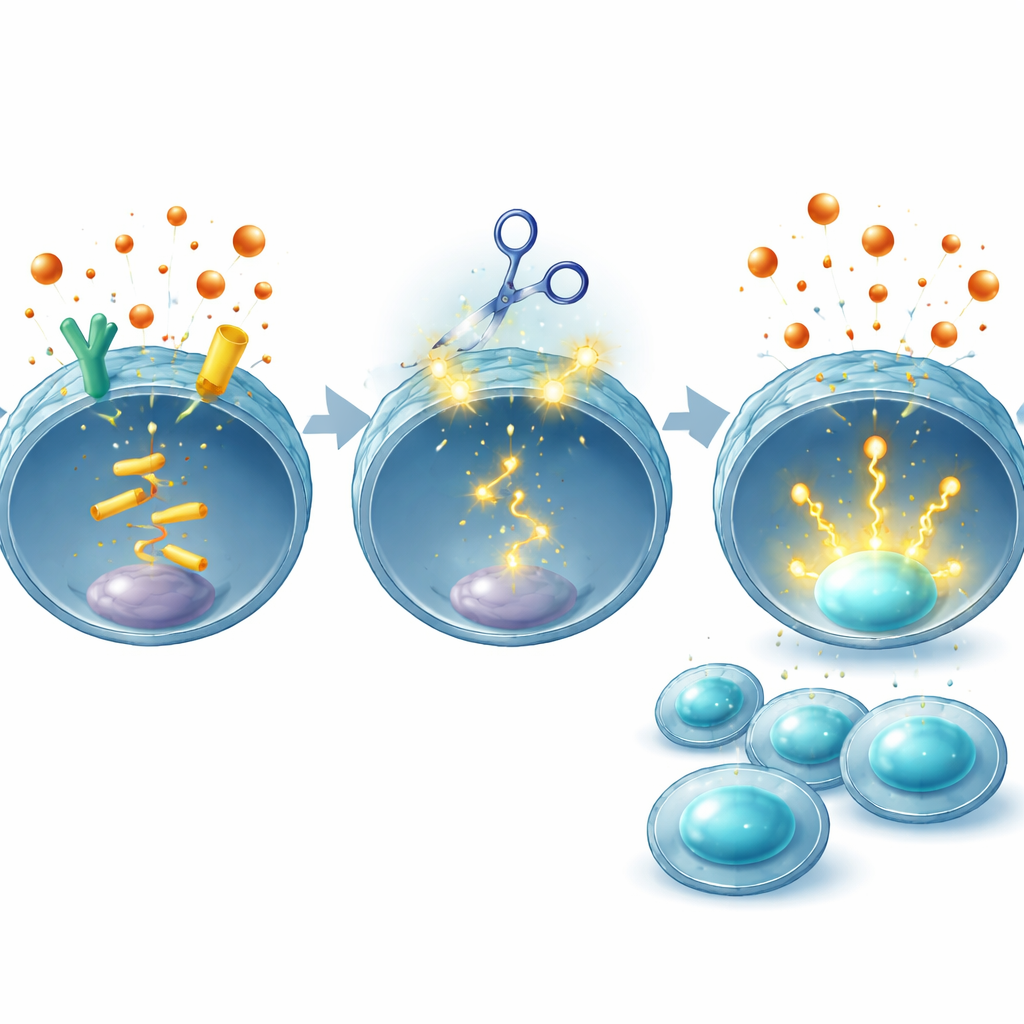
Concilier puissance et sécurité
Comme toute stratégie d’édition génétique suscite des inquiétudes quant à des modifications involontaires de l’ADN, l’équipe a réalisé des contrôles approfondis. À l’aide d’outils informatiques et de séquençage du génome complet, elle a recherché des modifications hors cible dans des cellules CAR T humaines et n’en a trouvé aucune en dehors des gènes EP2 et EP4 prévus chez le donneur examiné. Les auteurs notent également que des CAR T éditées par CRISPR sont déjà testées chez des patients pour d’autres cibles sans toxicité apparente supplémentaire à ce jour. Surtout, en modifiant uniquement les cellules T et en n’inhibant pas la production de PGE2 dans tout l’organisme, cette stratégie vise à préserver les rôles physiologiques de cette hormone dans des tissus comme l’intestin et les reins, évitant les effets secondaires qui ont compliqué les médicaments systémiques.
Ce que cela pourrait signifier pour les patients
En termes simples, ce travail montre que de nombreuses cellules CAR T échouent dans les tumeurs solides non parce qu’elles ne reconnaissent pas leurs cibles, mais parce que la tumeur les baigne d’un voile chimique qui les empêche de se multiplier. En supprimant deux petits sites d’accrochage pour ce voile — EP2 et EP4 — des cellules thérapeutiques, les scientifiques peuvent leur permettre de continuer à se diviser et à agir même dans un environnement hostile. L’étude fournit une feuille de route pour améliorer les cellules CAR T afin qu’elles deviennent sélectivement insensibles à l’un des principaux signaux d’extinction du cancer, ce qui pourrait rendre les thérapies cellulaires plus efficaces contre certains des tumeurs solides les plus meurtrières tout en minimisant les dommages au reste de l’organisme.
Citation: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Mots-clés: Thérapie par cellules CAR T, Tumeurs solides, prostaglandine E2, édition génique CRISPR, microenvironnement tumoral