Clear Sky Science · ar
إلغاء إشارات البروستاجلاندين E2 عبر حذف مستقبلين مزدوجين في خلايا CAR T يعزز الفعالية العلاجية في الأورام الصلبة
لماذا تهم هذه الدراسة لعلاجات السرطان المستقبلية
سمع الكثيرون عن علاج خلايا CAR T، وهو شكل من العلاج المناعي المخصص الذي يستطيع القضاء على بعض سرطانات الدم. ومع ذلك، فشلت الاستراتيجية نفسها في الأورام الصلبة مثل سرطان البنكرياس أو القولون. تستكشف هذه الدراسة كبحًا كيميائيًا مخفيًا داخل الأورام الصلبة — يتوسطه جزيء دهني يُسمى البروستاجلاندين E2 — وتبيّن كيف يمكن لتحرير موقعين لهما على خلايا T العلاجية أن يعزّز قوتها بشكل ملحوظ دون تعطيل وظائف الجسم الأخرى.
ترقية ذكية للأدوية الحية المضادة للسرطان
خلايا CAR T هي خلايا مناعية عادية تؤخذ من المريض وتُعاد برمجتها للتعرف على علامة محددة على خلايا السرطان. في سرطانات الدم، يمكن أن تتكاثر بسرعة وتهاجم وتؤدي أحيانًا إلى الشفاء بعد حقنة واحدة فقط. الأورام الصلبة مختلفة: فهي محاطة بجوار عدائي، يُعرف بالبيئة الدقيقة للورم، المليئة بمواد تُجهد أو تشل خلايا T. ومن أكثر هذه المواد تأثيرًا البروستاجلاندين E2 (PGE2)، إشارة دهنية تنتجها العديد من الأورام بكميات كبيرة وترتبط بنتائج سيئة. بدلاً من محاولة حجب PGE2 في جميع أنحاء الجسم — وهي استراتيجية تسببت في آثار جانبية خطيرة في تجارب سابقة — تساءل الباحثون عما إذا كان بإمكانهم جعل خلايا CAR T تتجاهل هذه الإشارة ببساطة.
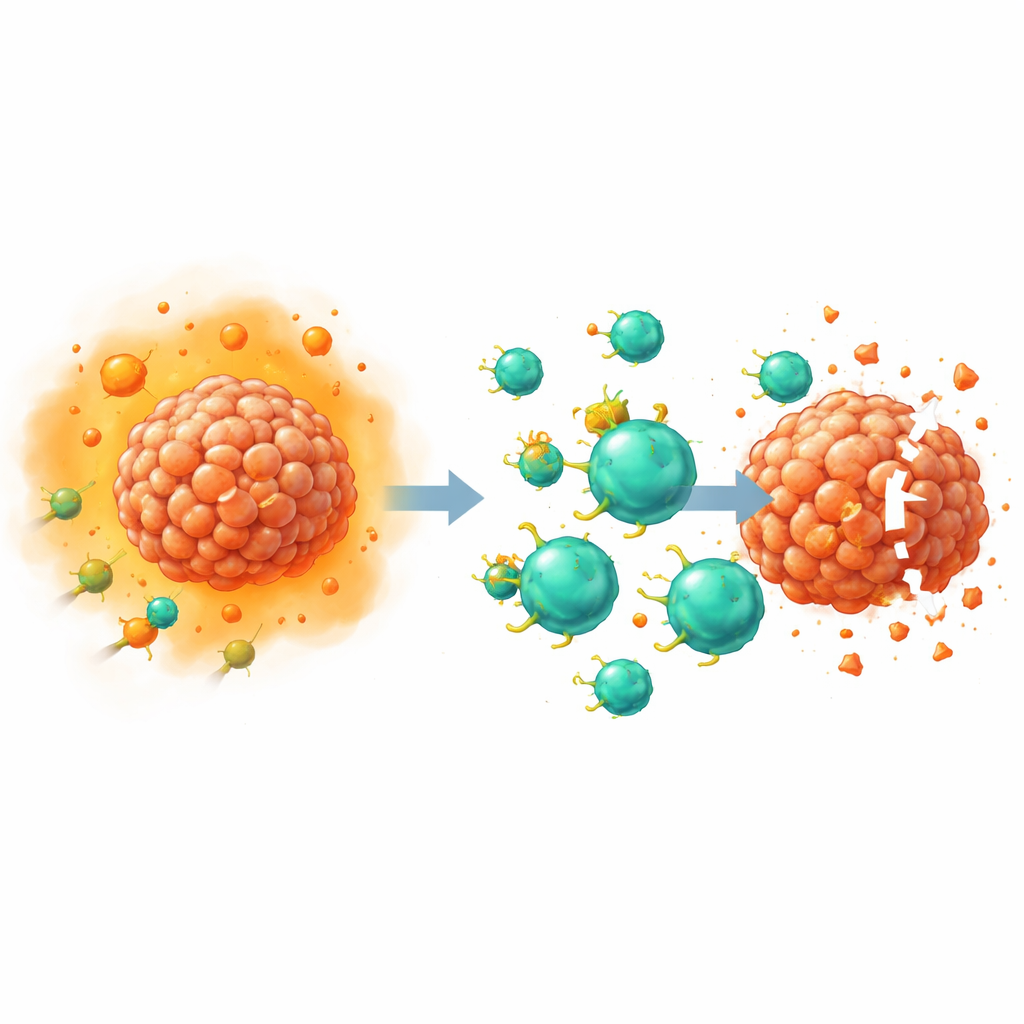
تعطيل إشارة كبح رئيسية
يعمل PGE2 عن طريق الارتباط بأربعة مستقبلات على سطح الخلايا، تسمى EP1 إلى EP4. أظهرت أعمال سابقة من هذه المجموعة ومجموعات أخرى أن مستقبلَي EP2 وEP4 على خلايا T مهمان بشكل خاص في إضعاف المناعة المضادة للورم، إلى حد كبير عن طريق تعطيل قدرة الخلايا على الاستجابة لعامل النمو إنترلوكين-2. في هذه الدراسة، استخدم الباحثون نظام CRISPR–Cas9 لتحرير الجينات وإزالة EP2 وEP4 تحديدًا من خلايا T التي جُهِزت كخلايا CAR T. وبما أن هذه المستقبلات يصعب كشفها باستخدام الأجسام المضادة المخبرية القياسية، فقد حقق الفريق في التعديلات بشكل غير مباشر: قاسوا الرُّسُل الكيميائيين المتبوعين، مثل جزيء الإشارة cAMP والشكل المنشط لبروتين يدعى CREB، بعد إضافة جرعات عالية من PGE2. أظهرت الخلايا المُعدلة مزدوجًا فقدانًا شبه كامل لإشارات PGE2، مما أكد تعطيل المستقبلات بفعالية.
من أطباق المختبر إلى الفئران وأورام المرضى
اختبر الفريق أولًا خلايا CAR T المُحررة في مزروعات خلوية. عندما تعرّضت خلايا CAR T العادية مسبقًا لـPGE2، تراجعت قدرتها على التكاثر وإزالة الخلايا السرطانية بشكل حاد، رغم أن كل خلية ظلت قادرة على القتل عند تنشيطها. بالمقابل، حافظت خلايا CAR T الخالية من EP2 وEP4 على تكاثرها وأزالت الخلايا الورمية بالكامل بالرغم من وجود PGE2. تكرر هذا النمط في أنظمة فأرية وبشرية باستخدام أهداف ذات صلة بسرطان البنكرياس وأورام صلبة أخرى. الاختلاف الرئيسي لم يكن في أن الخلايا المُعدلة كانت أكثر عدوانية لكل خلية، بل أن عددًا أكبر منها نجا وانقسم في ظل ظروف كابحة.
استجابات أقوى وأطول أمداً في النماذج الحية
بعد ذلك، انتقل الباحثون إلى نماذج حيوانية. في الفئران التي تحمل أورامًا غنية بـPGE2، تراكمت خلايا T أو خلايا CAR T الخالية من EP2 وEP4 داخل الأورام بأعداد أكبر بكثير من نظيراتها غير المُعدلة، بينما ظلت الأعداد في العقد الليمفاوية والدم مشابهة. تباطأ نمو الورم، تحسنت البقاء على قيد الحياة، وشهدت مجموعة من الفئران إزاحة كاملة للورم — نتيجة نادرة الحدوث مع خلايا CAR T التقليدية في السرطانات الصلبة. أكدت دراسات التصوير باستخدام مراسل بيلومينيسنت أن خلايا CAR T المُعدلة توسعت بشكل أقوى داخل الأورام قبل أن تتراجع في نهاية المطاف مع نمو الأورام من جديد، رابطين سيطرة الورم بثبات خلايا T. أخيرًا، في مزروعات ثلاثية الأبعاد مأخوذة من عينات مرضى بسرطانات القولون والبنكرياس والأورام العصبية الصماء، قضت خلايا CAR T ذات التعديل المزدوج باستمرار على خلايا ورمية أكثر من خلايا CAR T القياسية، مما يبرز صلة هذا النهج بالسياق السريري.
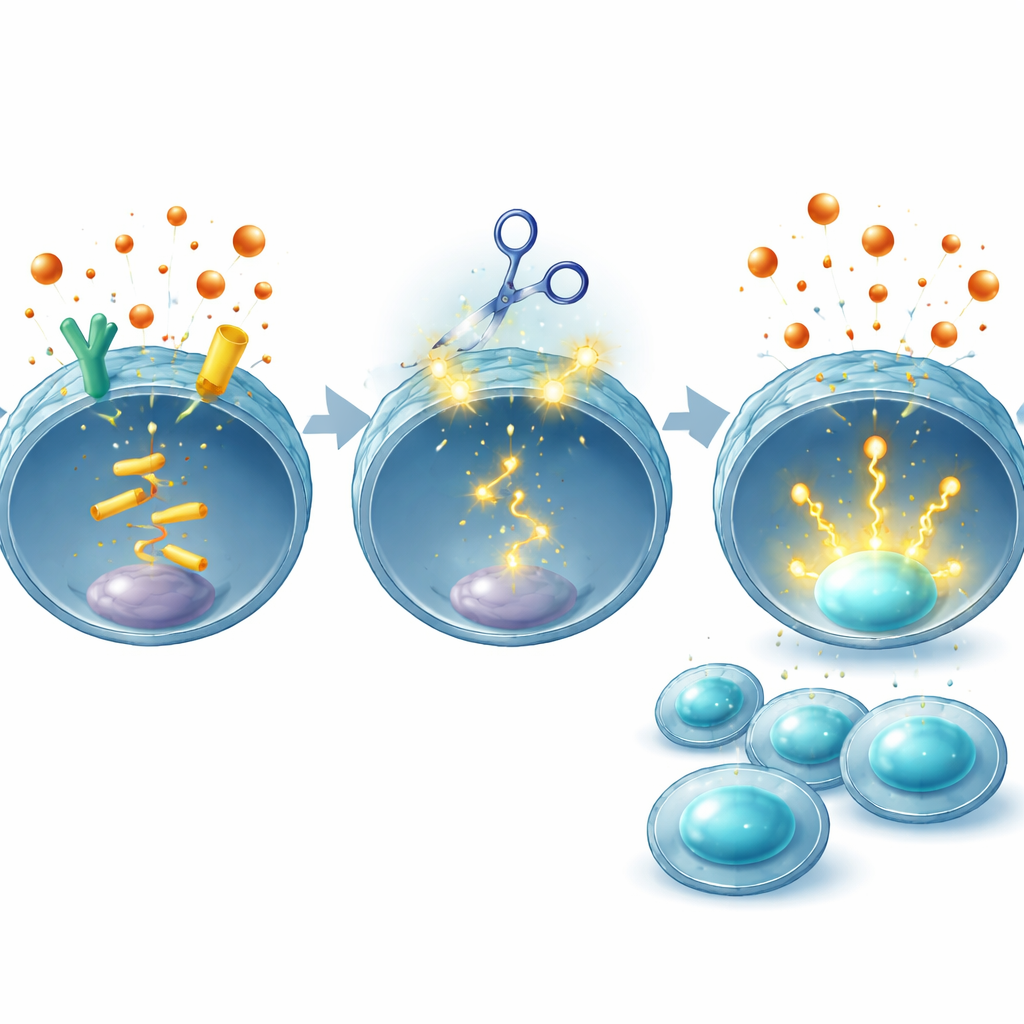
موازنة القوة والسلامة
نظرًا لأن أي استراتيجية لتحرير الجينات تثير مخاوف بشأن تغييرات DNA غير مقصودة، أجرى الفريق فحوصات واسعة. باستخدام أدوات حسابية وتسلسل جينوم كامل، بحثوا عن تعديلات خارجة عن الهدف في خلايا CAR T البشرية ولم يجدوا أيًا بخلاف جينات EP2 وEP4 المقصودة في المتبرع الذي فحصوه. وأشاروا أيضًا إلى أن خلايا CAR T المُعدلة بـCRISPR تُجرَّب بالفعل في مرضى لأهداف أخرى دون سمية مضافة واضحة حتى الآن. والأهم من ذلك، أن تغيير خلايا T فقط بدلاً من حجب إنتاج PGE2 في أنحاء الجسم يهدف إلى الحفاظ على الأدوار الطبيعية لهذا الهرمون في أنسجة مثل الأمعاء والكلى، متجنبًا الآثار الجانبية التي لاحقت الأدوية الجهازية.
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، تُظهر هذه الدراسة أن العديد من خلايا CAR T تفشل في الأورام الصلبة ليس لأنها لا تتعرف على أهدافها، بل لأن الورم يغمرها بضباب كيميائي يمنعها من التكاثر. بإزالة موقعين صغيرين لارتباط ذلك الضباب — EP2 وEP4 — من الخلايا العلاجية، يمكن للعلماء أن يسمحوا لها بالاستمرار في الانقسام والعمل حتى في بيئة عدائية. تقدم الدراسة مخططًا لترقية خلايا CAR T لتصبح صماء انتقائيًا لإحدى إشارات الصمت الرئيسية لدى السرطان، ما قد يجعل العلاجات الخلوية أكثر فعالية ضد بعض أخطر الأورام الصلبة مع تقليل الأذى لبقية الجسم.
الاستشهاد: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
الكلمات المفتاحية: علاج خلايا CAR T, الأورام الصلبة, البروستاجلاندين E2, تحرير جينات CRISPR, البيئة الدقيقة للورم