Clear Sky Science · pt
Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours
Por que esta pesquisa importa para tratamentos futuros do câncer
Muitas pessoas já ouviram falar da terapia com células CAR T, uma forma de imunoterapia personalizada que pode erradicar certos cânceres sanguíneos. Ainda assim, a mesma estratégia tem encontrado dificuldades em tumores sólidos, como os de pâncreas ou colorretal. Este estudo explora um freio químico escondido dentro dos tumores sólidos — mediado por uma molécula lipídica chamada prostaglandina E2 — e mostra como editar com precisão dois de seus locais de acoplamento nas células T terapêuticas pode aumentar significativamente seu poder sem perturbar o resto do organismo.
Uma atualização inteligente para medicamentos vivos contra o câncer
Células CAR T são células imunes comuns retiradas do paciente e reprogramadas para reconhecer um marcador específico nas células cancerígenas. Em cânceres sanguíneos, elas podem expandir vigorosamente, atacar e às vezes curar a doença após uma única infusão. Tumores sólidos são diferentes. Eles estão rodeados por um ambiente hostil, conhecido como microambiente tumoral, repleto de substâncias que exaurem ou paralisam as células T. Uma das mais influentes é a prostaglandina E2, ou PGE2, um sinal lipídico produzido em altas quantidades por muitos tumores e associado a piores desfechos. Em vez de tentar bloquear PGE2 por todo o corpo — estratégia que causou efeitos adversos graves em testes de medicamentos anteriores — os autores perguntaram se poderiam fazer com que as células CAR T simplesmente ignorassem esse sinal.
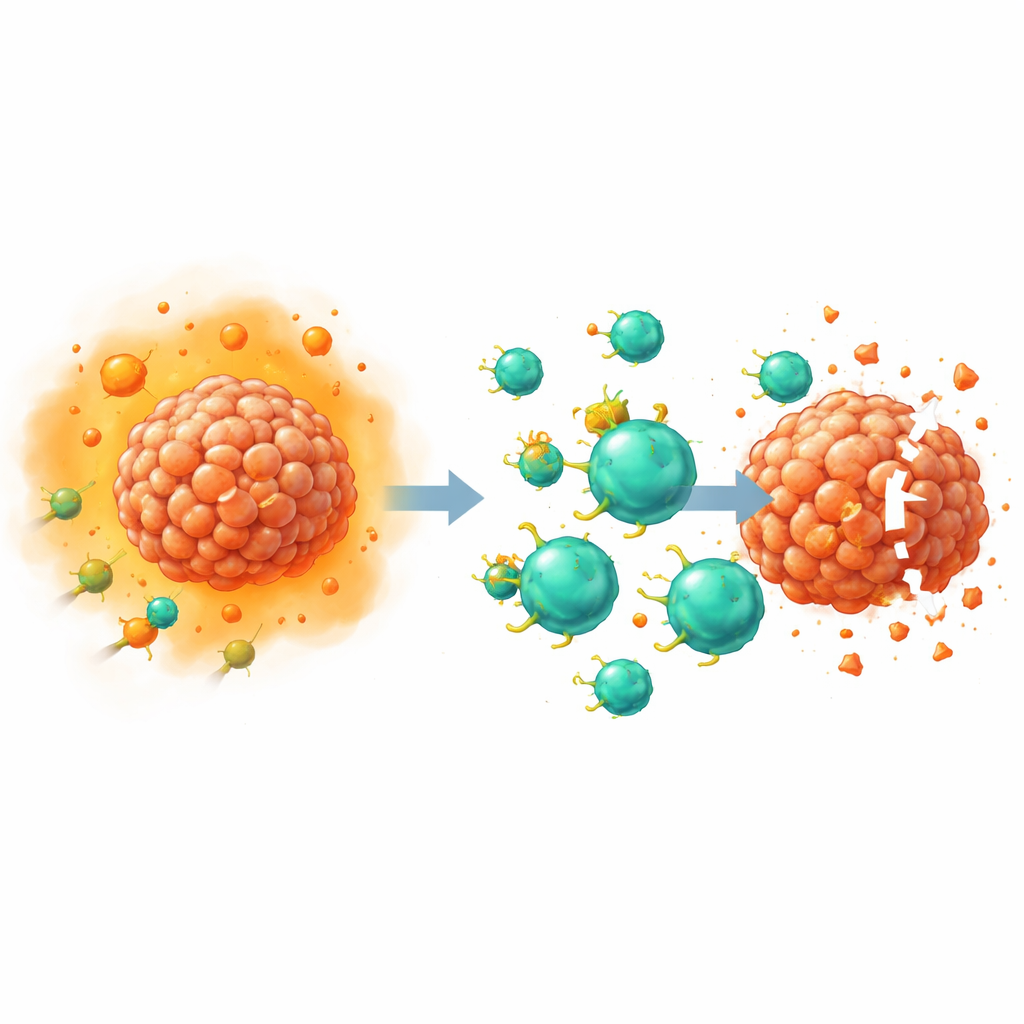
Desarmando um sinal supressor chave
A PGE2 atua ligando-se a quatro receptores na superfície celular, chamados EP1 a EP4. Trabalhos anteriores deste e de outros grupos mostraram que os receptores EP2 e EP4 nas células T são particularmente importantes para enfraquecer a imunidade antitumoral, em grande parte por interromper a capacidade das células de responder ao fator de crescimento interleucina-2. Neste estudo, os pesquisadores usaram edição gênica CRISPR–Cas9 para remover EP2 e EP4 especificamente de células T que haviam sido modificadas como CAR T. Como esses receptores são difíceis de detectar com anticorpos laboratoriais padrão, a equipe validou as edições indiretamente: mediram mensageiros químicos a jusante, como a molécula de sinalização cAMP e a forma ativada de uma proteína chamada CREB, após a adição de altas doses de PGE2. As células duplamente editadas mostraram perda quase completa da sinalização por PGE2, confirmando que os receptores haviam sido efetivamente desativados.
Do cultivo em pratos a camundongos e tumores de pacientes
A equipe testou primeiro suas células CAR T editadas em culturas celulares. Quando células CAR T comuns foram pré-expostas à PGE2, sua capacidade de se multiplicar e eliminar células cancerígenas diminuiu acentuadamente, embora cada célula permanecesse capaz de matar uma vez ativada. Em contraste, células CAR T sem EP2 e EP4 continuaram a se expandir e eliminaram completamente as células tumorais apesar da presença de PGE2. Esse padrão se manteve tanto em modelos de camundongo quanto em sistemas humanos, usando alvos relevantes para câncer de pâncreas e outros tumores sólidos. A diferença chave não foi que as células editadas fossem mais agressivas por célula, mas que um número maior delas sobreviveu e se dividiu em condições supressivas.
Respostas mais fortes e de maior duração em modelos vivos
Em seguida, os pesquisadores avançaram para modelos animais. Em camundongos com tumores ricos em PGE2, células T ou CAR T sem EP2 e EP4 acumularam-se nos tumores em números muito maiores do que suas equivalentes não editadas, enquanto os números em linfonodos e sangue permaneceram semelhantes. O crescimento tumoral desacelerou, a sobrevida melhorou e um subconjunto de camundongos experimentou eliminação completa do tumor — um resultado raramente observado com CAR T convencionais em cânceres sólidos. Estudos de imagem usando um repórter bioluminescente confirmaram que as CAR T editadas expandiram-se mais robustamente dentro dos tumores antes de eventualmente declinar à medida que os tumores recresciam, ligando diretamente o controle tumoral à persistência das células T. Finalmente, em culturas tridimensionais feitas a partir de amostras tumorais de pacientes com câncer colorretal, de pâncreas e neuroendócrino, as CAR T duplamente editadas mataram consistentemente mais células tumorais do que as CAR T padrão, ressaltando a relevância clínica da abordagem.
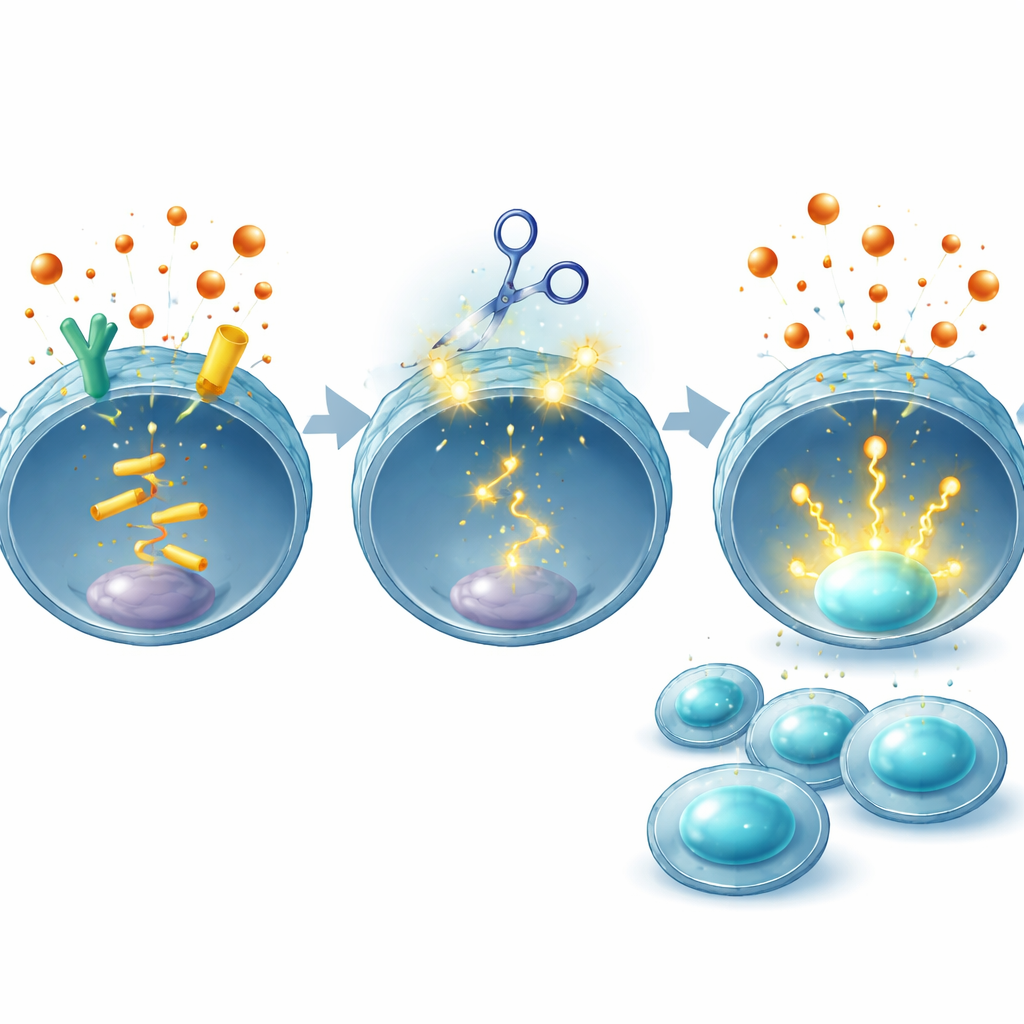
Equilibrando potência e segurança
Como qualquer estratégia de edição gênica levanta preocupações sobre mudanças de DNA não intencionais, a equipe realizou verificações extensas. Usando ferramentas computacionais e sequenciamento do genoma inteiro, procuraram por edições fora do alvo em células CAR T humanas e não encontraram nada além dos genes EP2 e EP4 pretendidos no doador examinado. Eles também observaram que células CAR T editadas com CRISPR já estão sendo testadas em pacientes para outros alvos sem toxicidade adicional clara até agora. Importante, ao alterar apenas as células T e não bloquear a produção de PGE2 em todo o corpo, essa estratégia busca preservar os papéis normais desse hormônio em tecidos como intestino e rins, evitando efeitos colaterais que prejudicaram drogas sistêmicas.
O que isso pode significar para pacientes
Em termos simples, este trabalho mostra que muitas células CAR T falham em tumores sólidos não porque não conseguem reconhecer seus alvos, mas porque o tumor as banha em uma névoa química que as impede de se multiplicar. Ao remover dois pequenos locais de ancoragem para essa névoa — EP2 e EP4 — das células terapêuticas, os cientistas podem permitir que elas continuem a se dividir e a atuar mesmo em um ambiente hostil. O estudo fornece um roteiro para aprimorar células CAR T de modo que fiquem seletivamente surdas a um dos principais sinais de silenciamento do câncer, potencialmente tornando as terapias celulares mais eficazes contra alguns dos tumores sólidos mais letais, minimizando danos ao restante do corpo.
Citação: Dörr, J., Gregor, L., Lacher, S.B. et al. Ablation of prostaglandin E2 signalling through dual receptor knockout in CAR T cells enhances therapeutic efficacy in solid tumours. Nat. Biomed. Eng 10, 697–710 (2026). https://doi.org/10.1038/s41551-025-01610-6
Palavras-chave: CAR T cell therapy, solid tumours, prostaglandin E2, CRISPR gene editing, tumour microenvironment