Clear Sky Science · zh
使用单细胞与空间转录组数据校准组织尺度配体动力学偏微分方程模型
细胞如何在愈合的伤口间交流
当我们的皮肤受伤时,无数细胞必须协调配合以修复损伤,同时尽量减少瘢痕组织的形成。它们通过发送和感知称为配体的化学信号来完成这一过程,这些信号在组织中扩散并在邻近细胞中触发反应。本研究表明,现代的单细胞与空间分辨率的基因测量如何被转化为一种强大的新方法,用于校准这些化学信号的数学模型,帮助研究者更好地理解正常愈合过程以及与瘢痕相关的疾病。
为什么组织中的化学信号重要
组织中的细胞很少独自行事。它们持续交换信号,告诉彼此何时分裂、移动或恢复静止。其中许多信号是由一类细胞释放、被另一类细胞表面受体捕获的短程化学物质。这类信号对伤口愈合、炎症以及纤维化和癌症等疾病至关重要。研究者长期以来使用称为反应—扩散模型的数学方程来描述这些化学物质如何被产生、扩散和降解。然而,一个长期存在的问题是如何选择现实的参数值(例如产生速率和结合强度),以便模型真实反映活组织内的情况,而非理想化的实验室条件。
以崭新的视角观察活组织
近来,两种实验技术改变了科学家观察组织的方式。单细胞RNA测序可以测量成千上万单个细胞中哪些基因处于活跃状态,揭示它们的身份和信号能力。相比之下,空间转录组学在组织切片上像网格一样测量许多微小点的基因活动,从而保留了不同细胞的空间位置信息。在这项工作中,作者将来自受伤后30天的人皮肤样本的两类数据结合起来,此时组织处于愈合的“重塑”阶段。他们关注三种关键信号分子——转化生长因子β(TGFβ)的不同形式,已知这些分子影响瘢痕形成与组织修复。
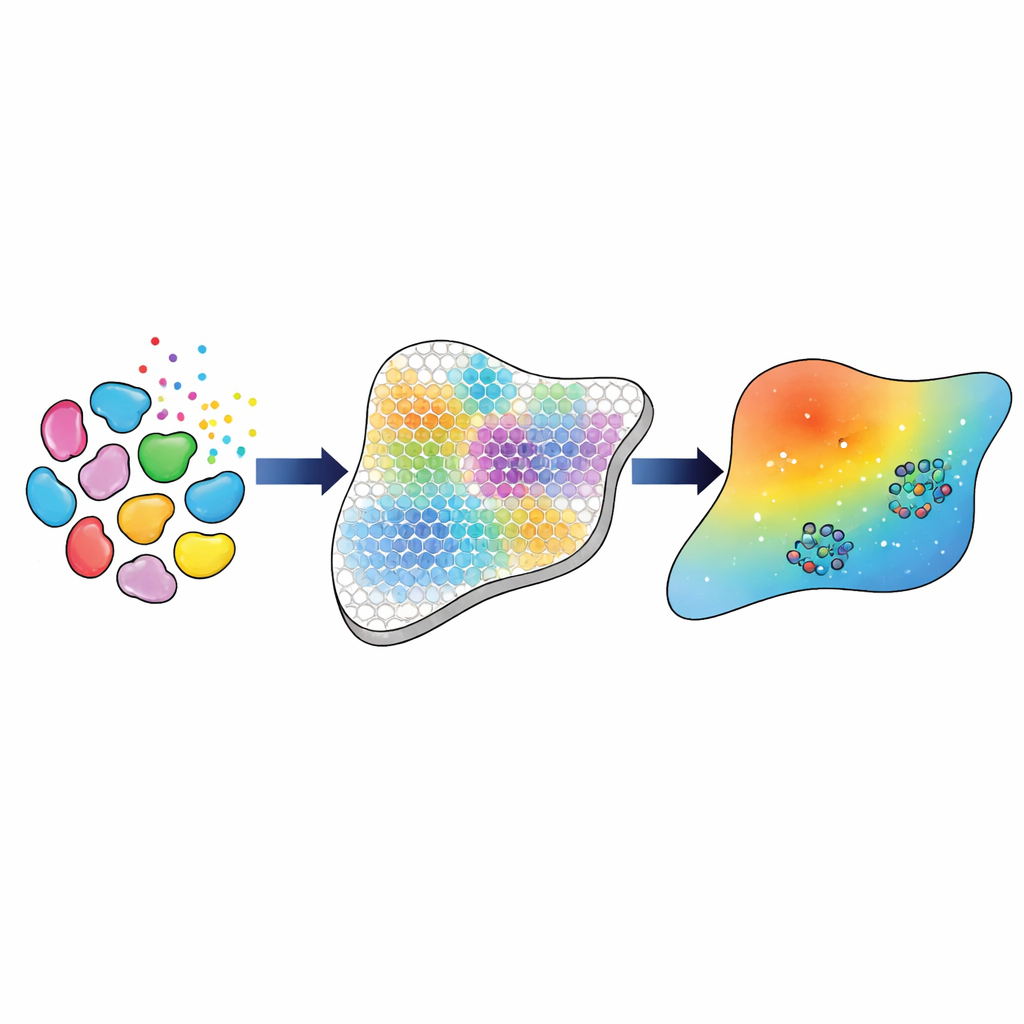
从基因到模型参数的分步流程
研究者构建了一个计算流程,将这些丰富的基因测量结果连接到一个组织尺度的TGFβ运动与作用模型。首先,他们使用成熟的生物信息学工具识别主要细胞类型与亚型——例如三类不同的成纤维细胞、巨噬细胞和内皮细胞——并估算每个网格点上各类细胞的数量。随后,他们基于发送细胞的配体基因活性与接收细胞的受体基因活性,推断每类细胞通过TGFβ相互交流的强度。这些推断出的“相互作用强度”成为数学模型必须再现的实验目标。
让模型学会匹配组织
接下来,研究团队用一组偏微分方程在与空间转录组布局相对应的网格上表示TGFβ在组织中的扩散。对于任意一组参数值——例如TGFβ的扩散速度、降解速率以及各细胞类型的产生或吸收量——模型会预测三种TGFβ形式的浓度场以及细胞类型之间由此产生的相互作用强度。为调优这些参数,作者采用了三阶段的校准策略。首先,他们应用近似贝叶斯方法在由先前实验信息限制的合理参数空间内进行广泛扫描,逐步缩小与基因数据推断的相互作用强度高度相关的参数组合。然后,他们将这些有前景的候选参数输入基于梯度的优化方法,精细调整参数以最大化一致性。该混合方法实现了模型预测与数据推断的相互作用强度之间几乎完美的线性拟合(相关系数为0.99)。
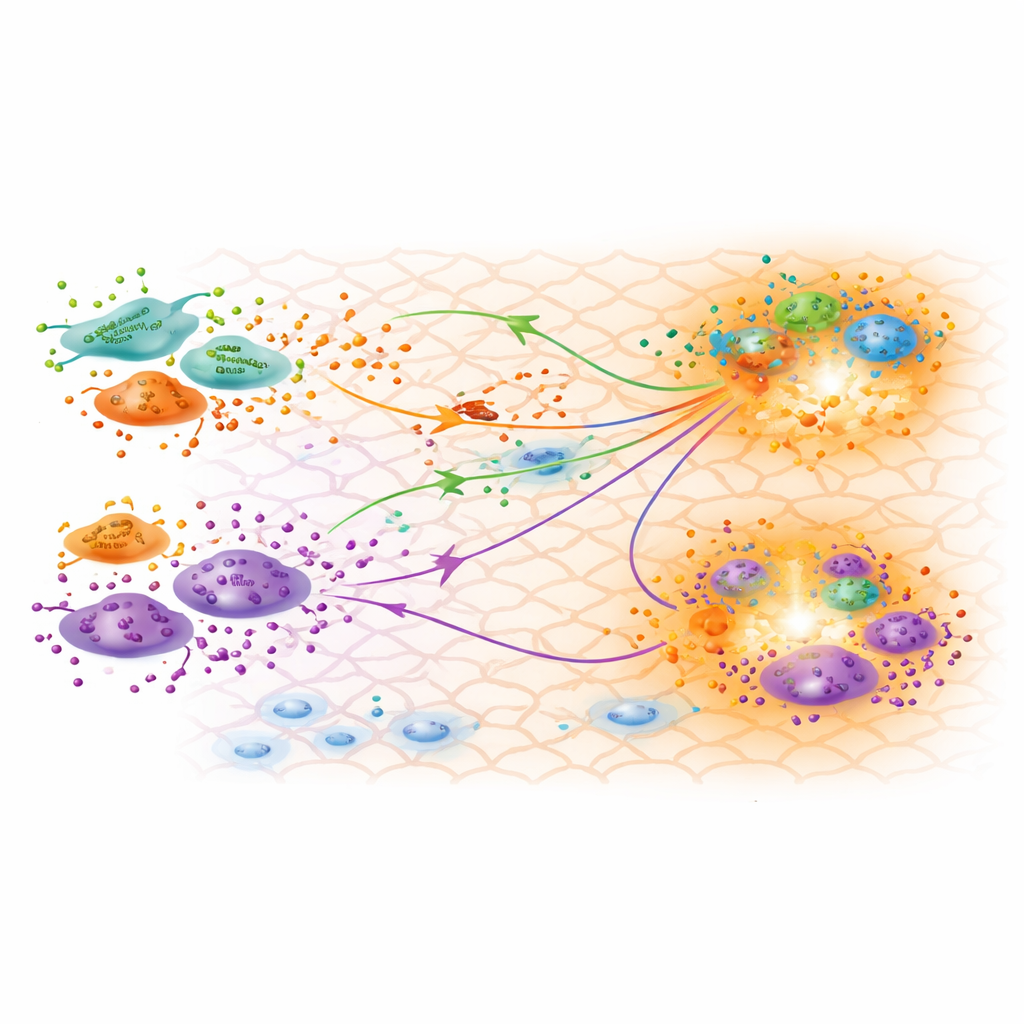
校准模型对愈合过程的启示
在得到一个高度匹配的模型后,研究者进一步探讨这些推断参数对生物学的指示。他们证实了基于基因表达数据识别出的三种成纤维细胞亚型在功能上是不同的,一种表现出强烈的炎症特征,另一种则显示出有助于伤口收缩的肌纤维母细胞特征。校准得到的产生速率表明,在重塑阶段促炎成纤维细胞产生的TGFβ最少,这与炎症在第30天消退是一致的。令人意外的是,一种被称为乳头层成纤维细胞的亚型似乎产生相对较高量的TGFβ3,这种形式常与较少瘢痕和更再生性的结果相关。模型预测的TGFβ浓度图与成纤维细胞和巨噬细胞聚集的区域相吻合,提示这些部位可能是主动交流的热点,进而影响瘢痕形成的方式。
可扩展到其他组织与疾病的灵活框架
除了这个特定的伤口愈合案例外,研究的主要贡献是提出了一个通用流程,可将现代基因数据转化为良好校准的组织尺度模型。通过将单细胞与空间转录组学数据与先进的统计与优化工具相结合,研究者可以更严格地估计配体的传播速度、结合强度以及哪些细胞在信号传递中贡献最大。该框架可适应于其他组织、其他信号分子及纤维化瘢痕或癌症等疾病状态,最终有助于将复杂的分子快照转化为对整体组织行为的可预测模型。
引用: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
关键词: 伤口愈合, 细胞信号传导, 空间转录组学, TGF β, 数学建模