Clear Sky Science · he
כיול מודלים ברמת רקמה עבור דינמיקת ליגנדים באמצעות נתוני ריצוף חד-תאי וטרנסקריפטומיקה מרחבית
כיצד תאים מתקשרים מעבר לפצע שמחלִים
כשעורנו נפגע, מיליוני תאים חייבים לתאם פעולות כדי לתקן את הנזק מבלי להשאיר אחריהם צלקת מוגזמת. הם עושים זאת על ידי שליחת וקבלה של מסרים כימיים הנקראים ליגנדים, אשר מתפשטים ברקמה ומעוררים תגובות בתאים שכנים. המחקר הזה מציג כיצד מדידות גנטיות מודרניות ברזולוציה חד-תאית ומרחבית ניתנות להמרה לשיטת כיול חזקה של מודלים מתמטים של אותות כימיים אלה, ובכך מסייע לחוקרים להבין טוב יותר ריפוי נורמלי ומחלות הקשורות לצלקת.
מדוע המסרים הכימיים חשובים ברקמות
תאים ברקמות שלנו בקושי פועלים לבד. הם מחליפים באופן קבוע אותות שמורים להם מתי להתחלק, לזוז או להירגע. רבים מהאותות האלה הם חומרים בטווח קצר שמשתחררים מתא אחד ונקלטים על ידי קולטנים בתא אחר. מסרים כאלה נמצאים במרכז תהליכי ריפוי פצעים, דלקת ומחלות כמו פיברוזיס וסרטן. חוקרים השתמשו מזה זמן רב במשוואות מתמטיות, הנקראות מודלי תגובה–דיפוזיה, כדי לתאר כיצד חומרים אלה מיוצרים, מתפשטים ומתפרקים. עם זאת, בעיה ממושכת הייתה כיצד לבחור ערכי פרמטר ריאליסטיים — כגון שיעורי ייצור ועוצמות קשירה — כך שהמודלים ייצגו באמת מה שקורה בתוך רקמה חיה ולא רק בתנאי מעבדה אידיאליים.
עיניים חדשות על רקמה חיה
לאחרונה שתי טכנולוגיות ניסיוניות שינו את דרך הצפייה של מדענים ברקמות. ריצוף RNA חד-תאי מודד אילו גנים פעילים באלפי תאים בודדים, וחושף את זהותם ויכולות האיתות שלהם. לעומת זאת, טרנסקריפטומיקה מרחבית מודדת פעילות גנים במאות או אלפי נקודות קטנות הפרושות כמו רשת על חתך הרקמה, ושומרת על המיקום של תאים שונים. בעבודה זו, המחברים משלבים שני סוגי נתונים מנתחי עור אנושיים שנלקחו 30 יום לאחר פגיעה, כאשר הרקמה נמצאת בשלב ה"שיקום" של הריפוי. הם מתמקדים בשלוש צורות של מולקולת איתות מרכזית, גורם הגדילה הממגר (TGFβ), הידוע בהשפעתו על היווצרות צלקת ותיקון רקמה.
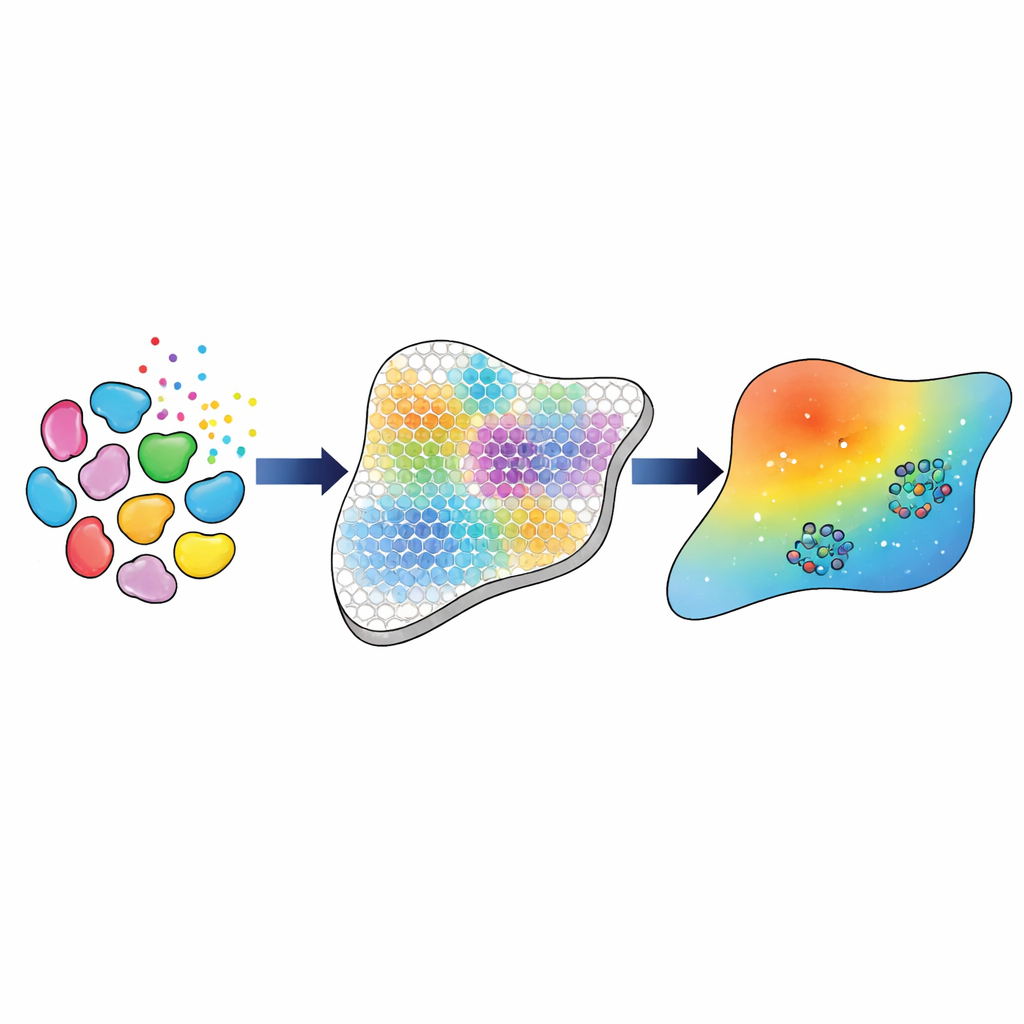
צנרת שלב אחר שלב מהגנים לפרמטרי המודל
החוקרים בונים צנרת חישובית שמחברת את המדידות הגנטיות העשירות האלה למודל ברמת רקמה של תנועת ופעולת ה-TGFβ. ראשית, הם משתמשים בכלי ביו-אינפורמטיקה מבוססים כדי לזהות את סוגי ותתי-הסוגים העיקריים של תאים — כגון שלוש כיתות מובחנות של פיברובלסטים, מאקרופאגים ותאי אנדותל — ולהעריך כמה מכל סוג יש בכל נקודה ברשת הטרנסקריפטומיקה. לאחר מכן הם מסיקים עד כמה כל סוג תא צפוי "לדבר" עם סוגים אחרים באמצעות TGFβ, על סמך פעילות הגנים של הליגנדים בתאים משדרים והקולטנים בתאים מקבלים. אותן "עוצמות אינטראקציה" שנגזרות משמשות כמטרת הניסוי שעל המודל המתמטי לשחזר.
להכשיר את המודל כדי להתאים לרקמה
בהמשך, הצוות מייצג את התפשטות ה-TGFβ ברקמה באמצעות מערכת משוואות דפרנציאליות חלקיות הנפתרות על גבי רשת המשקפת את פריסת הטרנסקריפטומיקה המרחבית. לכל סט פרמטרים נבחר — למשל מהירות דיפוזיה של ה-TGFβ, קצב פירוק ומה כל סוג תא מייצר או סופג — המודל מנבא שדות ריכוז עבור שלוש צורות ה-TGFβ ואת עוצמות האינטראקציה הנובעות בין סוגי התאים. כדי לכוונן את הפרמטרים, המחברים משתמשים באסטרטגיית כיול בשלושה שלבים. ראשית הם מיישמים שיטות בייסיאניות מקורבות כדי לסרוק באופן רחב פרמטרים סבירים בהשראת ניסויים קודמים, ומצמצמים בהדרגה לשילובים שמתאימים היטב לעוצמות האינטראקציה שנגזרו מנתוני הגנים. לאחר מכן הם מזינים מועמדים מבטיחים אלה לשיטת אופטימיזציה מבוססת שיפוע שמדוייקת את הפרמטרים כדי למקסם את ההסכמה. גישה היברידית זו משיגה התאמה כמעט מושלמת בקורלציה ליניארית (0.99) בין עוצמות האינטראקציה שחזה המודל לאלה שנגזרו מהנתונים.
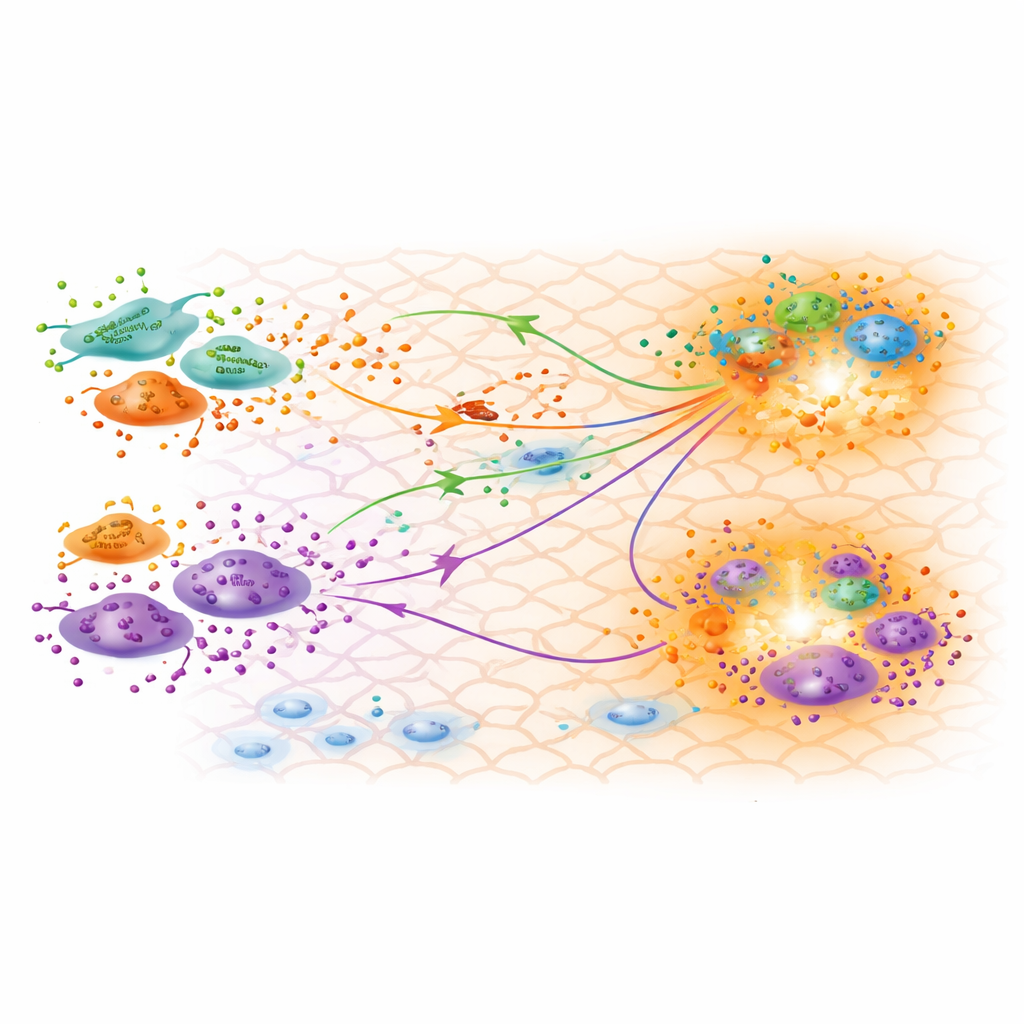
מה המודל המכויל חושף על הריפוי
עם מודל שמתאים היטב, החוקרים חקרו מה הפרמטרים שנגזרו מעידים על הביולוגיה. הם מאשרים שתתי-הסוגים השלושה של פיברובלסטים שזוהו מנתוני הביטוי הגני הם פונקציונלית מובחנים, כאשר אחד מראה פרופיל דלקתי חזק ואחר מציג מאפיינים של מיו-פיברובלסטים המסייעים לכווץ את הפצע. שיעורי הייצור המכוילים מצביעים שפיברובלסטים פרו-דלקתיים מייצרים את כמות ה-TGFβ הנמוכה ביותר בשלב השיקום, בהתאמה להחלשות הדלקת ביום ה-30. באופן מפתיע, תת-סוג הידוע כפיברובלסטים פפילריים נראה מייצר כמויות יחסית גבוהות של TGFβ3, צורה שמקושרת לעתים להפחתת צלקת ותוצאות רגנרטיביות יותר. מפות הריכוז של ה-TGFβ שחזה המודל תואמות לאזורים שבהם פיברובלסטים ומאקרופאגים מצטברים, ומרמזות על מוקדי תקשורת פעילים שעשויים לכוון כיצד הצלקת תיווצר.
מסגרת גמישה לרקמות ומחלות עתידיות
מעבר למקרה הספציפי של ריפוי פצעים זה, התרומה העיקרית של המחקר היא צנרת כללית להמרת נתוני גנום מודרניים למודלים ברמת רקמה עם כיול טוב. על ידי שילוב ריצוף חד-תאי וטרנסקריפטומיקה מרחבית עם כלים סטטיסטיים ואופטימיזציה מתקדמים, חוקרים יכולים להעריך באופן מחושב עד כמה מהר ליגנדים נעים, כמה חזק הם נקשרים ואילו תאים תורמים הכי הרבה לאיתות. מסגרת זו ניתנת להתאמה לרקמות אחרות, למולקולות איתות אחרות ולמצבי מחלה כמו צלקת פיברוטית או סרטן, ובסופו של דבר מסייעת להפוך תמונות מולקולריות מורכבות למודלים חזויים של התנהגות רקמות שלמות.
ציטוט: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
מילות מפתח: החלמת פצעים, אותות בין תאים, טרנסקריפטומיקה מרחבית, TGF בטא, מודלינג מתמטי