Clear Sky Science · pl
Kalibracja modeli PDE na poziomie tkanki opisujących dynamikę ligandów przy użyciu danych z sekwencjonowania pojedynczych komórek i transkryptomiki przestrzennej
Jak komórki komunikują się przez gojącą się ranę
Gdy nasza skóra zostaje uszkodzona, niezliczone komórki muszą się skoordynować, aby naprawić uszkodzenie, nie pozostawiając przy tym nadmiernej blizny. Robią to, wysyłając i odbierając chemiczne komunikaty zwane ligandami, które rozprzestrzeniają się w tkance i wywołują reakcje w sąsiednich komórkach. W tym badaniu pokazano, jak nowoczesne pomiary genetyczne o rozdzielczości pojedynczej komórki i przestrzennej można wykorzystać do potężnej, nowej metody kalibracji matematycznych modeli tych chemicznych sygnałów, pomagając naukowcom lepiej zrozumieć zarówno normalne gojenie, jak i choroby związane z bliznowaceniem.
Dlaczego chemiczne komunikaty mają znaczenie w tkankach
Komórki w naszych tkankach rzadko działają samodzielnie. Stale wymieniają sygnały, które mówią im, kiedy się dzielić, przemieszczać lub uspokoić. Wiele z tych sygnałów to związki krótkiego zasięgu uwalniane przez jedną komórkę i wychwytywane przez receptory innej. Takie komunikaty są kluczowe przy gojeniu ran, stanie zapalnym oraz w chorobach takich jak włóknienie i rak. Badacze od dawna używają równań reakcji i dyfuzji, aby opisać, jak te chemikalia są produkowane, rozprzestrzeniają się i są rozkładane. Jednak od dawna istnieje problem, jak dobrać realistyczne wartości parametrów — takie jak tempo produkcji czy siła wiązania — aby modele rzeczywiście odzwierciedlały procesy zachodzące w żywej tkance, a nie tylko w idealnych warunkach laboratoryjnych.
Nowe spojrzenie na żywą tkankę
Ostatnio dwie technologie eksperymentalne zmieniły sposób, w jaki naukowcy obserwują tkanki. Sekwencjonowanie RNA pojedynczych komórek mierzy, które geny są aktywne w tysiącach pojedynczych komórek, ujawniając ich tożsamość i zdolności sygnalizacyjne. Transkryptomika przestrzenna natomiast mierzy aktywność genów w wielu małych punktach ułożonych jak siatka na przekroju tkanki, zachowując informację o położeniu różnych komórek. W tej pracy autorzy łączą oba typy danych z próbek ludzkiej skóry pobranych 30 dni po zranieniu, gdy tkanka znajduje się w fazie „remodelingu” gojenia. Skupiają się na trzech wersjach kluczowej cząsteczki sygnalizacyjnej, transformującego czynnika wzrostu beta (TGFβ), znanej z wpływu na tworzenie blizn i naprawę tkanek.
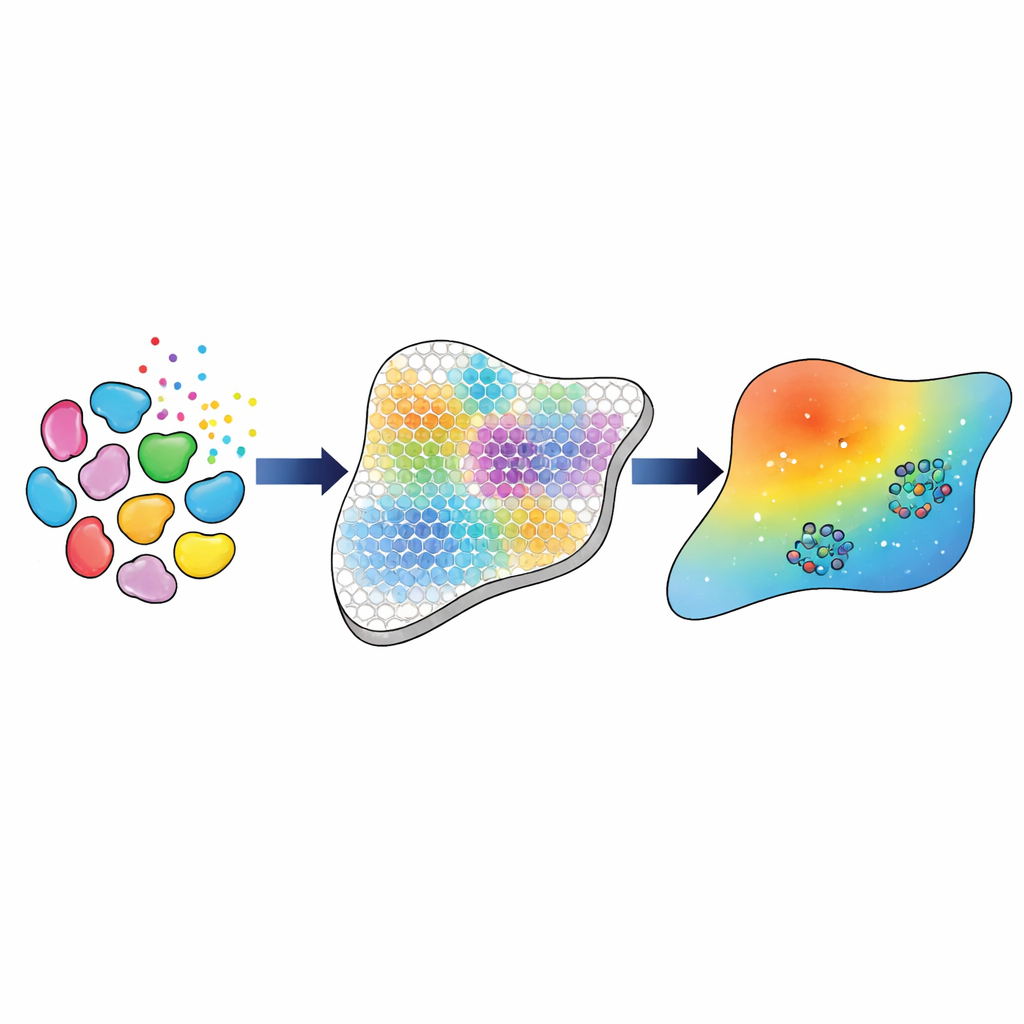
Krokowy proces od genów do parametrów modelu
Naukowcy zbudowali pipeline obliczeniowy, który łączy te bogate pomiary genetyczne z modelem tkankowym opisującym ruch i działanie TGFβ. Najpierw używają sprawdzonych narzędzi bioinformatycznych, aby zidentyfikować główne typy i podtypy komórek — takie jak trzy odrębne klasy fibroblastów, makrofagi i komórki śródbłonka — oraz oszacować, ile każdej z nich występuje w każdym punkcie siatki przestrzennej. Następnie wnioskowali, jak silnie każdy typ komórki prawdopodobnie komunikuje się z innymi za pośrednictwem TGFβ, na podstawie skumulowanej aktywności genów ligandów w komórkach nadawczych i receptorów w komórkach odbiorczych. Te wywnioskowane „siły interakcji” służą jako eksperymentalny cel, który model matematyczny musi odtworzyć.
Uczenie modelu dopasowania do tkanki
Następnie zespół opisuje rozprzestrzenianie się TGFβ w tkance zestawem równań różniczkowych cząstkowych rozwiązywanych na siatce odzwierciedlającej układ transkryptomiki przestrzennej. Dla dowolnego wybranego zestawu wartości parametrów — na przykład jak szybko TGFβ dyfunduje, jak szybko ulega degradacji oraz ile każdy typ komórki produkuje lub absorbuje — model przewiduje pola stężeń trzech form TGFβ i wynikające z nich siły interakcji między typami komórek. Aby dostroić te parametry, autorzy stosują trzystopniową strategię kalibracji. Najpierw używają przybliżonych metod bayesowskich, aby szeroko przeskanować dopuszczalne parametry inspirowane wcześniejszymi eksperymentami, stopniowo zawężając się do kombinacji dobrze skorelowanych z siłami interakcji wyprowadzonymi z danych genetycznych. Następnie obiecujące kandydatury trafiają do metody optymalizacji opartej na gradientach, która precyzyjnie dopracowuje parametry, maksymalizując zgodność. To hybrydowe podejście osiąga niemal doskonałe liniowe dopasowanie (korelacja 0,99) między siłami interakcji przewidywanymi przez model a tymi wyprowadzonymi z danych.
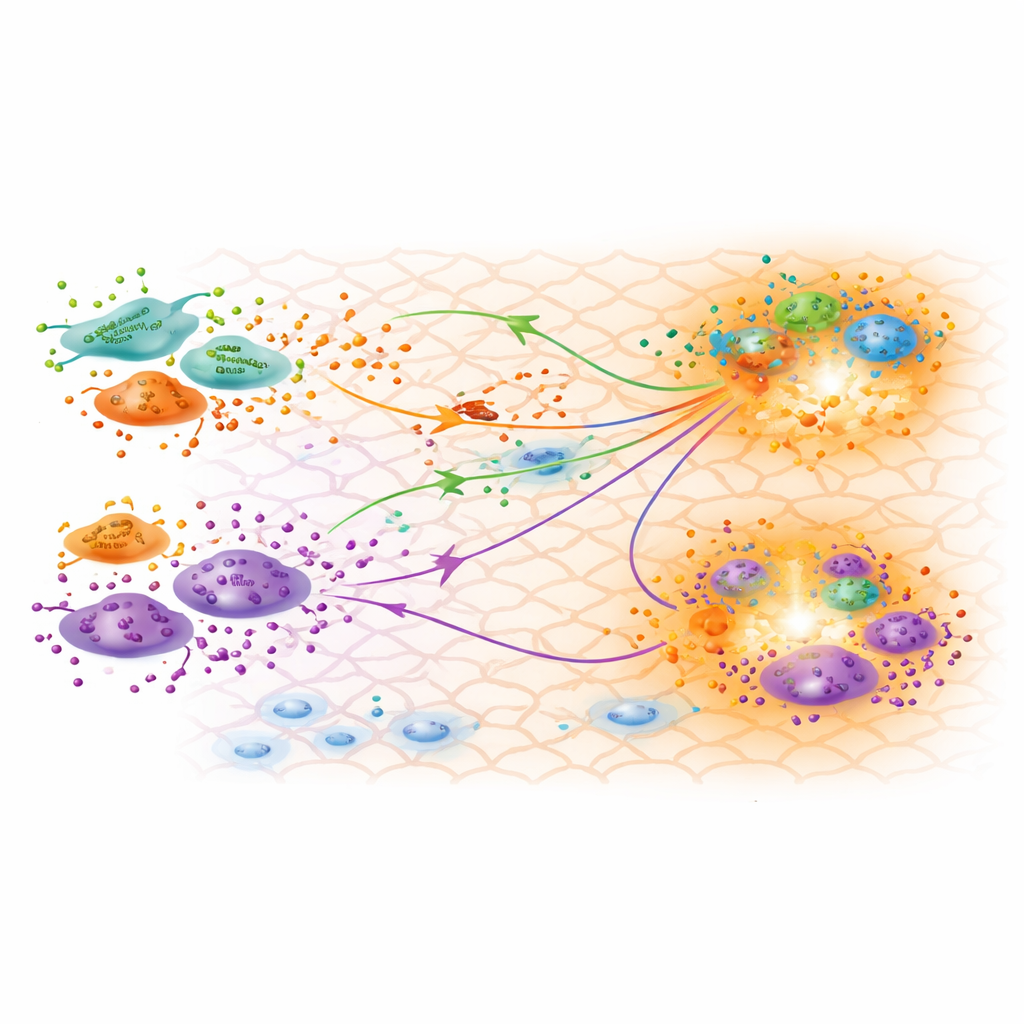
Co skalibrowany model mówi o gojeniu
Majac dobrze dopasowany model, badacze analizują, co wywnioskowane parametry mówią o biologii. Potwierdzają, że trzy podtypy fibroblastów zidentyfikowane na podstawie ekspresji genów są funkcjonalnie odmienne: jeden wykazuje silny profil zapalny, a inny cechy miofibroblastów pomagających w obkurczaniu rany. Skalibrowane tempo produkcji sugeruje, że fibroblasty prozapalne produkują najmniej TGFβ w stadium remodelingu, co jest zgodne z ustępowaniem zapalenia po 30 dniach. Zaskakująco, podtyp znany jako fibroblasty brodawkowate (papillary) wydaje się produkować stosunkowo dużo TGFβ3, formy często kojarzonej z mniejszym bliznowaceniem i bardziej regeneracyjnymi wynikami. Przewidywane przez model mapy stężeń TGFβ pokrywają się z obszarami, gdzie gromadzą się fibroblasty i makrofagi, sugerując istnienie punktów o intensywnej komunikacji, które mogą kierować procesem formowania blizny.
Elastyczne ramy dla przyszłych badań nad tkankami i chorobami
Ponad to konkretne studium przypadku gojenia ran, głównym wkładem pracy jest ogólny pipeline do przekształcania nowoczesnych danych genetycznych w dobrze skalibrowane modele na poziomie tkanki. Łącząc sekwencjonowanie pojedynczych komórek i transkryptomikę przestrzenną z zaawansowanymi narzędziami statystycznymi i optymalizacyjnymi, badacze mogą bardziej rygorystycznie oszacować, jak szybko ligandy się poruszają, jak silnie wiążą oraz które komórki najbardziej przyczyniają się do sygnalizacji. Ramy te można zaadaptować do innych tkanek, innych cząsteczek sygnalizacyjnych i stanów chorobowych, takich jak włóknienie czy rak, co ostatecznie pomaga przekształcić złożone molekularne „migawki” w predykcyjne modele zachowania całych tkanek.
Cytowanie: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Słowa kluczowe: gojenie ran, sygnalizacja komórkowa, transkryptomika przestrzenna, TGF beta, modelowanie matematyczne