Clear Sky Science · es
Calibración de modelos PDE a nivel tisular de la dinámica de ligandos usando datos de transcriptómica espacial y de célula única
Cómo se comunican las células a través de una herida en curación
Cuando nuestra piel resulta lesionada, un sinnúmero de células debe coordinarse para reparar el daño sin dejar demasiado tejido cicatricial. Lo hacen enviando y percibiendo mensajes químicos llamados ligandos, que se propagan por el tejido y desencadenan respuestas en las células vecinas. Este estudio muestra cómo las mediciones genéticas modernas a resolución de célula única y espacial pueden transformarse en una nueva y potente manera de calibrar modelos matemáticos de esos mensajes químicos, ayudando a los investigadores a comprender mejor la curación normal y las enfermedades relacionadas con la cicatrización.
Por qué importan los mensajes químicos en los tejidos
Las células en nuestros tejidos rara vez actúan de forma aislada. Intercambian constantemente señales que les indican cuándo dividirse, moverse o reducir su actividad. Muchas de estas señales son químicos de corto alcance liberados por una célula y captados por receptores en otra. Estos mensajes son centrales en la cicatrización, la inflamación y enfermedades como la fibrosis y el cáncer. Durante mucho tiempo, los investigadores han utilizado ecuaciones matemáticas, conocidas como modelos de reacción–difusión, para describir cómo se producen, se difunden y se degradan estos químicos. Sin embargo, un problema persistente ha sido cómo escoger valores de parámetros realistas —como las tasas de producción y las afinidades de unión— para que los modelos reflejen verdaderamente lo que ocurre en tejido vivo y no solo condiciones idealizadas de laboratorio.
Nuevas miradas al tejido vivo
Recientemente, dos tecnologías experimentales han transformado la forma en que los científicos pueden observar los tejidos. La secuenciación de ARN unicelular mide qué genes están activos en miles de células individuales, revelando sus identidades y capacidades de señalización. La transcriptómica espacial, en contraste, mide la actividad génica en muchos pequeños puntos dispuestos como una cuadrícula sobre una rebanada de tejido, preservando la localización de las distintas células. En este trabajo, los autores combinan ambos tipos de datos procedentes de muestras de piel humana tomadas 30 días después de una herida, cuando el tejido se encuentra en la fase de “remodelado” de la curación. Se centran en tres variantes de una molécula de señalización clave, el factor de crecimiento transformante beta (TGFβ), conocida por influir en la formación de cicatrices y la reparación tisular.
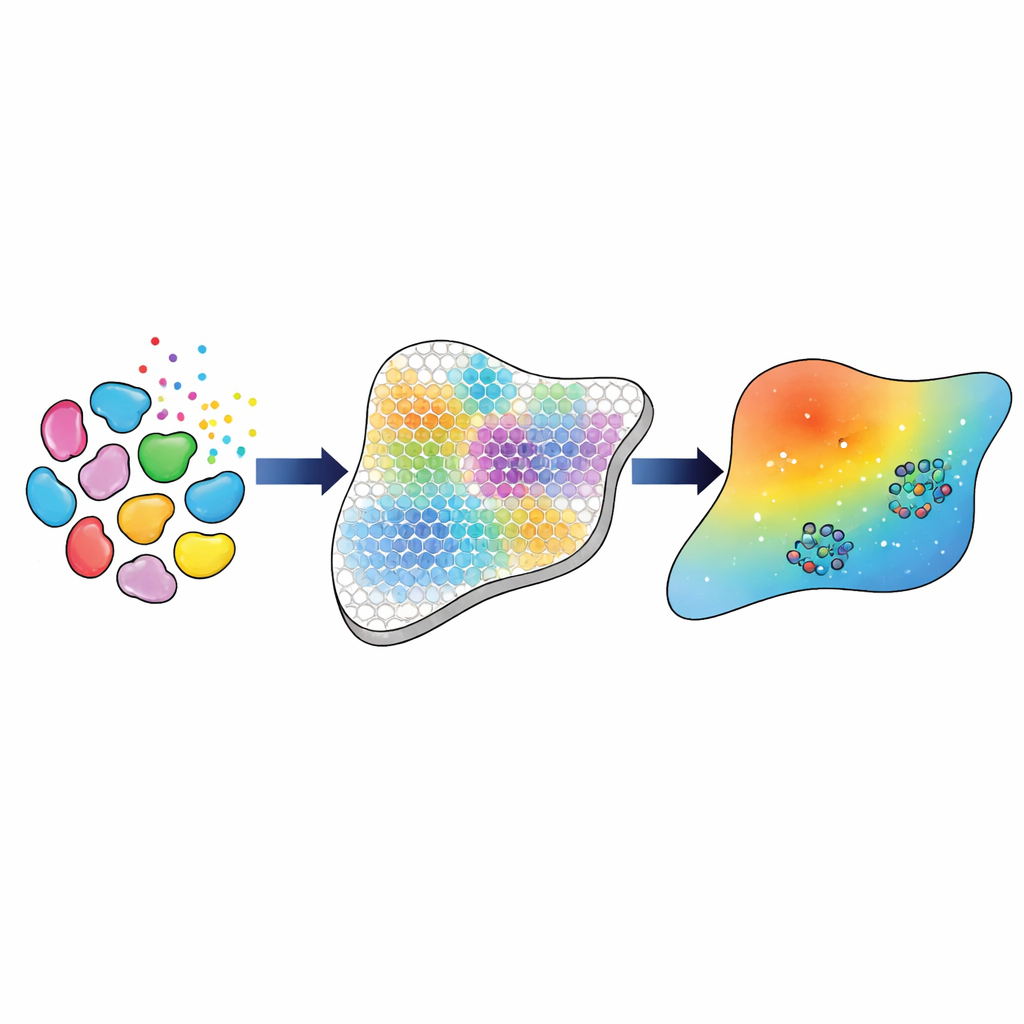
Un flujo de trabajo por etapas desde genes hasta parámetros del modelo
Los investigadores construyen una canalización computacional que conecta estas ricas mediciones genéticas con un modelo a escala tisular del movimiento y la acción del TGFβ. Primero, emplean herramientas bioinformáticas establecidas para identificar los principales tipos y subtipos celulares —como tres clases distintas de fibroblastos, macrófagos y células endoteliales— y estimar cuántos de cada uno están presentes en cada punto de la cuadrícula del tejido. A continuación, infieren cuán fuertemente es probable que cada tipo celular se comunique con otro vía TGFβ, basándose en la actividad génica combinada de ligandos en las células emisoras y de receptores en las células receptoras. Estas “fuerzas de interacción” inferidas sirven como el objetivo experimental que el modelo matemático debe reproducir.
Enseñar al modelo a coincidir con el tejido
A continuación, el equipo representa la propagación del TGFβ por el tejido mediante un conjunto de ecuaciones en derivadas parciales resueltas en una cuadrícula que reproduce la disposición de la transcriptómica espacial. Para cualquier conjunto elegido de valores de parámetros —como la velocidad de difusión del TGFβ, la rapidez de su decaimiento y cuánto produce o absorbe cada tipo celular—, el modelo predice campos de concentración de las tres formas de TGFβ y las fuerzas de interacción resultantes entre tipos celulares. Para ajustar esos parámetros, los autores utilizan una estrategia de calibración en tres fases. Primero aplican métodos bayesianos aproximados para explorar de forma amplia parámetros plausibles informados por experimentos previos, acotando gradualmente combinaciones que correlacionan bien con las fuerzas de interacción derivadas de los datos genéticos. Luego introducen estos candidatos prometedores en un método de optimización basado en gradientes que afina los parámetros para maximizar el acuerdo. Este enfoque híbrido logra una coincidencia lineal casi perfecta (correlación de 0,99) entre las fuerzas de interacción predichas por el modelo y las inferidas a partir de los datos.
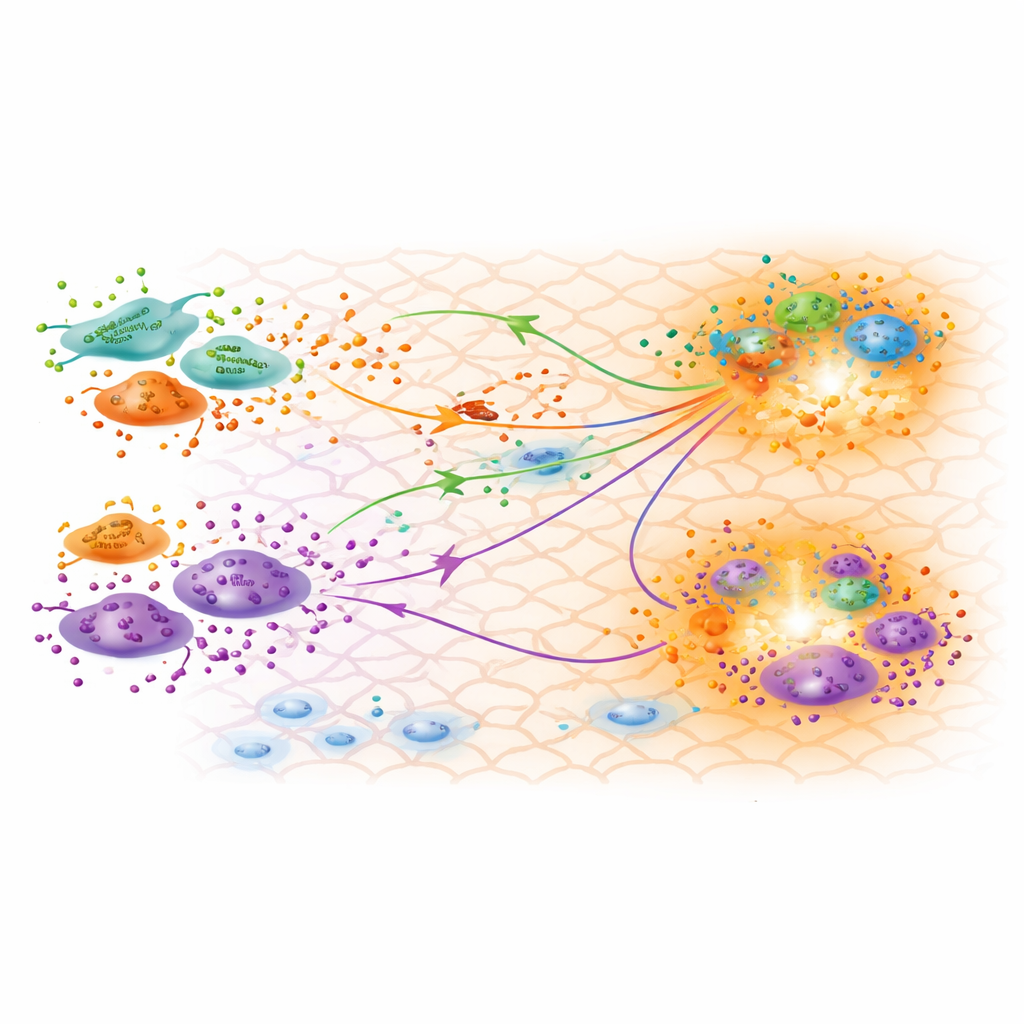
Lo que el modelo calibrado revela sobre la curación
Con un modelo bien ajustado en mano, los investigadores exploran qué indican los parámetros inferidos sobre la biología. Confirman que los tres subtipos de fibroblastos identificados a partir de los datos de expresión génica son funcionalmente distintos, con uno mostrando un perfil fuertemente inflamatorio y otro exhibiendo rasgos de miofibroblastos que ayudan a contraer la herida. Las tasas de producción calibradas sugieren que los fibroblastos proinflamatorios producen menos TGFβ durante la fase de remodelado, coherente con la disminución de la inflamación a los 30 días. Sorprendentemente, un subtipo conocido como fibroblastos papilares parece producir cantidades relativamente altas de TGFβ3, una forma a menudo vinculada con menor formación de cicatrices y resultados más regenerativos. Los mapas de concentración de TGFβ predichos por el modelo se alinean con las regiones donde se agrupan fibroblastos y macrófagos, sugiriendo puntos calientes de intercambio activo que podrían dirigir cómo se forma la cicatriz.
Un marco flexible para otros tejidos y enfermedades
Más allá de este caso específico de cicatrización, la principal contribución del estudio es una canalización general para convertir datos genéticos modernos en modelos tisulares bien calibrados. Al combinar transcriptómica de célula única y espacial con herramientas estadísticas y de optimización avanzadas, los investigadores pueden estimar con mayor rigor qué tan rápido se desplazan los ligandos, con qué fuerza se unen y qué células contribuyen más a la señalización. Este marco puede adaptarse a otros tejidos, otras moléculas de señalización y estados patológicos como la fibrosis o el cáncer, ayudando en última instancia a traducir instantáneas moleculares complejas en modelos predictivos del comportamiento de los tejidos completos.
Cita: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Palabras clave: cicatrización de heridas, señalización celular, transcriptómica espacial, TGF beta, modelado matemático