Clear Sky Science · tr
Doku düzeyi ligand dinamiğinin PDE modellerini tek hücre ve uzamsal transkriptomik verileri kullanarak kalibre etme
Hücreler İyileşen Bir Yarada Nasıl Haberleşir
Derimiz zarar gördüğünde, çok sayıda hücre fazla iz bırakmadan hasarı onarmak için koordineli hareket etmelidir. Bunu, dokuda yayılan ve komşu hücrelerde tepkileri tetikleyen ligand adı verilen kimyasal mesajları gönderip algılayarak yaparlar. Bu çalışma, tek hücreli ve uzamsal çözünürlükteki modern genetik ölçümlerin bu kimyasal mesajların matematiksel modellerini kalibre etmek için güçlü bir araca nasıl dönüştürülebileceğini gösteriyor; böylece araştırmacılar normal iyileşmeyi ve skar oluşturmaya bağlı hastalıkları daha iyi anlayabiliyor.
Dokularda Kimyasal Mesajların Önemi
Dokularımızdaki hücreler nadiren tek başına hareket eder. Sürekli olarak ne zaman bölüneceklerini, hareket edeceklerini veya sakinleşeceklerini söyleyen sinyaller değiş tokuş ederler. Bu sinyallerin çoğu, bir hücre tarafından salınan ve başka bir hücredeki reseptörler tarafından yakalanan kısa menzilli kimyasallardır. Bu tür mesajlar yara iyileşmesi, inflamasyon ve fibroz ile kanser gibi hastalıklar açısından merkezidir. Araştırmacılar, bu kimyasalların nasıl üretildiğini, yayıldığını ve parçalandığını tanımlamak için uzun zamandır reaksiyon–difüzyon modelleri olarak bilinen matematiksel denklemleri kullandı. Ancak gerçekçi parametre değerlerini—örneğin üretim hızları ve bağlanma güçleri—nasıl seçecekleri, böylece modellerin laboratuvar koşullarından ziyade canlı doku içindeki gerçekliği yansıtacağı sorunu uzun zamandır çözülmeyi bekliyordu.
Canlı Dokuya Yeni Bakışlar
Son zamanlarda iki deneysel teknoloji, bilim insanlarının dokuları gözlemleme biçimini dönüştürdü. Tek hücreli RNA dizileme, binlerce bireysel hücrede hangi genlerin aktif olduğunu ölçerek hücre kimliklerini ve sinyal verme kapasitelerini ortaya koyar. Buna karşılık uzamsal transkriptomik, bir doku kesitinde ızgara gibi yerleştirilmiş çok sayıda küçük noktadaki gen aktivitesini ölçerek farklı hücrelerin nerede bulunduğunu korur. Bu çalışmada yazarlar, dokuyun "yeniden şekillenme" aşamasında olduğu, yaralanmadan 30 gün sonra alınmış insan deri örneklerinden her iki veri tipini birleştirir. Yaralanma izi ve doku onarımı üzerinde etkili olduğu bilinen dönüştürücü büyüme faktörü beta (TGFβ) adlı anahtar sinyal molekülünün üç formuna odaklanırlar.
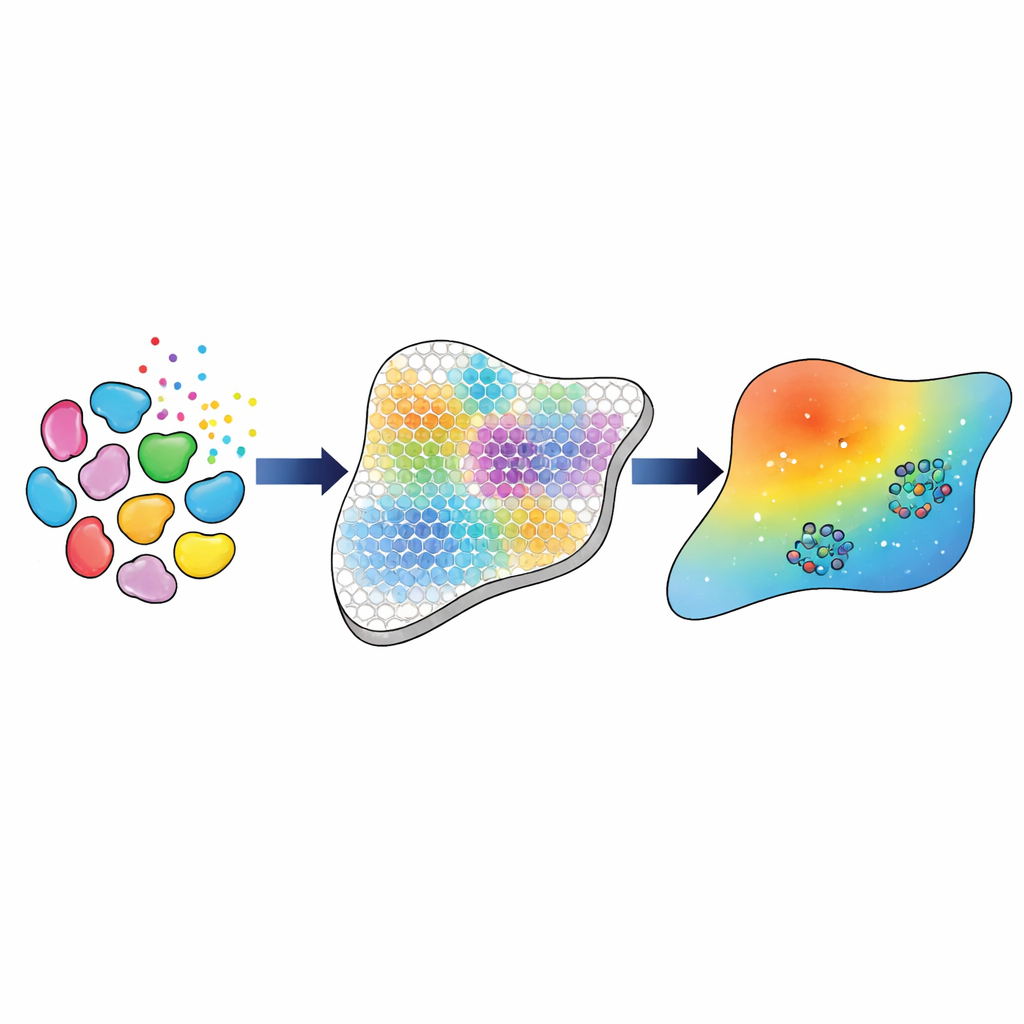
Genlerden Model Parametrelerine Adım Adım Bir İşlem Hattı
Araştırmacılar, bu zengin genetik ölçümleri TGFβ hareketi ve etkisini tanımlayan doku ölçeğinde bir modelle birleştiren hesaplamalı bir işlem hattı kurar. Önce, yerleşik biyoinformatik araçları kullanarak başlıca hücre tiplerini ve alt tiplerini—örneğin üç farklı fibroblast sınıfı, makrofajlar ve endotelyal hücreler—tanımlar ve her doku ızgarası noktasında her birinden kaç tane olduğunu tahmin ederler. Ardından, gönderen hücrelerdeki ligandların ve alan hücrelerdeki reseptörlerin birleşik gen aktivitesine dayalı olarak her hücre tipinin TGFβ yoluyla birbirleriyle ne kadar güçlü konuşma eğiliminde olduğunu çıkarırlar. Bu çıkarılan "etkileşim güçleri", matematiksel modelin yeniden üretmesi gereken deneysel hedef olarak hizmet eder.
Modeli Dokuya Uydurmayı Öğretmek
Sonraki adımda ekip, TGFβ’nin doku içindeki yayılımını uzamsal transkriptomik düzeni yansıtan bir ızgarada çözülen kısmi diferansiyel denklemler kümesi ile temsil eder. Seçilen herhangi bir parametre seti için—örneğin TGFβ’nin ne kadar hızlı difüze olduğu, ne kadar çabuk parçalandığı ve her hücre tipinin ne kadar ürettiği veya absorbe ettiği—model, üç TGFβ formunun konsantrasyon alanlarını ve hücre tipleri arasındaki ortaya çıkan etkileşim güçlerini tahmin eder. Bu parametreleri ayarlamak için yazarlar üç aşamalı bir kalibrasyon stratejisi kullanır. Önce yaklaşık Bayes yöntemleriyle önceki deneylerden bilgilenmiş makul parametreler üzerinde geniş bir tarama yaparak genetik verilere dayalı etkileşim güçleriyle iyi korelasyon gösteren kombinasyonlara doğru kademeli olarak daralırlar. Ardından bu umut verici adayları, parametreleri uyumu maksimize edecek şekilde ince ayar yapan gradient tabanlı bir optimizasyon yöntemine verirler. Bu hibrit yaklaşım, model tarafından tahmin edilen ve veri-sonrası çıkarılan etkileşim güçleri arasında neredeyse mükemmel bir lineer uyum (0.99 korelasyon) elde eder.
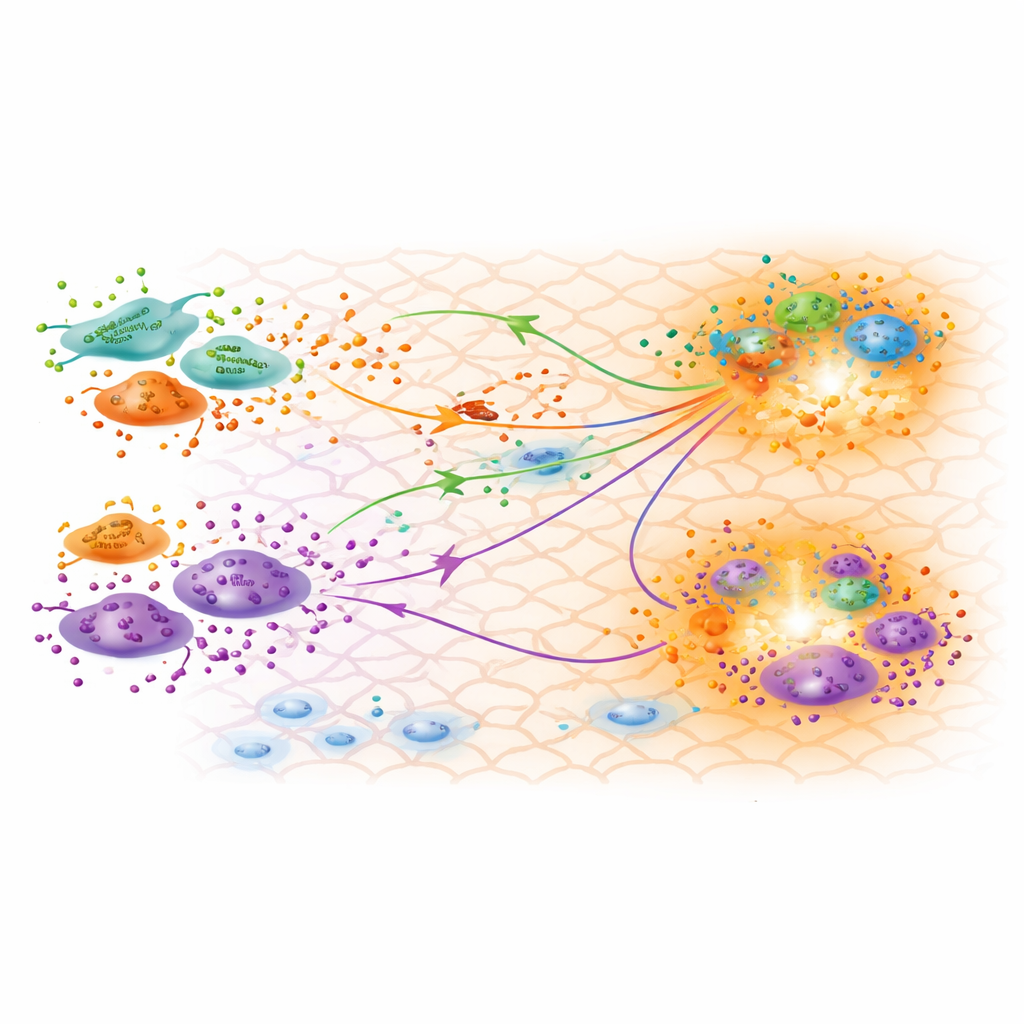
Kalibre Edilmiş Modelin İyileşme Hakkında Ne Anlattığı
İyi uyum sağlamış bir modelle, araştırmacılar çıkarılan parametrelerin biyoloji hakkında ne söylediğini keşfeder. Gen ifade verilerinden tanımlanan üç fibroblast alt tipinin işlevsel olarak farklı olduğunu doğrularlar; bir tanesi güçlü bir inflamatuar profil gösterirken bir diğeri yaranın kasılmasına yardımcı olan myofibroblast özellikleri sergiler. Kalibre edilen üretim hızları, yeniden şekillenme aşamasında pro-inflamatuar fibroblastların en az TGFβ ürettiğini, bunun da 30. günde inflamasyonun yatışmasıyla tutarlı olduğunu gösterir. Sürpriz olarak, papiller fibroblast adı verilen bir alt tipin nispeten yüksek miktarda TGFβ3 ürettiği gözlemlenir; TGFβ3 genellikle daha az skar ve daha rejeneratif sonuçlarla ilişkilidir. Modelin öngördüğü TGFβ konsantrasyon haritaları, fibroblastlar ve makrofajların kümelendiği bölgelerle örtüşerek, yaranın nasıl şekilleneceğini yönlendirebilecek aktif çapraz iletişim merkezlerine işaret eder.
Gelecek Dokular ve Hastalıklar İçin Esnek Bir Çerçeve
Bu özel yara iyileşmesi örneğinin ötesinde, çalışmanın ana katkısı modern genetik verileri iyi kalibre edilmiş doku düzeyi modellere dönüştüren genel bir işlem hattıdır. Tek hücreli ve uzamsal transkriptomiki gelişmiş istatistiksel ve optimizasyon araçlarıyla birleştirerek, araştırmacılar ligandların ne kadar hızlı hareket ettiğini, ne kadar güçlü bağlandığını ve hangi hücrelerin sinyalleşmeye en çok katkıda bulunduğunu daha titizlikle tahmin edebilir. Bu çerçeve diğer dokulara, diğer sinyal moleküllerine ve fibrotik skarlaşma veya kanser gibi hastalık durumlarına uyarlanabilir; nihayetinde karmaşık moleküler anlık görüntüleri bütün doku davranışlarını öngören modellere çevirmeye yardımcı olur.
Atıf: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Anahtar kelimeler: yaraların iyileşmesi, hücre sinyalleşmesi, uzamsal transkriptomik, TGF beta, matematiksel modelleme