Clear Sky Science · nl
Kalibreren van weefselniveau PDE-modellen van liganddynamica met single-cell en ruimtelijke transcriptomica gegevens
Hoe cellen communiceren over een genezende wond
Wanneer onze huid beschadigd raakt, moeten talloze cellen gecoördineerd samenwerken om de schade te herstellen zonder te veel littekenweefsel achter te laten. Ze doen dit door chemische boodschappers, liganden genoemd, uit te zenden en te detecteren; die verspreiden zich door het weefsel en roepen reacties op in naburige cellen. Deze studie toont hoe moderne genetische metingen op single-cell- en ruimtelijke resolutie kunnen worden omgezet in een krachtige nieuwe manier om wiskundige modellen van die chemische boodschappen te kalibreren, wat onderzoekers helpt normale genezing en ziekten gerelateerd aan littekenvorming beter te begrijpen.
Waarom chemische boodschappen van belang zijn in weefsels
Cellen in onze weefsels handelen zelden op zichzelf. Ze wisselen continu signalen uit die aangeven wanneer ze moeten delen, bewegen of tot rust komen. Veel van die signalen zijn kortafstandschemische stoffen die door de ene cel worden vrijgegeven en door receptoren op een andere cel worden opgevangen. Zulke boodschappen zijn centraal bij wondheling, ontsteking en aandoeningen zoals fibrose en kanker. Onderzoekers gebruiken al lange tijd wiskundige vergelijkingen, bekend als reactie–diffusiemodellen, om te beschrijven hoe deze chemicaliën worden geproduceerd, verspreid en afgebroken. Een hardnekkig probleem is echter hoe realistische parameterwaarden te kiezen—zoals productiesnelheden en bindingssterktes—zodat de modellen werkelijk weergeven wat er in levend weefsel gebeurt in plaats van geidealiseerde laboratoriumomstandigheden.
Nieuwe manieren om naar levend weefsel te kijken
Recentelijk hebben twee experimentele technologieën de waarneming van weefsels veranderd. Single-cell RNA-sequencing meet welke genen actief zijn in duizenden individuele cellen, waardoor hun identiteit en signaleringscapaciteiten zichtbaar worden. Ruimtelijke transcriptomica meet daarentegen genactiviteit over vele kleine plekjes die als een raster op een weefselplaat liggen, waardoor de locatie van verschillende cellen behouden blijft. In dit werk combineren de auteurs beide datatypes van humane huidmonsters genomen 30 dagen na verwonding, wanneer het weefsel in de ‘remodellerings’-fase van genezing verkeert. Ze richten zich op drie vormen van een belangrijk signaalmolecuul, transformerende groeifactor beta (TGFβ), waarvan bekend is dat het invloed heeft op littekenvorming en weefselherstel.
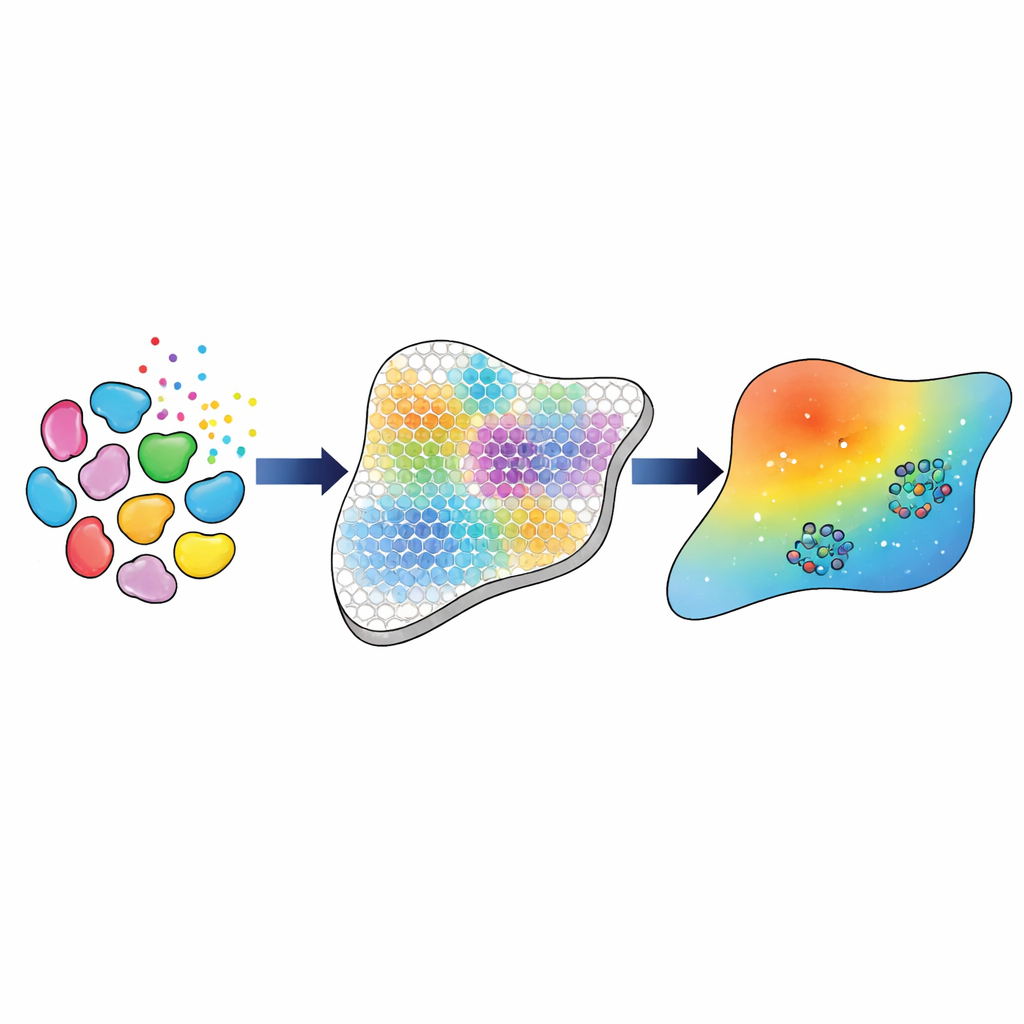
Een stapsgewijze pijplijn van genen naar modelparameters
De onderzoekers bouwen een computationele pijplijn die deze rijke genetische metingen koppelt aan een weefsel-schaalmodel van TGFβ-beweging en -werking. Eerst gebruiken ze gevestigde bioinformatica-instrumenten om de belangrijkste celtypen en subtypen te identificeren—zoals drie verschillende klassen fibroblasten, macrofagen en endotheelcellen—en om te schatten hoeveel van elk type aanwezig is op elk punt in het weefsellijst. Vervolgens leiden ze af hoe sterk elk celtype waarschijnlijk met elk ander communiceert via TGFβ, gebaseerd op de gecombineerde genactiviteit van liganden in zendende cellen en receptoren in ontvangende cellen. Deze afgeleide “interactiekrachten” dienen als het experimentele doel dat het wiskundige model moet reproduceren.
Het model leren overeen te komen met het weefsel
Vervolgens vertegenwoordigt het team de verspreiding van TGFβ door het weefsel met een stel partiële differentiaalvergelijkingen die worden opgelost op een raster dat het ruimtelijke transcriptomica-opzet weerspiegelt. Voor elke gekozen set parameterwaarden—zoals hoe snel TGFβ diffuseert, hoe snel het vervalt, en hoeveel elk celtype produceert of opneemt—voorspelt het model concentratievelden van de drie TGFβ-vormen en de resulterende interactiekrachten tussen celtypen. Om die parameters af te stemmen gebruiken de auteurs een driedelige kalibratiestrategie. Eerst passen ze benaderende Bayesiaanse methoden toe om breed te scannen over redelijke parameters geïnformeerd door eerdere experimenten, en vernauwen ze geleidelijk naar combinaties die goed correleren met de uit de genetische data afgeleide interactiekrachten. Vervolgens voeren ze deze veelbelovende kandidaten in een gradiëntgebaseerde optimalisatiemethode die de parameters verfijnt om overeenstemming te maximaliseren. Deze hybride aanpak bereikt een bijna perfecte lineaire overeenkomst (correlatie van 0,99) tussen model-voorspelde en data-afgeleide interactiekrachten.
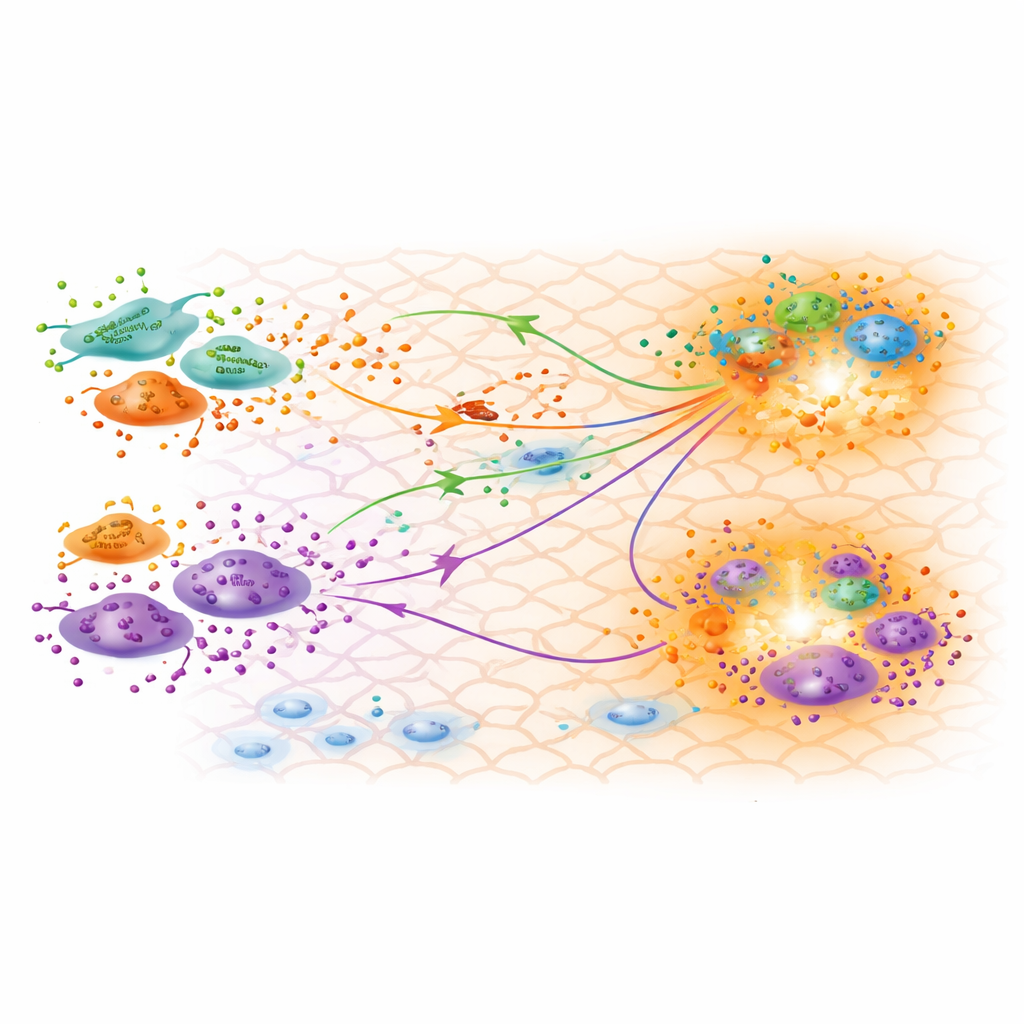
Wat het gekalibreerde model onthult over genezing
Met een goed afgestemd model verkennen de onderzoekers wat de afgeleide parameters over de biologie zeggen. Ze bevestigen dat de drie fibroblast-subtypen die uit genexpressiegegevens zijn geïdentificeerd functioneel verschillend zijn, met één subtype dat een sterk inflammatoir profiel toont en een ander dat kenmerken van myofibroblasten vertoont die helpen de wond te samentrekken. De gekalibreerde productiesnelheden suggereren dat pro-inflammatoire fibroblasten tijdens de remodelleringsfase het minste TGFβ produceren, wat overeenkomt met het afnemen van ontsteking rond dag 30. Verrassend genoeg blijkt een subtype bekend als papillaire fibroblasten relatief hoge hoeveelheden TGFβ3 te produceren, een vorm die vaak geassocieerd wordt met verminderd littekenweefsel en meer regeneratieve uitkomsten. De door het model voorspelde TGFβ-concentratiekaarten sluiten aan bij regio’s waar fibroblasten en macrofagen clusteren, wat wijst op hotspots van actieve kruispratingen die kunnen sturen hoe het litteken zich vormt.
Een flexibel kader voor toekomstige weefsels en ziekten
Voorbij dit specifieke geval van wondheling is de belangrijkste bijdrage van de studie een algemeen bruikbare pijplijn om moderne genetische data om te zetten in goed gekalibreerde weefselniveau-modellen. Door single-cell en ruimtelijke transcriptomica te combineren met geavanceerde statistische en optimalisatietools, kunnen onderzoekers strikter schatten hoe snel liganden zich verplaatsen, hoe sterk ze binden en welke cellen het meest bijdragen aan signalering. Dit kader kan worden aangepast aan andere weefsels, andere signaalmoleculen en ziektebeelden zoals fibrotische littekenvorming of kanker, en helpt uiteindelijk complexe moleculaire snapshots te vertalen naar voorspellende modellen van hoe hele weefsels zich gedragen.
Bronvermelding: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Trefwoorden: wondheling, celsignalering, ruimtelijke transcriptomica, TGF beta, wiskundige modellering