Clear Sky Science · de
Kalibrierung von PDE-Gewebemodellen der Ligandendynamik mithilfe von Einzelzell- und räumlicher Transkriptomikdaten
Wie Zellen über eine heilende Wunde hinweg kommunizieren
Wenn unsere Haut verletzt wird, müssen zahllose Zellen koordiniert zusammenarbeiten, um den Schaden zu reparieren, ohne zu viel Narbengewebe zu hinterlassen. Sie tun dies, indem sie chemische Botenstoffe, so genannte Liganden, aussenden und wahrnehmen; diese breiten sich im Gewebe aus und lösen in benachbarten Zellen Reaktionen aus. Diese Studie zeigt, wie moderne genetische Messungen auf Einzelzell- und räumlicher Ebene in eine leistungsfähige neue Methode zur Kalibrierung mathematischer Modelle dieser chemischen Signale verwandelt werden können, was Forschern hilft, normale Heilungsprozesse und narbenbedingte Erkrankungen besser zu verstehen.
Warum chemische Botschaften im Gewebe wichtig sind
Zellen in unserem Gewebe agieren selten allein. Sie tauschen ständig Signale aus, die ihnen sagen, wann sie sich teilen, bewegen oder beruhigen sollen. Viele dieser Signale sind kurzreichweitige Chemikalien, die von einer Zelle freigesetzt und von Rezeptoren einer anderen Zelle gebunden werden. Solche Botschaften sind zentral für Wundheilung, Entzündung und Krankheiten wie Fibrose und Krebs. Forscher verwenden seit langem mathematische Gleichungen, so genannte Reaktions–Diffusions-Modelle, um zu beschreiben, wie diese Chemikalien produziert, verteilt und abgebaut werden. Ein langjähriges Problem war jedoch, wie man realistische Parameterwerte — etwa Produktionsraten und Bindungsstärken — wählt, sodass die Modelle tatsächlich widerspiegeln, was im lebenden Gewebe passiert, statt idealisierter Laborbedingungen.
Neue Einblicke in lebendes Gewebe
Kürzlich haben zwei experimentelle Technologien die Beobachtungsmöglichkeiten für Gewebe transformiert. Einzelzell-RNA-Sequenzierung misst, welche Gene in Tausenden einzelner Zellen aktiv sind und offenbart so deren Identität und Signalfähigkeiten. Räumliche Transkriptomik hingegen misst die Genaktivität über viele winzige Punkte, die wie ein Gitter auf einem Gewebeschnitt angeordnet sind, und bewahrt dabei die Lage verschiedener Zellen. In dieser Arbeit kombinieren die Autoren beide Datentypen aus menschlichen Hautproben, die 30 Tage nach einer Verletzung entnommen wurden, wenn sich das Gewebe in der sogenannten "Remodelling"-Phase der Heilung befindet. Sie konzentrieren sich auf drei Varianten eines Schlüssel-Botenstoffs, des Transforming Growth Factor beta (TGFβ), der dafür bekannt ist, die Narbenbildung und Gewebereparatur zu beeinflussen.
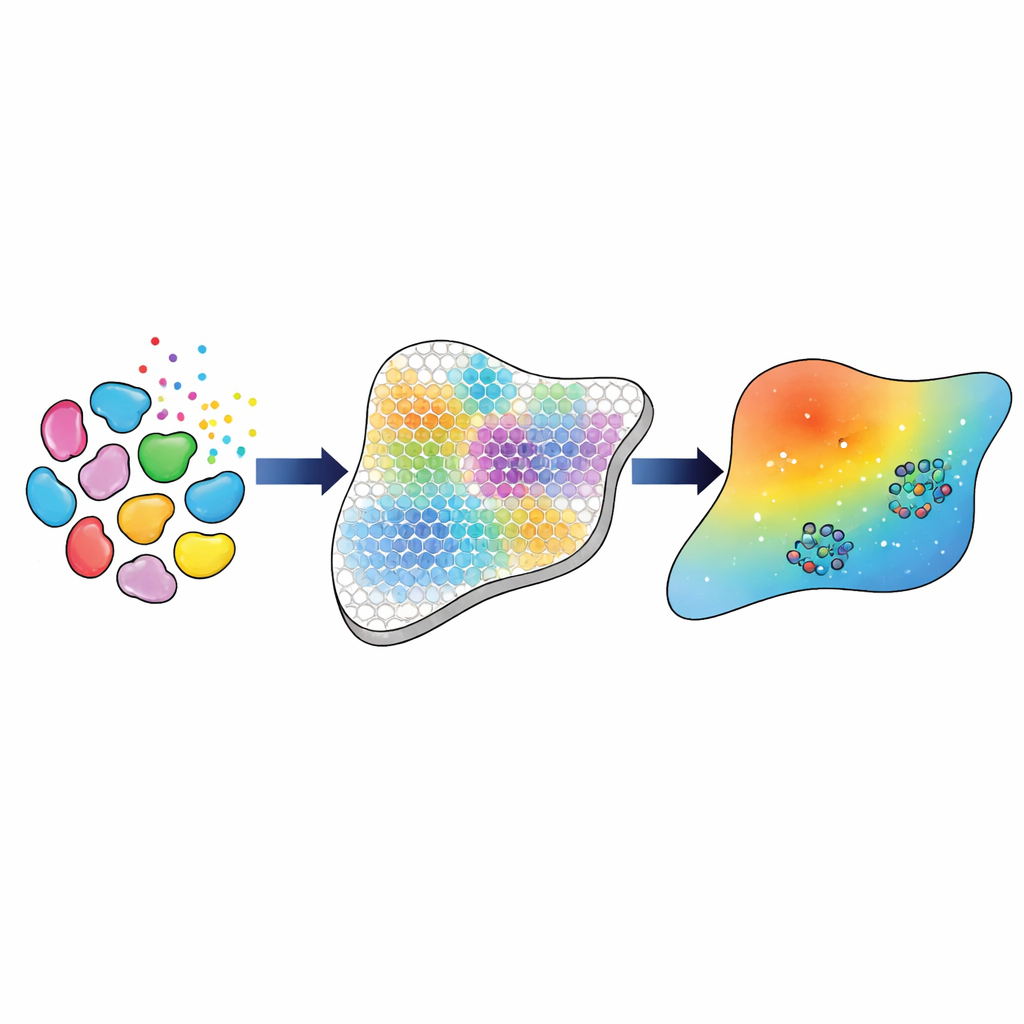
Eine schrittweise Pipeline von Genen zu Modellparametern
Die Forschenden bauen eine rechnerische Pipeline auf, die diese umfangreichen genetischen Messungen mit einem Gewebe-Modell für Bewegung und Wirkung von TGFβ verbindet. Zunächst verwenden sie etablierte Bioinformatik-Werkzeuge, um die Hauptzelltypen und -subtypen zu identifizieren — etwa drei unterschiedliche Klassen von Fibroblasten, Makrophagen und Endothelzellen — und abzuschätzen, wie viele von jedem Typ an jedem Punkt des Gewebegitters vorhanden sind. Anschließend leiten sie daraus ab, wie stark jeder Zelltyp wahrscheinlich über TGFβ miteinander kommuniziert, basierend auf der kombinierten Genaktivität von Liganden in sendenden Zellen und Rezeptoren in empfangenden Zellen. Diese abgeleiteten „Interaktionsstärken“ dienen als experimentelles Ziel, das das mathematische Modell reproduzieren muss.
Das Modell lehren, dem Gewebe zu entsprechen
Im nächsten Schritt stellen die Autoren die Ausbreitung von TGFβ im Gewebe durch ein System partieller Differentialgleichungen dar, das auf einem Gitter gelöst wird, das dem Layout der räumlichen Transkriptomik entspricht. Für jede gewählte Parameterkombination — etwa wie schnell TGFβ diffundiert, wie rasch es zerfällt und wie viel jeder Zelltyp produziert oder aufnimmt — sagt das Modell Konzentrationsfelder der drei TGFβ-Formen und die daraus resultierenden Interaktionsstärken zwischen Zelltypen voraus. Um diese Parameter zu justieren, verwenden die Autoren eine dreistufige Kalibrierungsstrategie. Sie wenden zunächst approximative Bayes-Verfahren an, um breit über plausible Parameter zu suchen, gestützt auf vorhergehende Experimente, und eingrenzend jene Kombinationen zu identifizieren, die gut mit den aus den genetischen Daten abgeleiteten Interaktionsstärken korrelieren. Diese vielversprechenden Kandidaten werden dann in ein gradientenbasiertes Optimierungsverfahren eingespeist, das die Parameter feinabstimmt, um die Übereinstimmung zu maximieren. Dieser hybride Ansatz erzielt eine nahezu perfekte lineare Übereinstimmung (Korrelation von 0,99) zwischen modellvorhergesagten und datenabgeleiteten Interaktionsstärken.
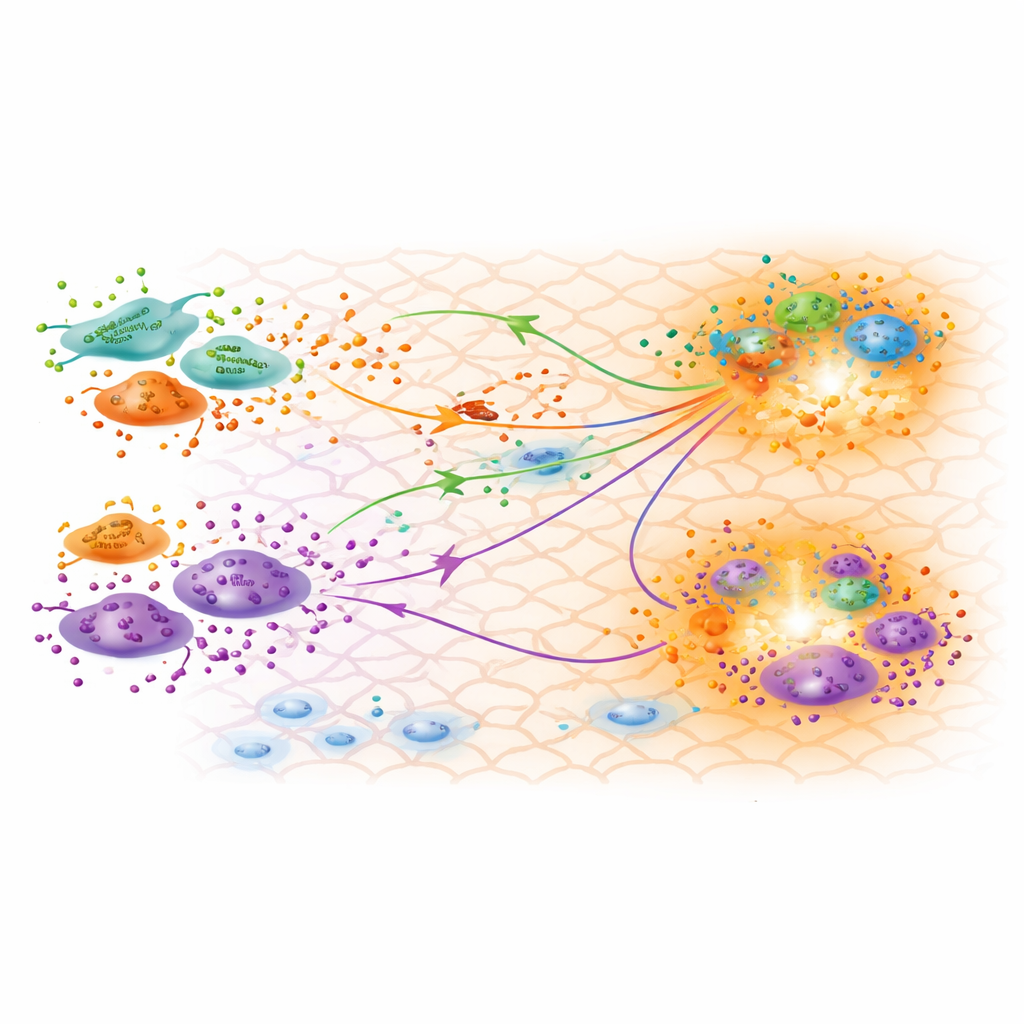
Was das kalibrierte Modell über die Heilung aussagt
Mit einem gut angepassten Modell in der Hand untersuchen die Forschenden, was die abgeleiteten Parameter über die Biologie aussagen. Sie bestätigen, dass die drei Fibroblasten-Subtypen, die aus den Genexpressionsdaten identifiziert wurden, funktionell unterschiedlich sind: Einer zeigt ein starkes inflammatorisches Profil, ein anderer Merkmale von Myofibroblasten, die bei der Wundkontraktion helfen. Die kalibrierten Produktionsraten legen nahe, dass proinflammatorische Fibroblasten in der Remodelling-Phase die geringste TGFβ-Produktion aufweisen, was mit dem Abklingen der Entzündung bis Tag 30 übereinstimmt. Überraschenderweise scheint ein Subtyp, bekannt als papilläre Fibroblasten, relativ hohe Mengen an TGFβ3 zu produzieren — eine Form, die oft mit geringerer Narbenbildung und regenerativeren Ergebnissen assoziiert wird. Die vom Modell vorhergesagten TGFβ-Konzentrationskarten stimmen mit Regionen überein, in denen Fibroblasten und Makrophagen gehäuft auftreten, was auf Hotspots aktiven Austauschs hindeutet, die die Narbenbildung steuern könnten.
Ein flexibles Framework für künftige Gewebe und Krankheiten
Über diesen spezifischen Fall der Wundheilung hinaus besteht der Hauptbeitrag der Studie in einer allgemeinen Pipeline zur Umwandlung moderner genetischer Daten in gut kalibrierte Gewebe-Modelle. Durch die Kombination von Einzelzell- und räumlicher Transkriptomik mit fortgeschrittenen statistischen und Optimierungswerkzeugen können Forschende fundierter abschätzen, wie schnell Liganden sich ausbreiten, wie stark sie binden und welche Zellen am meisten zur Signalübertragung beitragen. Dieses Framework lässt sich an andere Gewebe, andere Signalstoffe und Krankheitszustände wie fibrotische Narbenbildung oder Krebs anpassen und trägt letztlich dazu bei, komplexe molekulare Momentaufnahmen in prädiktive Modelle für das Verhalten ganzer Gewebe zu übersetzen.
Zitation: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Schlüsselwörter: Wundheilung, Zellkommunikation, räumliche Transkriptomik, TGF beta, mathematische Modellierung