Clear Sky Science · sv
Kalibrering av vävnadsnivå PDE‑modeller för liganddynamik med hjälp av single cell- och spatialtranskriptomikdata
Hur celler kommunicerar över ett läkande sår
När vår hud skadas måste otaliga celler samordna sig för att reparera skadan utan att lämna för mycket ärrvävnad. De gör detta genom att sända och uppfatta kemiska budskap kallade ligander, som sprider sig genom vävnaden och utlöser svar i närliggande celler. Denna studie visar hur moderna genetiska mätningar på single‑cell‑ och spatial nivå kan omvandlas till ett kraftfullt nytt sätt att kalibrera matematiska modeller av dessa kemiska budskap, vilket hjälper forskare att bättre förstå normal läkning och sjukdomar relaterade till ärrbildning.
Varför kemiska budskap är viktiga i vävnader
Celler i våra vävnader agerar sällan ensamma. De utbyter ständigt signaler som talar om när de ska dela sig, förflytta sig eller lugna ner sig. Många av dessa signaler är kortväga kemikalier som frisätts av en cell och fångas upp av receptorer på en annan. Sådana budskap är centrala för sårläkning, inflammation och sjukdomar som fibros och cancer. Forskare har länge använt matematiska ekvationer, kända som reaktion–diffusionsmodeller, för att beskriva hur dessa kemikalier produceras, sprids och bryts ner. Ett långvarigt problem har dock varit hur man väljer realistiska parameter‑värden — såsom produktionshastigheter och bindningsstyrkor — så att modellerna verkligen speglar vad som händer i levande vävnad snarare än idealiserade laboratorieförhållanden.
Nya ögon på levande vävnad
På senare tid har två experimentella tekniker förändrat hur forskare kan observera vävnader. Single‑cell RNA‑sekvensering mäter vilka gener som är aktiva i tusentals enskilda celler, och avslöjar deras identiteter och signaleringskapaciteter. Spatial transkriptomik mäter däremot genaktivitet över många små punkter ordnade som ett rutnät på en vävnadsskiva, vilket bevarar var olika celler är belägna. I detta arbete kombinerar författarna båda datatyperna från humana hudprover tagna 30 dagar efter sårning, när vävnaden befinner sig i det så kallade ”remodelleringsstadiet” av läkningsprocessen. De fokuserar på tre varianter av ett nyckelsignalmolekyl, transformerande tillväxtfaktor beta (TGFβ), som är känd för att påverka ärrbildning och vävnadsreparation.
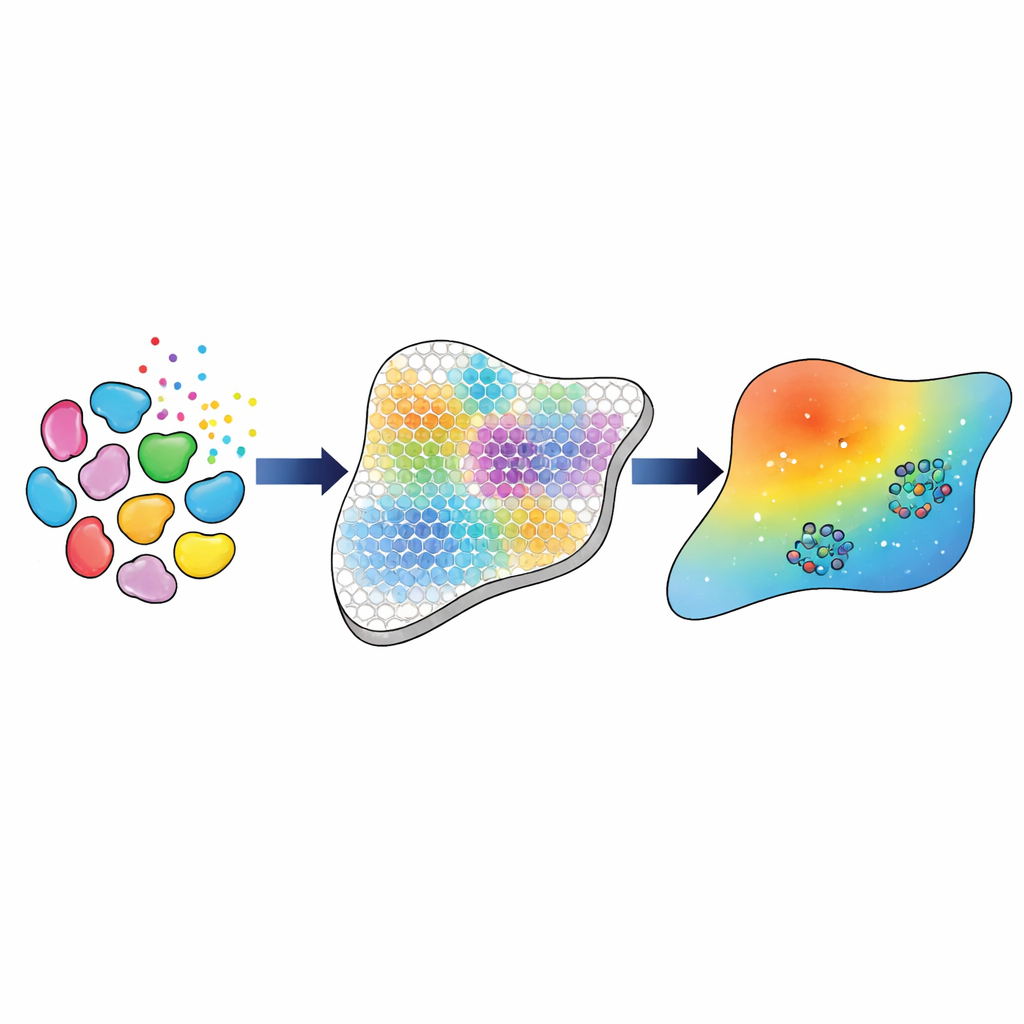
En stegvis pipeline från gener till modellparametrar
Forskarna bygger en beräkningspipeline som kopplar dessa rika genetiska mätningar till en vävnadsskale modell för TGFβ‑rörelse och verkan. Först använder de etablerade bioinformatiska verktyg för att identifiera huvudcelltyper och undertyper — såsom tre distinkta klasser av fibroblaster, makrofager och endotelceller — och för att uppskatta hur många av varje som finns vid varje punkt i vävnadsrutnätet. Därefter härleder de hur starkt varje celltyp sannolikt kommunicerar med varandra via TGFβ, baserat på den kombinerade genaktiviteten hos ligander i sändande celler och receptorer i mottagande celler. Dessa härledda ”interaktionsstyrkor” fungerar som det experimentella målet som den matematiska modellen måste reproducera.
Att lära modellen att matcha vävnaden
Nästa steg representerar teamet TGFβ:s spridning genom vävnaden med ett system av partiella differentialekvationer som löses på ett rutnät som återspeglar spatialtranskriptomikens layout. För varje valt uppsättning parameter‑värden — såsom hur snabbt TGFβ diffunderar, hur snabbt det sönderfaller och hur mycket varje celltyp producerar eller absorberar — förutser modellen koncentrationsfält för de tre TGFβ‑formerna och de resulterande interaktionsstyrkorna mellan celltyper. För att ställa in dessa parametrar använder författarna en trestegs kalibreringsstrategi. Först använder de approximativa bayesianska metoder för att brett söka över plausibla parametrar informerade av tidigare experiment, och avsmalnar gradvis till kombinationer som korrelerar väl med de interaktionsstyrkor som härletts från den genetiska datan. De lovande kandidaterna matas sedan in i en gradientbaserad optimeringsmetod som finslipar parametrarna för att maximera överensstämmelsen. Denna hybrida strategi uppnår en nästan perfekt linjär överensstämmelse (korrelation 0,99) mellan modellpredicerade och data‑härledda interaktionsstyrkor.
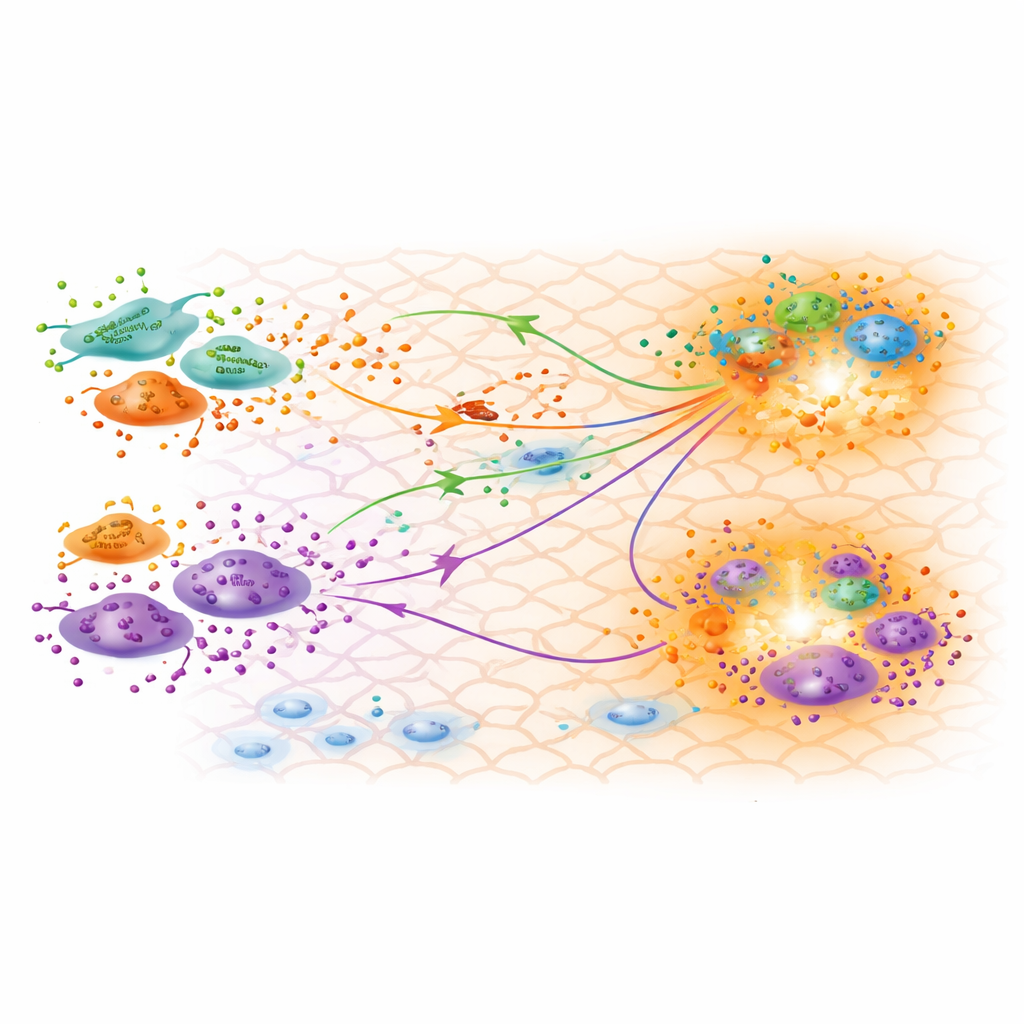
Vad den kalibrerade modellen avslöjar om läkning
Med en välmatchad modell i handen utforskar forskarna vad de härledda parametrarna säger om biologin. De bekräftar att de tre fibroblast‑undertyperna som identifierats från genuttrycksdata är funktionellt skilda, där en visar en stark inflammatorisk profil och en annan uppvisar kännetecken för myofibroblaster som hjälper till att dra ihop såret. De kalibrerade produktionshastigheterna tyder på att proinflammatoriska fibroblaster producerar minst TGFβ under remodelleringsstadiet, i linje med att inflammationen avklingar vid dag 30. Överraskande nog verkar en undertyp känd som papillär fibroblast producera relativt höga mängder TGFβ3, en form som ofta förknippas med mindre ärrbildning och mer regenerativa utfall. Modellens förutsagda TGFβ‑koncentrationskartor överensstämmer med regioner där fibroblaster och makrofager klustrar sig, vilket antyder hotspots för aktiv kommunikation som kan styra hur ärret formas.
Ett flexibelt ramverk för framtida vävnader och sjukdomar
Utöver detta specifika fall av sårläkning är studiens huvudbidrag en generell pipeline för att omvandla moderna genetiska data till välkalibrerade vävnadsmodeller. Genom att kombinera single‑cell och spatial transkriptomik med avancerade statistiska och optimeringsverktyg kan forskare mer rigoröst uppskatta hur snabbt ligander rör sig, hur starkt de binder, och vilka celler som bidrar mest till signaleringen. Detta ramverk kan anpassas till andra vävnader, andra signalmolekyler och sjukdomstillstånd såsom fibrotisk ärrbildning eller cancer, och hjälper i förlängningen till att omvandla komplexa molekylära ögonblicksbilder till prediktiva modeller av hur hela vävnader beter sig.
Citering: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Nyckelord: sårläkning, cellsignalering, spatial transkriptomik, TGF beta, matematisk modellering