Clear Sky Science · fr
Calibrage de modèles aux échelles tissulaires (EDP) de la dynamique des ligands à partir de données de transcriptomique unicellulaire et spatiale
Comment les cellules communiquent à travers une plaie en cours de cicatrisation
Lorsque notre peau est blessée, d’innombrables cellules doivent se coordonner pour réparer la lésion sans laisser d’excès de tissu cicatriciel. Elles le font en envoyant et en détectant des messages chimiques appelés ligands, qui se propagent dans le tissu et déclenchent des réponses chez les cellules voisines. Cette étude montre comment des mesures génétiques modernes, à résolution unicellulaire et spatiale, peuvent être transformées en une nouvelle méthode puissante pour calibrer des modèles mathématiques de ces signaux chimiques, aidant les chercheurs à mieux comprendre la cicatrisation normale et les maladies liées à la formation de cicatrices.
Pourquoi les messages chimiques sont importants dans les tissus
Les cellules de nos tissus agissent rarement de façon isolée. Elles échangent constamment des signaux qui leur indiquent quand se diviser, se déplacer ou se mettre au repos. Nombre de ces signaux sont des molécules à courte portée libérées par une cellule et captées par des récepteurs sur une autre. Ces messages sont centraux dans la cicatrisation, l’inflammation et des maladies comme la fibrose et le cancer. Les chercheurs utilisent depuis longtemps des équations mathématiques, dites de réaction–diffusion, pour décrire comment ces molécules sont produites, se diffusent et sont dégradées. Pourtant, un problème persistant est de choisir des valeurs de paramètres réalistes — telles que les taux de production et les forces de liaison — pour que les modèles reflètent réellement ce qui se passe dans le tissu vivant plutôt que des conditions expérimentales idéalisées.
De nouveaux regards sur le tissu vivant
Récemment, deux technologies expérimentales ont transformé la façon dont les scientifiques observent les tissus. Le séquençage d’ARN unicellulaire mesure quels gènes sont actifs dans des milliers de cellules individuelles, révélant leur identité et leur capacité de signalisation. La transcriptomique spatiale, en revanche, mesure l’activité génique sur de nombreux petits points disposés comme une grille sur une coupe de tissu, conservant la localisation des différents types cellulaires. Dans ce travail, les auteurs combinent ces deux types de données issues d’échantillons de peau humaine prélevés 30 jours après une blessure, lorsque le tissu est en phase de « remodelage » de la cicatrisation. Ils se concentrent sur trois formes d’un signal clé, le facteur de croissance transformant bêta (TGFβ), connu pour influencer la formation de cicatrices et la réparation tissulaire.
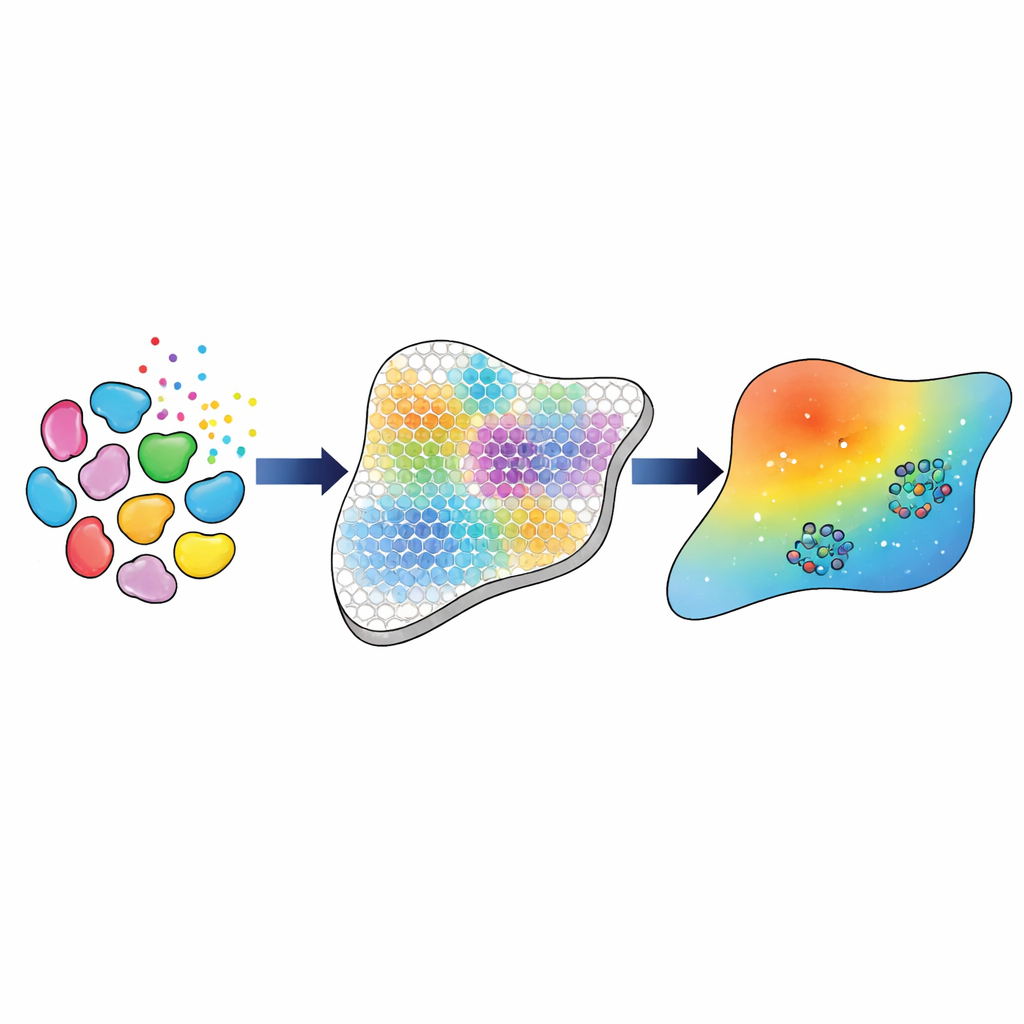
Un pipeline étape par étape des gènes aux paramètres du modèle
Les chercheurs construisent un pipeline computationnel qui relie ces riches mesures génétiques à un modèle à l’échelle tissulaire du mouvement et de l’action du TGFβ. D’abord, ils utilisent des outils bioinformatiques établis pour identifier les principaux types et sous-types cellulaires — comme trois classes distinctes de fibroblastes, des macrophages et des cellules endothéliales — et estimer combien de chacun sont présents à chaque point de la grille spatiale. Ils infèrent ensuite la force avec laquelle chaque type cellulaire est susceptible de communiquer via le TGFβ, en se basant sur l’activité combinée des gènes codant les ligands dans les cellules émettrices et des récepteurs dans les cellules réceptrices. Ces « forces d’interaction » déduites servent de cible expérimentale que le modèle mathématique doit reproduire.
Apprendre au modèle à correspondre au tissu
Ensuite, l’équipe représente la diffusion du TGFβ dans le tissu par un jeu d’équations aux dérivées partielles résolues sur une grille qui reflète la disposition de la transcriptomique spatiale. Pour un ensemble donné de valeurs de paramètres — telles que la vitesse de diffusion du TGFβ, sa vitesse de dégradation et la quantité produite ou absorbée par chaque type cellulaire — le modèle prédit les champs de concentration des trois formes de TGFβ et les forces d’interaction résultantes entre types cellulaires. Pour ajuster ces paramètres, les auteurs emploient une stratégie de calibration en trois étapes. Ils appliquent d’abord des méthodes bayésiennes approchées pour explorer largement des paramètres plausibles informés par des expériences antérieures, rétrécissant progressivement vers des combinaisons qui corrèlent bien avec les forces d’interaction dérivées des données génétiques. Ils injectent ensuite ces candidats prometteurs dans une méthode d’optimisation à base de gradient qui affine les paramètres pour maximiser l’accord. Cette approche hybride atteint une correspondance linéaire quasi parfaite (corrélation de 0,99) entre les forces d’interaction prédites par le modèle et celles inférées des données.
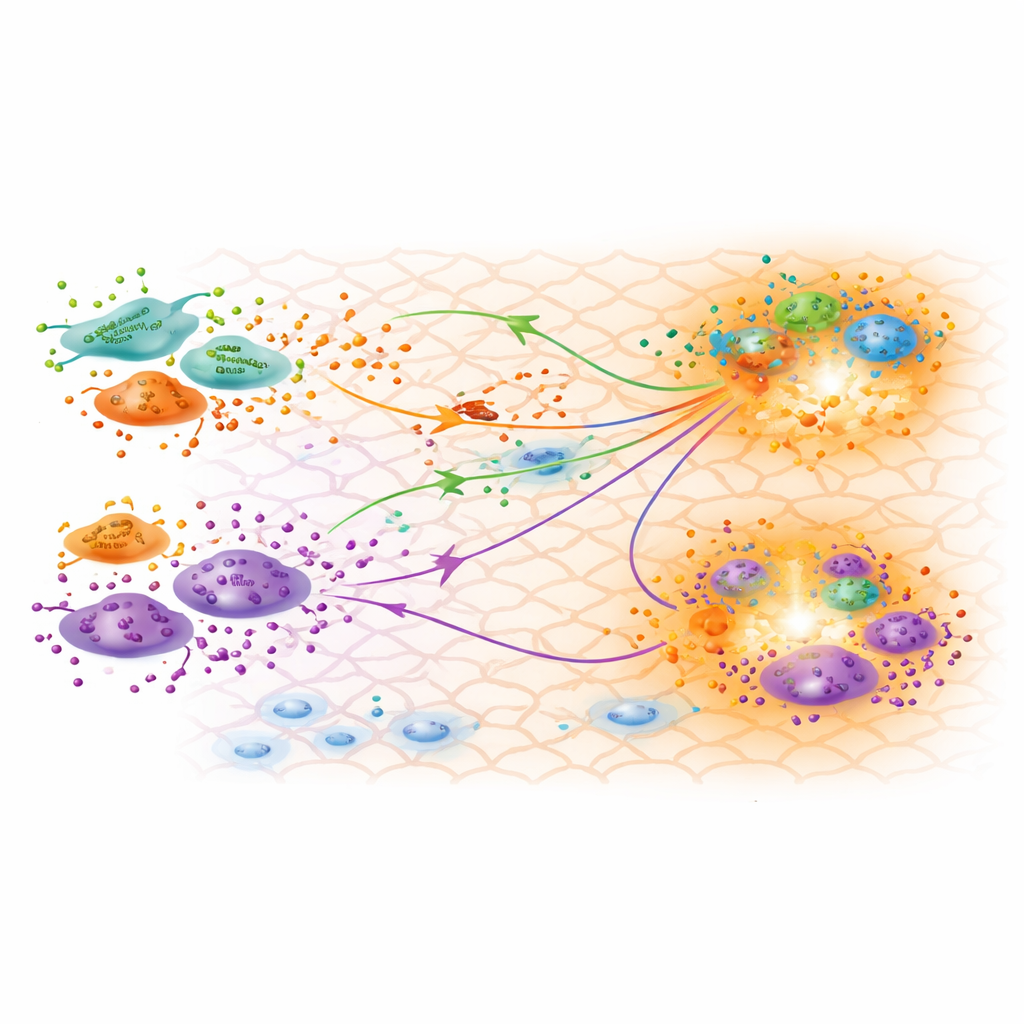
Ce que révèle le modèle calibré sur la cicatrisation
Avec un modèle bien ajusté, les chercheurs explorent ce que disent les paramètres inferés sur la biologie. Ils confirment que les trois sous-types de fibroblastes identifiés par l’expression génique sont fonctionnellement distincts, l’un présentant un profil fortement inflammatoire et un autre des caractéristiques de myofibroblastes participant à la contraction de la plaie. Les taux de production calibrés suggèrent que les fibroblastes pro-inflammatoires produisent le moins de TGFβ durant la phase de remodelage, cohérent avec une inflammation résorbée au jour 30. De façon surprenante, un sous-type connu comme fibroblastes papillaires semble produire des quantités relativement élevées de TGFβ3, une forme souvent associée à une réduction des cicatrices et à des issues plus régénératives. Les cartes de concentration de TGFβ prédites par le modèle s’alignent sur des régions où se regroupent fibroblastes et macrophages, suggérant des points chauds de communication active susceptibles d’orienter la formation de la cicatrice.
Un cadre flexible pour d’autres tissus et maladies
Au-delà de ce cas de cicatrisation particulier, la contribution principale de l’étude est un pipeline général pour transformer des données génétiques modernes en modèles tissulaires bien calibrés. En combinant transcriptomique unicellulaire et spatiale avec des outils statistiques et d’optimisation avancés, les chercheurs peuvent estimer de manière plus rigoureuse la vitesse de déplacement des ligands, la force de leurs liaisons et les cellules qui contribuent le plus à la signalisation. Ce cadre peut être adapté à d’autres tissus, à d’autres molécules de signalisation et à des états pathologiques comme la fibrose cicatricielle ou le cancer, aidant finalement à traduire des instantanés moléculaires complexes en modèles prédictifs du comportement des tissus entiers.
Citation: Daher, A., Trucu, D. & Eftimie, R. Calibrating tissue level PDE models of ligand dynamics using single cell and spatial transcriptomics data. npj Syst Biol Appl 12, 44 (2026). https://doi.org/10.1038/s41540-026-00657-8
Mots-clés: cicatrisation, signalisation cellulaire, transcriptomique spatiale, TGF bêta, modélisation mathématique