Clear Sky Science · zh
网络建模散发性结直肠癌揭示环氧合酶抑制剂的非靶向效应重要性
这对肠道健康和癌症为何重要
结直肠癌是全球最常见的癌症之一,许多人已经在服用影响该疾病相关通路的止痛药。本研究提出了一个具有重大影响的实际问题:当被称为 COX 抑制剂的药物似乎减缓或预防肠道肿瘤时,这究竟是它们的主要预期作用,还是细胞内其他“非靶向”效应在起作用?通过构建结肠细胞及其炎性微环境的详细数字模型,作者探讨了这些药物在何时以及如何真正将系统从失控增殖重新拉回到正常细胞更新的平衡。
解开复杂的信号网络
结肠肿瘤并非由单一基因损伤引起,而是源于肠道细胞、免疫细胞和炎性分子之间错综复杂的信号网络。研究者构建了一个大型的开关(布尔)网络,包含典型肠上皮细胞及其邻近免疫环境中 87 个关键成分。这些成分包括众所周知的促生长因子、抑制细胞死亡的分子以及炎症期间释放的介质。随后他们让该虚拟网络运行数千次,追踪“增殖”节点(细胞分裂)和“凋亡”节点(程序性细胞死亡)被激活的频率。该方法使他们能够测试不同条件——例如慢性炎症或常见的癌症相关基因变化——如何转移系统的整体行为。
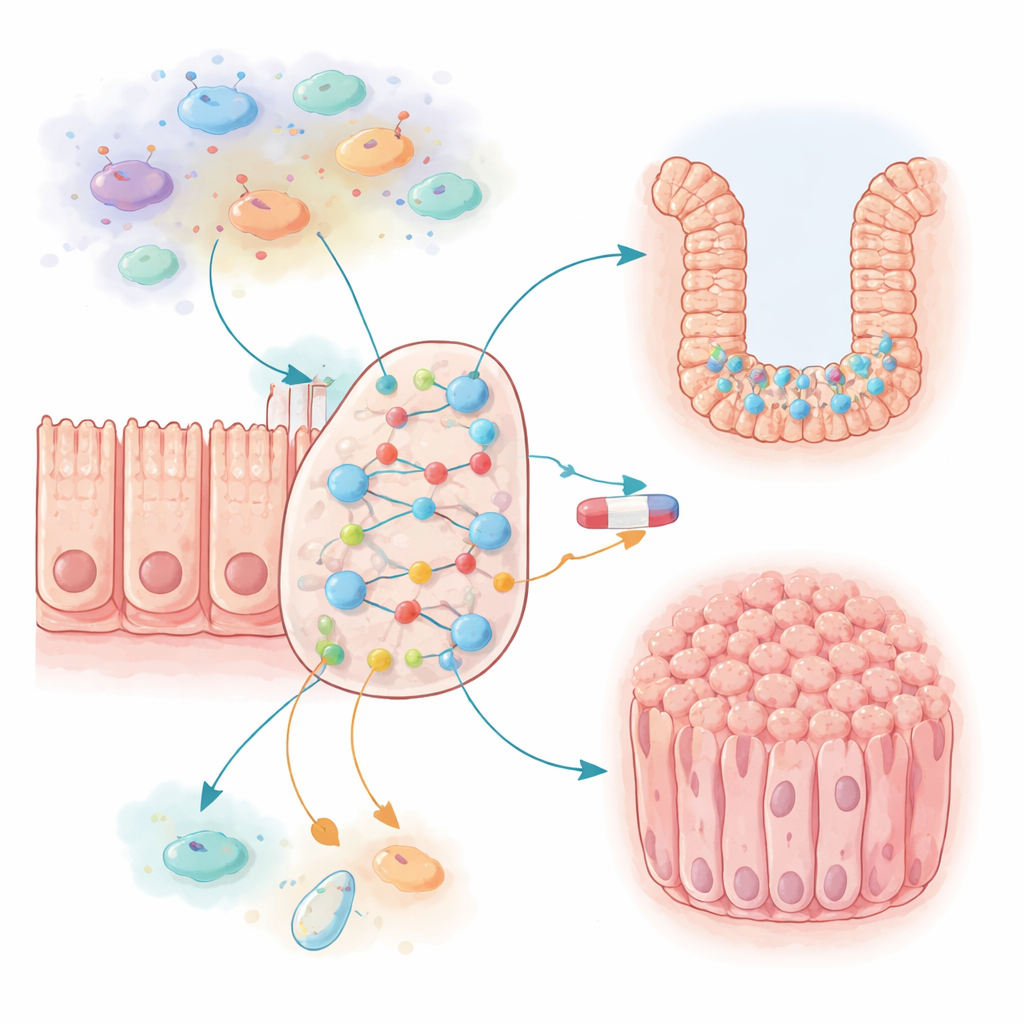
当炎症将细胞锁定在增殖模式时
团队在模型中开启炎性环境时得到的第一个意外发现是,像 IL6 和 CCL2 这样的信号由免疫细胞和上皮细胞产生,形成了两个互相强化的反馈回路,强烈提升了生长通路并抑制了细胞死亡。如果这些信号以全强度作用,模型中的结肠细胞会变得几乎无限增殖且难以被消除——这与健康组织的状况相差甚远。通过降低 IL6 和 CCL2 激活的概率,作者发现了一个平衡点:细胞维持较低、正常的生长速率,但仍能对炎性刺激作出反应。某些免疫细胞的持续激活会产生一种慢性状态,降低细胞死亡并略微提高增殖,模拟了长期炎症如何使肠黏膜更易发生癌变的过程。
常见基因改变如何将细胞推向边缘
接着,研究者在模型中引入了散发性结直肠癌中常见的基因改变,例如丧失 APC “守门员”基因、RAS 的激活性突变,以及守护基因 p53 的丧失。在模型里,这些改变各自以不同方式汇入相同的两个正反馈回路。结果表现为向生存和增殖明显偏移:细胞死亡信号下降,而生长信号激增。相比之下,模拟丢失包含 SMAD 和 DCC 的染色体区域——在真实患者中与不良预后相关的改变——在模型中几乎不影响增殖或凋亡,这表明这些基因控制的通路在模型中代表性不足,可能需要更详细的建模以匹配临床现实。
非靶向作用决定药物是否有益
研究的核心是观察阻断不同药物靶点如何影响该网络,特别是常见 COX 抑制剂(如塞来昔布和苏林达克)作用的靶点。当模拟细胞中唯一的问题是 APC 丧失时,直接阻断 COX2 或相关酶(例如 PDE5)能够完全恢复健康平衡:增殖下降,细胞死亡上升至正常以上,早期打断了反馈回路。但随着 RAS 和 p53 的额外突变叠加——代表中晚期肿瘤阶段——单纯阻断 COX2 的效果甚微。在这些晚期情形中,抑制以 AKT 为中心的生长通路,或在较小程度上抑制 NF-κB,对减缓增殖更为有效,尽管仍无法完全恢复细胞死亡。模型还提示,塞来昔布能够同时作用于 AKT 与 COX2,因此在存在多重突变时,抑制肿瘤细胞生长方面应优于苏林达克。
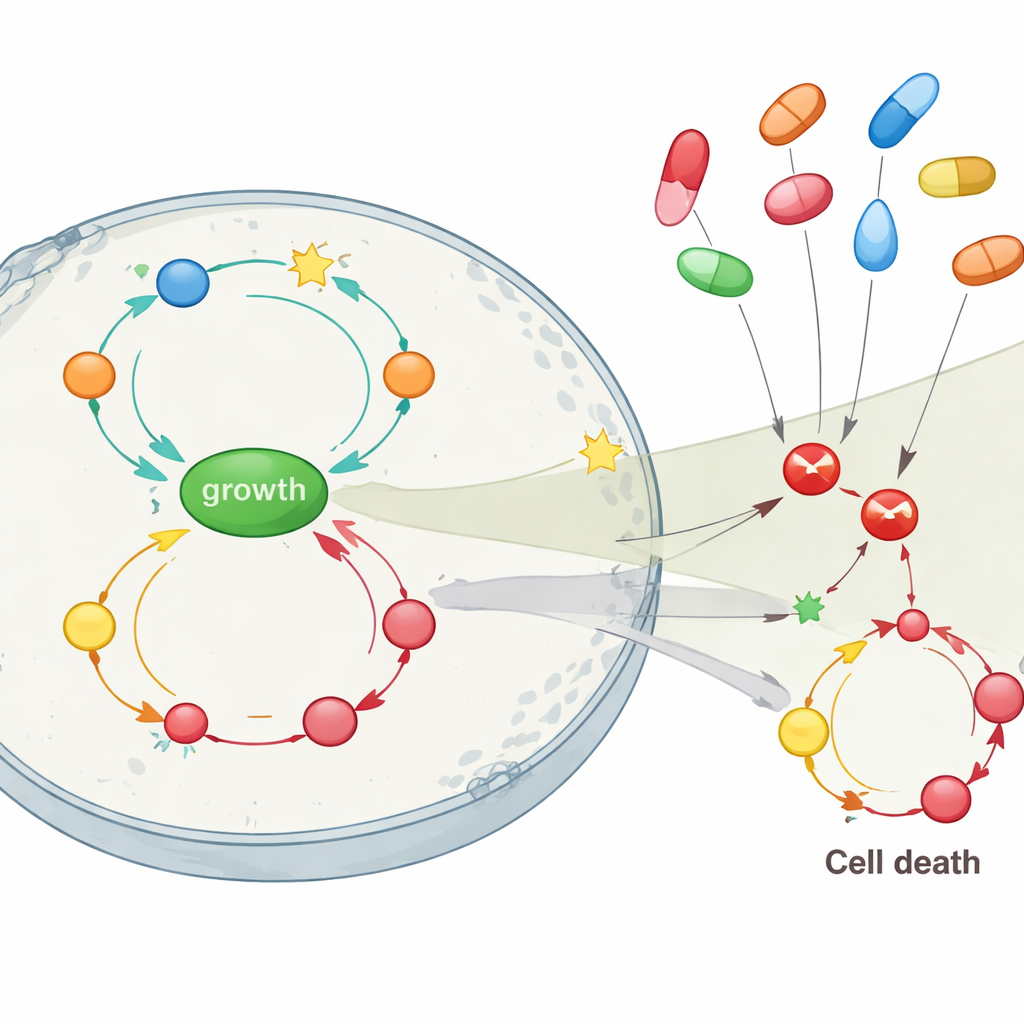
这对预防和治疗意味着什么
对非专业读者而言,关键讯息是 COX 抑制剂并非作为简单的单靶点药物对抗结肠癌而起作用。它们的有益效果,尤其在早期疾病中,可能在很大程度上依赖于对其他生长通路的附带作用。研究的模拟表明,这些药物在肿瘤积累大量突变之前——特别是在关键的 APC 守门员基因丧失但其他改变尚未完全激活生长回路时——最为强效。在更晚期的癌症中,单独阻断 COX2 很可能不足以奏效,注意力可能需要转向如 AKT 这样的通路。通过在计算机中映射这些复杂的反馈回路,这项工作支持更有针对性的策略:利用基因信息和炎症状态来决定谁可能受益于预防性 COX 抑制剂使用,以及何时可能需要针对网络中多个节点的组合策略。
引用: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
关键词: 结直肠癌, 炎症, COX 抑制剂, 信号网络, AKT 通路