Clear Sky Science · de
Netzwerkmodellierung sporadischen kolorektalen Krebses zeigt die Bedeutung von Off-Target-Effekten von Cyclooxygenase-Inhibitoren
Warum das für Darmgesundheit und Krebs wichtig ist
Kolorektaler Krebs gehört zu den weltweit häufigsten Krebserkrankungen, und viele Menschen nehmen bereits Schmerzmittel ein, die auf dieselben Signalwege wirken, die auch bei dieser Krankheit eine Rolle spielen. Die Studie stellt eine praktische Frage mit großen Folgen: Wenn sogenannte COX-Inhibitoren das Wachstum von Darmtumoren zu verlangsamen oder zu verhindern scheinen, liegt das dann wirklich an ihrer Hauptwirkung oder an anderen, „off-target“ Effekten in der Zelle? Durch den Aufbau eines detaillierten digitalen Modells von Darmzellen und ihrem entzündeten Umfeld untersuchen die Autoren, wann und wie diese Arzneien das Gleichgewicht tatsächlich vom unkontrollierten Wachstum zurück zu normalem Zellumsatz kippen können.
Ein dichtes Signalgewirr entwirren
Darmtumoren entstehen nicht durch ein einzelnes geschädigtes Gen, sondern durch ein vernetztes Geflecht aus Signalen zwischen Epithelzellen, Immunzellen und Entzündungsmediatoren. Die Forscher stellten ein großes Ein-/Aus-(Boolean-)Netzwerk zusammen, das 87 Schlüsselakteure innerhalb einer typischen Darmzelle und ihres nahen immunologischen Umfelds abbildet. Dazu gehören bekannte Wachstumsförderer, Bremsen des Zelltods und während der Entzündung freigesetzte Moleküle. Das virtuelle Netzwerk wurde tausende Male laufen gelassen, wobei verfolgt wurde, wie häufig der Knoten „Proliferation“ (Zellteilung) und der Knoten „Apoptose“ (programmierter Zelltod) eingeschaltet wurden. Mit diesem Ansatz konnten sie testen, wie unterschiedliche Bedingungen — etwa chronische Entzündung oder häufige, krebsassoziierte Genveränderungen — das Gesamtverhalten des Systems verschieben.
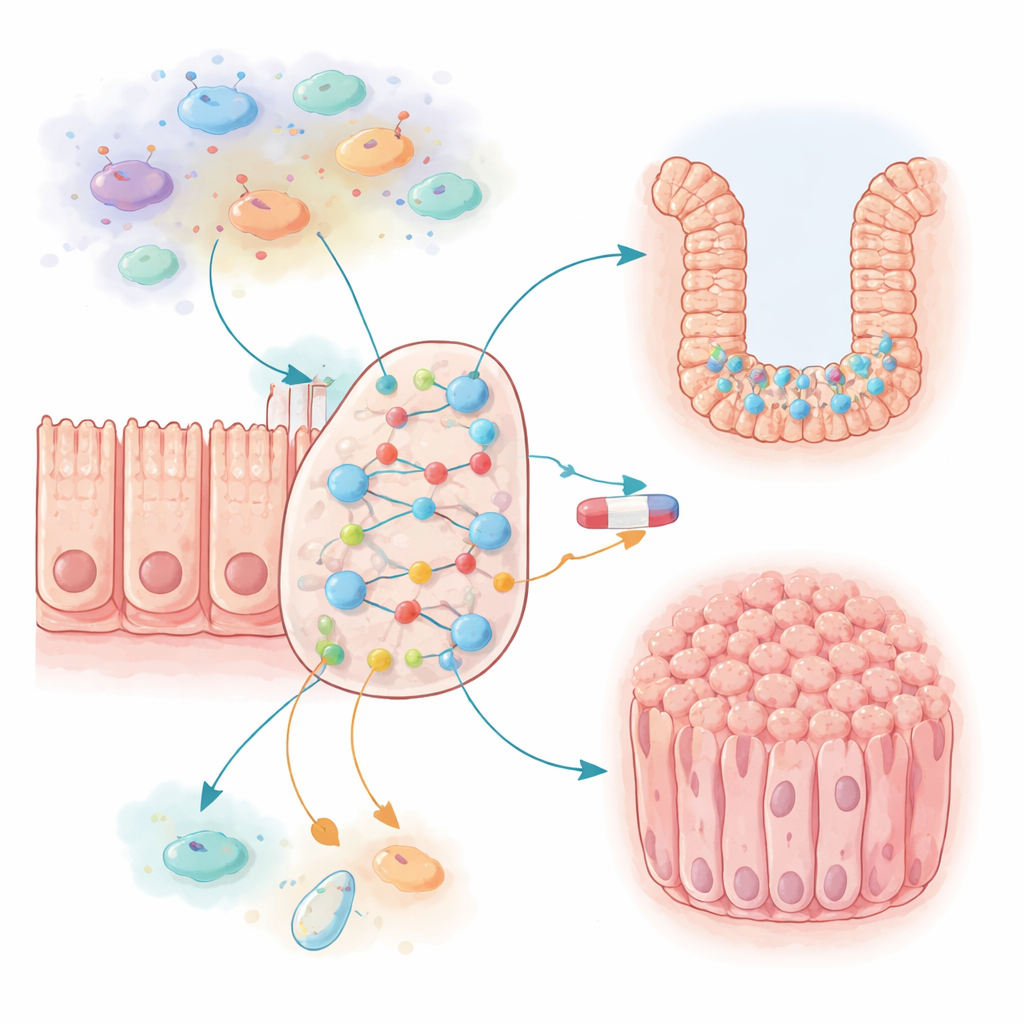
Wenn Entzündung Zellen in den Wachstumsmodus sperrt
Die erste Überraschung ergab sich, als das Team die entzündliche Umgebung im Modell aktivierte. Signale wie IL6 und CCL2, die von Immun- und Epithelzellen produziert werden, bildeten zwei sich verstärkende Rückkopplungsschleifen, die Wachstumswege stark förderten und den Zelltod unterdrückten. Wirken diese Signale mit voller Stärke, wurden Modell-Darmzellen nahezu endlos proliferativ und kaum tödlich zu machen — weit entfernt vom normalen Gewebezustand. Indem die Autoren die Wahrscheinlichkeit reduzierten, dass IL6 und CCL2 angeschaltet werden, fanden sie einen Bereich, in dem die Zellen eine niedrige, normale Wachstumsrate beibehielten, aber dennoch auf entzündliche Auslöser reagieren konnten. Anhaltende Aktivierung bestimmter Immunzellen erzeugte einen chronischen Zustand mit vermindertem Zelltod und leicht erhöhtem Wachstum, was nachahmt, wie langfristige Entzündungen die Darmschleimhaut anfälliger für Krebs machen können.
Wie häufige Genveränderungen Zellen über die Kante schieben
Als Nächstes führten die Forscher genetische Veränderungen ein, wie sie bei sporadischem kolorektalem Krebs häufig vorkommen — etwa Verlust des APC-„Torwächters“, aktivierende Veränderungen in RAS und Verlust des Wächtergens p53. Im Modell speisten all diese Veränderungen auf ihre Weise dieselben zwei positiven Rückkopplungsschleifen. Das Ergebnis war eine deutliche Verschiebung zugunsten von Überleben und Proliferation: Signale für den Zelltod sanken, während Wachstumssignale anstiegen. Demgegenüber veränderte der simulierte Verlust einer Chromosomenregion mit SMAD und DCC — Veränderungen, die in der Klinik mit schlechter Prognose assoziiert sind — Proliferation oder Apoptose im Modell kaum, was darauf hindeutet, dass die von diesen Genen gesteuerten Wege im Modell unterrepräsentiert sind und detaillierter abgebildet werden müssten, um die klinische Realität besser widerzuspiegeln.
Off-Target-Wirkungen entscheiden über Nutzen von Medikamenten
Im Mittelpunkt der Studie stand die Frage, wie das Blockieren verschiedener Medikamentenziele dieses Netzwerk beeinflusst — insbesondere Ziele, die von gängigen COX-Inhibitoren wie Celecoxib und Sulindac getroffen werden. Wenn das einzige Problem in der simulierten Zelle der APC-Verlust war, stellte die direkte Blockade von COX2 oder eines verwandten Enzyms (PDE5) das gesunde Gleichgewicht vollständig wieder her: Wachstum sank und Zelltod stieg über den Normalwert, wodurch die Rückkopplungsschleifen frühzeitig durchbrochen wurden. Mit zusätzlichen Mutationen in RAS und p53 — die mittlere und späte Tumorstadien repräsentieren — bewirkte das reine Blockieren von COX2 jedoch kaum etwas. In diesen späteren Szenarien war die Hemmung des wachstumsfördernden AKT-Wegs, oder in geringerem Maße von NF-κB, deutlich effektiver, die Proliferation zu verlangsamen, wenngleich sie den Zelltod nicht vollständig wiederherstellen konnte. Das Modell deutete außerdem an, dass Celecoxib, das neben COX2 auch AKT beeinflussen kann, Sulindac bei der Unterdrückung des Tumorwachstums überlegen sein dürfte, wenn mehrere Mutationen vorliegen.
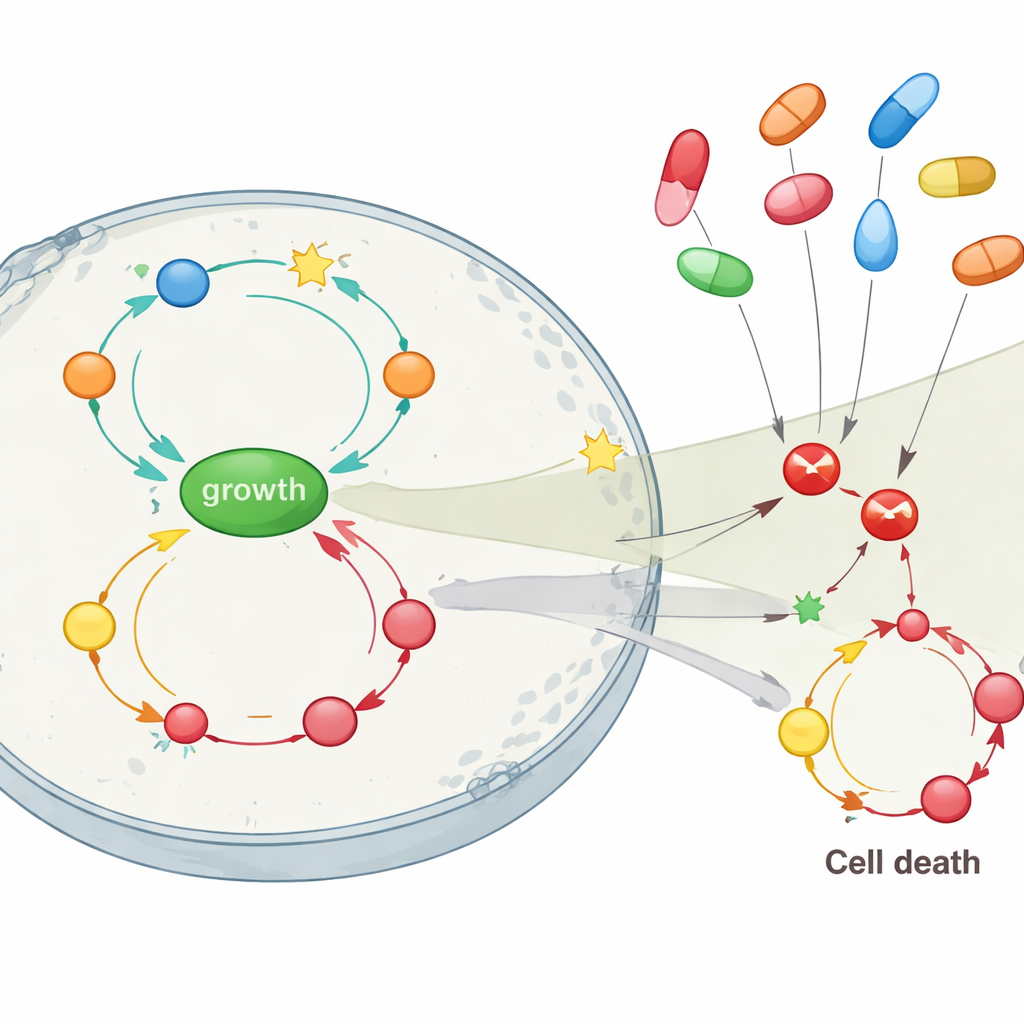
Was das für Prävention und Therapie bedeutet
Für Laien lautet die Kernbotschaft: COX-Inhibitoren wirken gegen Darmkrebs nicht als einfache, einzielige Medikamente. Ihre hilfreichen Effekte, besonders im Frühstadium, können stark von zusätzlichen Wirkungen gegen andere Wachstumswege abhängen. Die Simulationen der Studie legen nahe, dass diese Medikamente am wirksamsten sind, wenn sie vor der Akkumulation vieler Mutationen eingesetzt werden — insbesondere wenn das entscheidende APC-Torwächtersgen verloren ist, aber andere Veränderungen das Wachstumsnetz noch nicht vollständig aktiviert haben. Bei weiter fortgeschrittenen Tumoren ist die alleinige Blockade von COX2 wahrscheinlich nicht ausreichend, sodass der Fokus auf Wege wie AKT verlagert werden muss. Indem diese komplexen Rückkopplungskreise in silico kartiert werden, unterstützt die Arbeit einen stärker individualisierten Ansatz: genetische Informationen und Entzündungsstatus zu nutzen, um zu entscheiden, wer von einer präventiven COX-Inhibitor-Anwendung profitieren könnte und wann kombinierte Strategien nötig sind, die mehrere Knoten im Netzwerk ansprechen.
Zitation: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Schlüsselwörter: kolorektaler Krebs, Entzündung, COX-Inhibitoren, Signalnetzwerke, AKT-Signalweg