Clear Sky Science · tr
Sporadik kolon kanserinin ağ modellemesi, Siklooksijenaz inhibitörlerinin hedef dışı etkilerinin önemini ortaya koyuyor
Bağırsak sağlığı ve kanser açısından neden önemli
Kolorektal kanser dünya çapında en yaygın kanserlerden biridir ve birçok insan zaten bu hastalıkta rol oynayan aynı yolları etkileyen ağrı kesiciler kullanmaktadır. Bu çalışma, sonuçları büyük olan pratik bir soruyu ele alıyor: COX inhibitörü olarak adlandırılan ilaçlar bağırsak tümörlerini yavaşlatıyor veya önlüyor gibi göründüğünde, bunun gerçekten onların ana hedeflenen etkisinden mi kaynaklanıyor yoksa hücre içindeki diğer, "hedef dışı" etkiler mi rol oynuyor? Bağırsak hücreleri ve çevresindeki inflamatuar ortamın ayrıntılı dijital bir modelini kurarak, yazarlar bu ilaçların ne zaman ve nasıl kontrolsüz büyümeden normal hücre dengesine gerçekten müdahale edebileceğini araştırıyorlar.
Kalabalık bir sinyal manzarasını çözmek
Kolon tümörleri tek bir hasarlı genden doğmaz; bağırsak hücreleri, bağışıklık hücreleri ve inflamatuar moleküller arasındaki iç içe geçmiş sinyaller ağı sonucu ortaya çıkar. Araştırmacılar tipik bir bağırsak hücresi ve yakın bağışıklık ortamı içinde 87 kilit oyuncuyu yakalayan büyük bir açık/kapalı (Boolean) ağ kurdular. Bunlar iyi bilinen büyüme sürücüleri, hücre ölümünü frenleyen mekanizmalar ve inflamasyon sırasında salınan molekülleri içeriyor. Daha sonra bu sanal ağın binlerce kez çalışmasına izin verdiler ve "proliferasyon" düğümünün (hücre bölünmesi) ve "apoptoz" düğümünün (programlı hücre ölümü) ne sıklıkta açık sonlandığını izlediler. Bu yaklaşım, kronik inflamasyon veya kanserle ilişkili yaygın gen değişiklikleri gibi farklı koşulların sistemin genel davranışını nasıl kaydırdığını test etmelerini sağladı.
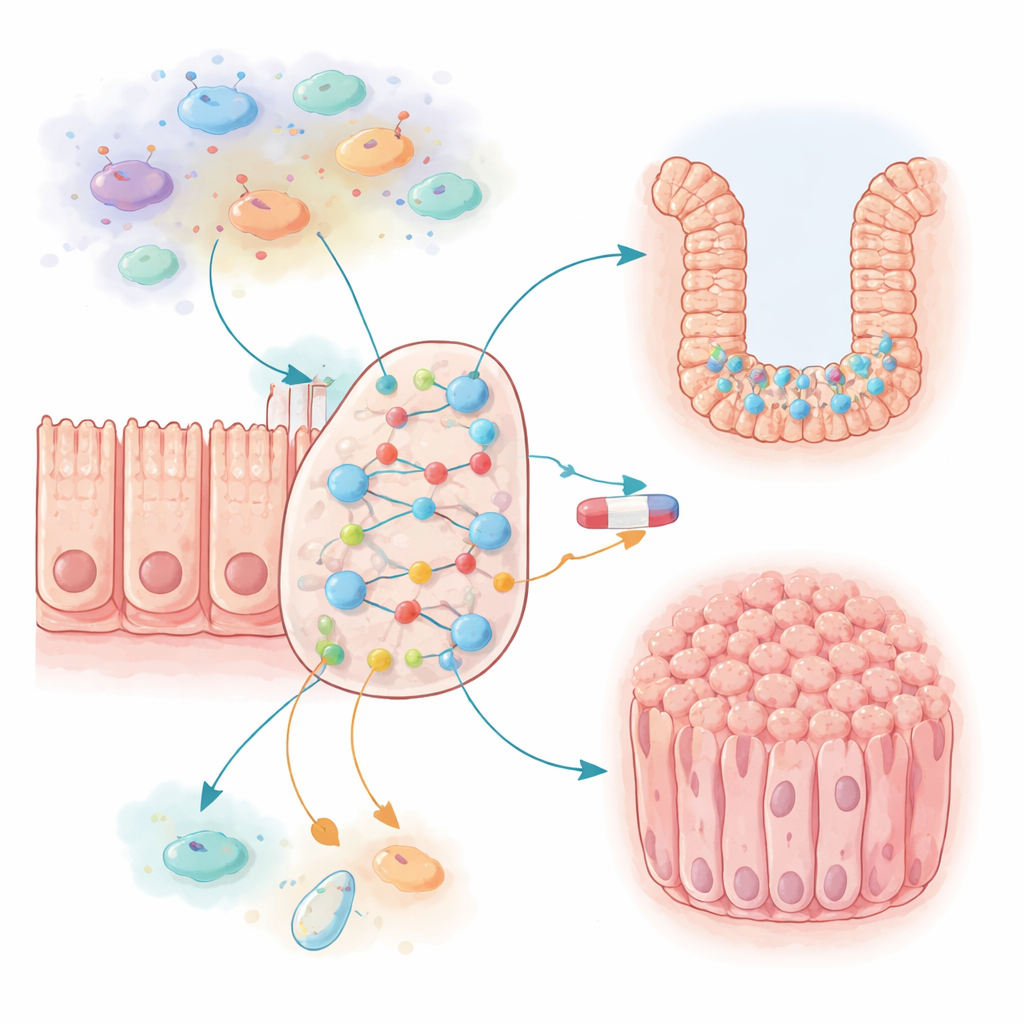
İnflamasyon hücreleri büyüme modunda kilitleyince
İlk şaşırtıcı bulgu, ekip modelde inflamatuar ortamı açtığında ortaya çıktı. Bağışıklık ve epitelyal hücreler tarafından üretilen IL6 ve CCL2 gibi sinyaller, büyüme yollarını güçlü şekilde destekleyen ve hücre ölümünü susturan iki pekiştirici geri besleme döngüsü oluşturdu. Bu sinyaller tam güçte etkin olmasına izin verilirse, modeldeki kolon hücreleri neredeyse sonsuz bir şekilde çoğalmaya ve neredeyse öldürülemez hale geldi—sağlıklı dokuda görülenin çok ötesinde. IL6 ve CCL2’nin açılma olasılığını düşürerek, yazarlar hücrelerin düşük, normal bir büyüme hızını korurken yine de inflamatuar tetikleyicilere yanıt verebildiği bir denge noktasını buldular. Belirli bağışıklık hücrelerinin sürekli aktivasyonu, hücre ölümünü azalttığı ve büyümeyi biraz artırdığı kronik bir durum üretti; bu da uzun süreli inflamasyonun bağırsak yüzeyini kansere karşı daha savunmasız hale getirebileceğini taklit ediyor.
Yaygın gen değişiklikleri hücreleri uçuruma nasıl iter
Sırada, araştırmacılar sporadik kolorektal kanserde sık görülen genetik değişiklikleri tanıttılar; örneğin APC “kapı bekçisi” geninin kaybı, RAS’ta aktive edici değişiklikler ve koruyucu gen p53’ün kaybı. Modelde bu değişikliklerin her biri kendi yoluyla aynı iki pozitif geri besleme döngüsüne katkıda bulundu. Sonuç, hayatta kalma ve proliferasyona doğru net bir kayış oldu: hücre ölümü sinyalleri düştü, büyüme sinyalleri arttı. Buna karşılık, SMAD ve DCC’yi içeren bir kromozom bölgesinin simüle edilmiş kaybı—gerçek hastalarda kötü prognozla ilişkilendirilen değişiklikler—modelde proliferasyon veya apoptozu neredeyse etkilemedi; bu da bu genlerin kontrol ettiği yolların modelde yeterince temsil edilmediğini ve klinik gerçeklikle uyumlu hale getirmek için daha ayrıntılı modellenmeleri gerekebileceğini öneriyor.
Hedef dışı etkiler ilacın yararını belirliyor
Çalışmanın özünü, farklı ilaç hedeflerinin bu ağı nasıl etkileyeceğini görmek oluşturuyordu; özellikle celecoxib ve sulindac gibi yaygın COX inhibitörlerinin hedeflediği noktalar üzerinde. Simüle edilen hücredeki tek sorun APC kaybı olduğunda, COX2’yi veya ilişkili bir enzimi (PDE5) doğrudan engellemek sağlıklı dengeyi tamamen geri getirdi: büyüme düştü ve hücre ölümü normalin üzerine çıktı, böylece geri besleme döngüleri erken kırıldı. Ancak RAS ve p53’te ek mutasyonlar eklendikçe—orta ve geç tümör aşamalarını temsil eden—sadece COX2’yi engellemek çok az etki yaptı. Bu ilerlemiş durumlarda, AKT merkezli büyüme yolunu veya daha az oranda NF-κB’yi inhibe etmek proliferasyonu yavaşlatmada çok daha etkiliydi, ancak yine de hücre ölümünü tamamen geri döndüremiyordu. Model ayrıca, COX2’nin yanı sıra AKT’yi de hedefleyebilen celecoxib’in, birden çok mutasyon varlığında tümör hücresi büyümesini dizginlemede sulindac’dan daha iyi performans göstermesi gerektiğini öne sürdü.
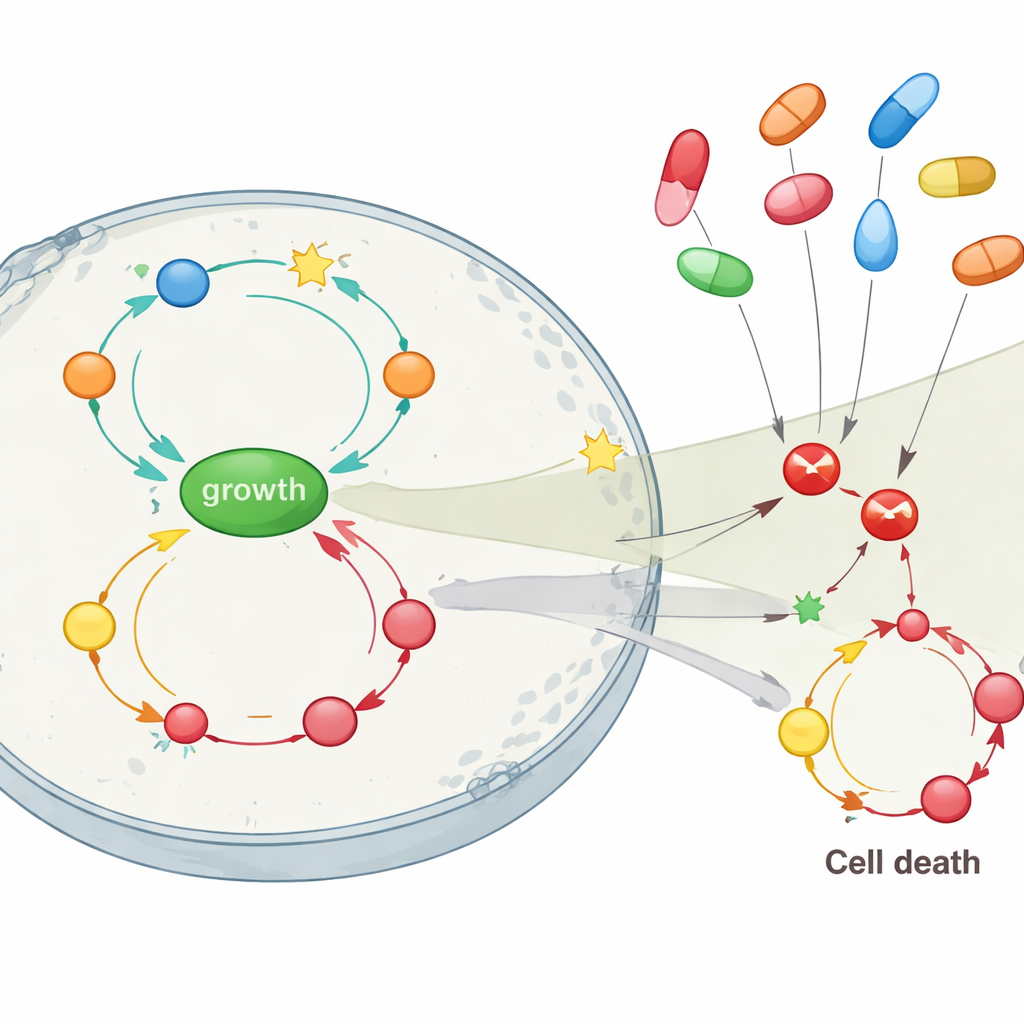
Koruma ve tedavi için anlamı
Halk için ana mesaj, COX inhibitörlerinin kolon kanserine karşı basit, tek hedefli ilaçlar olmadığıdır. Özellikle erken hastalıkta sağladıkları faydalar, büyük ölçüde diğer büyüme yollarına karşı ek etkilerine dayanıyor olabilir. Çalışmanın simülasyonları, bu ilaçların en etkili olduğu zamanın tümörler çok sayıda mutasyon biriktirmeden önce olduğu—özellikle kritik APC kapı bekçi geni kaybedildiğinde ancak diğer değişiklikler büyüme devrelerini tamamen açmamışken—önerisini destekliyor. Daha ileri kanserlerde yalnızca COX2 bloke etmek muhtemelen yeterli olmayacak ve dikkat AKT gibi yollara kaydırılabilir. Bu karmaşık geri besleme döngülerini in silico haritalandırarak, çalışma daha hedefe yönelik bir yaklaşımı destekliyor: kimlerin koruyucu COX inhibitörü kullanımından fayda sağlayabileceğini ve ne zaman ağdaki birden çok düğümü hedefleyen kombinasyon stratejilerine ihtiyaç duyulabileceğini belirlemek için genetik bilgi ve inflamasyon durumunun kullanılmasını öneriyor.
Atıf: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Anahtar kelimeler: kolorektal kanser, iltihap, COX inhibitörleri, sinyal ağları, AKT yolu