Clear Sky Science · es
Modelado de redes del cáncer colorrectal esporádico revela la importancia de los efectos fuera de objetivo de los inhibidores de ciclooxigenasa
Por qué importa para la salud intestinal y el cáncer
El cáncer colorrectal es uno de los cánceres más comunes en todo el mundo, y muchas personas ya toman analgésicos que afectan las mismas vías implicadas en esta enfermedad. Este estudio plantea una pregunta práctica con grandes implicaciones: cuando fármacos llamados inhibidores de COX parecen ralentizar o prevenir tumores intestinales, ¿es realmente por su acción principal prevista o por otros efectos “fuera de objetivo” dentro de las células? Al construir un modelo digital detallado de células del colon y su entorno inflamado, los autores exploran cuándo y cómo estos fármacos pueden inclinar genuinamente la balanza desde un crecimiento descontrolado de vuelta a la renovación celular normal.
Desentrañando un paisaje de señales congestionado
Los tumores de colon no surgen de un único gen dañado, sino de una maraña de señales entre células intestinales, células inmunitarias y moléculas inflamatorias. Los investigadores montaron una gran red binaria (Boolean) que captura 87 actores clave dentro de una célula intestinal típica y su entorno inmunitario cercano. Éstos incluyen impulsores de crecimiento bien conocidos, frenos de la muerte celular y moléculas liberadas durante la inflamación. Luego dejaron que esta red virtual funcionara miles de veces, registrando con qué frecuencia el nodo “proliferación” (división celular) y el nodo “apoptosis” (muerte celular programada) terminaban activados. Este enfoque les permitió probar cómo diferentes condiciones —como inflamación crónica o cambios genéticos vinculados al cáncer— desplazan el comportamiento general del sistema.
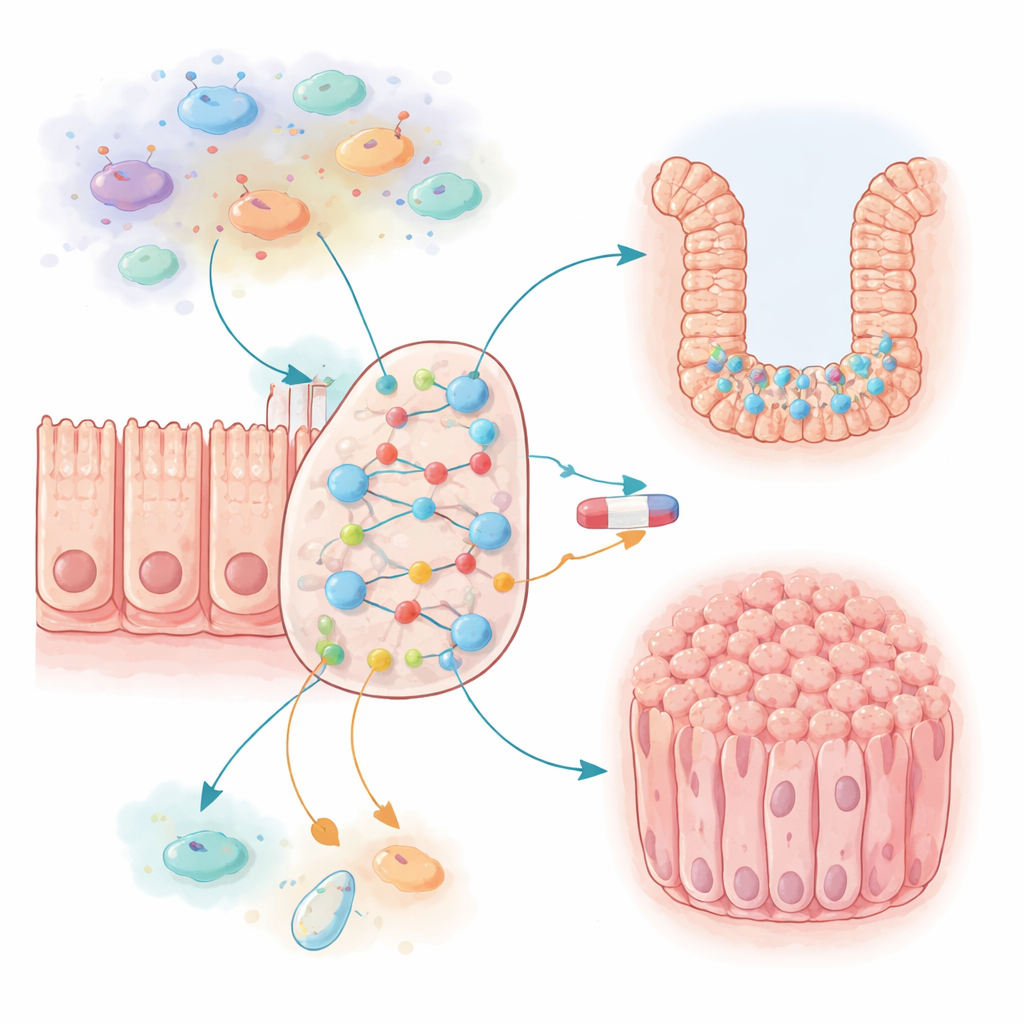
Cuando la inflamación atrapa a las células en modo crecimiento
La primera sorpresa llegó cuando el equipo activó el entorno inflamatorio en su modelo. Señales como IL6 y CCL2, producidas por células inmunitarias y epiteliales, formaron dos bucles de retroalimentación que se reforzaban entre sí, potenciando fuertemente las vías de crecimiento y apagando la muerte celular. Si estas señales actuaban a máxima intensidad, las células modelo del colon se volvían casi infinitamente proliferativas y casi imposibles de matar —muy distinto de lo que se observa en tejido sano. Al reducir la probabilidad de que IL6 y CCL2 se activaran, los autores encontraron un punto intermedio donde las células mantenían una tasa de crecimiento baja y normal pero aún podían responder a desencadenantes inflamatorios. La activación persistente de ciertas células inmunitarias produjo un estado crónico que redujo la muerte celular y aumentó ligeramente el crecimiento, emulando cómo la inflamación prolongada puede hacer que el revestimiento intestinal sea más vulnerable al cáncer.
Cómo los cambios genéticos comunes llevan a las células al límite
A continuación, los investigadores introdujeron alteraciones genéticas que se ven a menudo en el cáncer colorrectal esporádico, como la pérdida del gen “guardián” APC, cambios activadores en RAS y la pérdida del gen guardián p53. En el modelo, cada uno de estos cambios, a su manera, alimentó los mismos dos bucles de retroalimentación positiva. El resultado fue un claro desplazamiento hacia la supervivencia y la proliferación: las señales de muerte celular cayeron, mientras que las señales de crecimiento se dispararon. En contraste, la simulada pérdida de una región cromosómica que contiene SMAD y DCC —alteraciones asociadas a mal pronóstico en pacientes reales— apenas cambió la proliferación o la apoptosis en el modelo, lo que sugiere que las vías controladas por estos genes estaban subrepresentadas y podrían necesitar modelarse con más detalle para ajustarse a la realidad clínica.
Los efectos fuera de objetivo marcan la diferencia del beneficio farmacológico
El núcleo del estudio consistió en ver cómo bloquear distintos objetivos farmacológicos afectaría a esta red, especialmente dianas golpeadas por inhibidores comunes de COX como celecoxib y sulindac. Cuando el único problema en la célula simulada era la pérdida de APC, bloquear directamente COX2 o una enzima relacionada (PDE5) restauró totalmente un equilibrio saludable: el crecimiento disminuyó y la muerte celular aumentó por encima de lo normal, rompiendo los bucles de retroalimentación en etapas tempranas. Pero a medida que se añadían mutaciones adicionales en RAS y p53 —representando estadios tumorales intermedios y tardíos— el simple bloqueo de COX2 tuvo poco efecto. En esos escenarios avanzados, inhibir la vía de crecimiento centrada en AKT, o en menor medida NF-κB, fue mucho más eficaz para frenar la proliferación, aunque aún no logró restaurar completamente la muerte celular. El modelo también sugirió que el celecoxib, que puede afectar a AKT además de COX2, debería rendir mejor que el sulindac para contener el crecimiento de células tumorales cuando están presentes múltiples mutaciones.
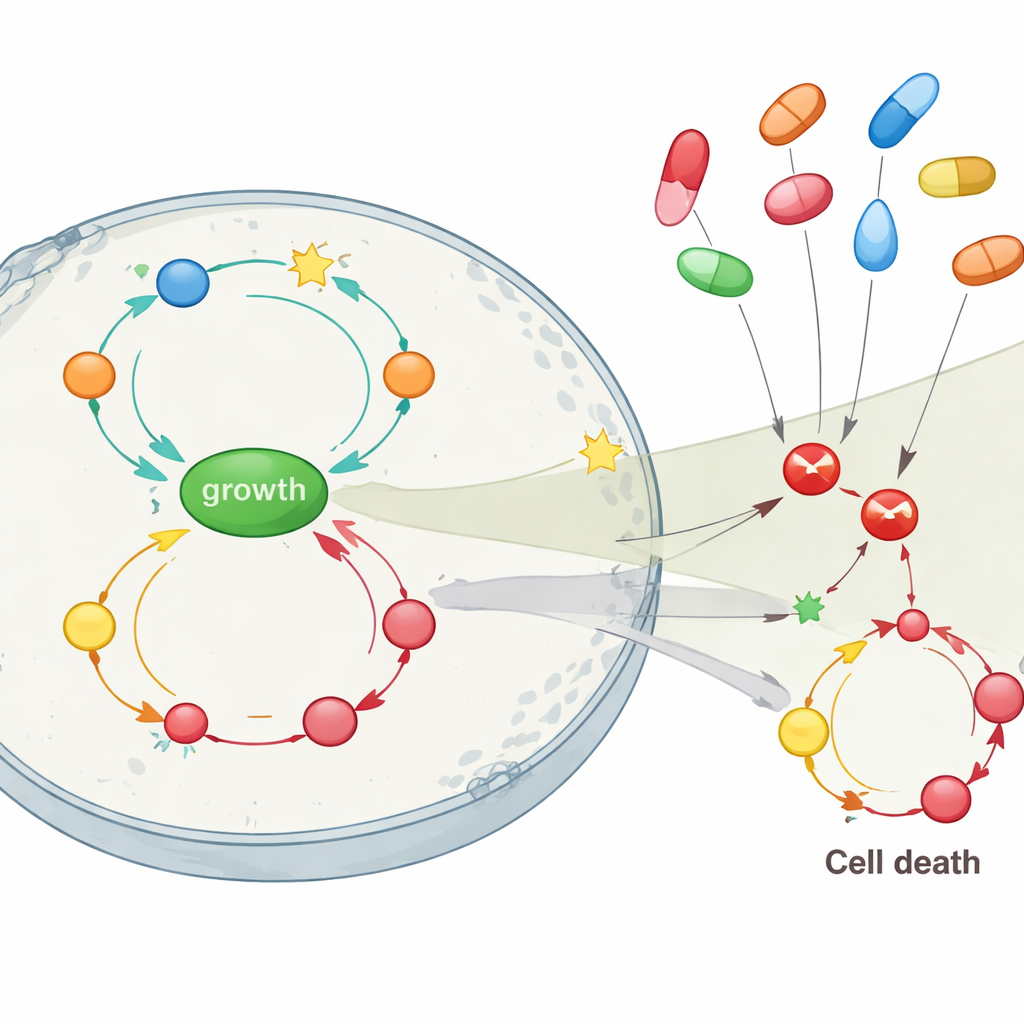
Qué significa esto para la prevención y el tratamiento
Para un lector no especialista, el mensaje clave es que los inhibidores de COX no actúan como fármacos simples de diana única contra el cáncer de colon. Sus efectos beneficiosos, especialmente en la enfermedad temprana, pueden depender en gran medida de acciones adicionales contra otras vías de crecimiento. Las simulaciones del estudio sugieren que estos fármacos son más potentes cuando se usan antes de que los tumores acumulen muchas mutaciones —particularmente cuando se ha perdido el crucial gen guardián APC pero otros cambios aún no han activado completamente los circuitos de crecimiento. En cánceres más avanzados, bloquear solo COX2 probablemente no sea suficiente, y la atención podría desplazarse hacia vías como AKT. Al cartografiar estos complejos bucles de retroalimentación in silico, el trabajo respalda un enfoque más personalizado: usar información genética y el estado inflamatorio para decidir quién podría beneficiarse del uso preventivo de inhibidores de COX y cuándo pueden ser necesarias estrategias combinadas que apunten a múltiples nodos de la red.
Cita: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Palabras clave: cáncer colorrectal, inflamación, inhibidores de COX, redes de señalización, vía AKT