Clear Sky Science · pl
Modelowanie sieciowe sporadycznego raka okrężnicy ujawnia znaczenie efektów pozaprzeznaczeniowych inhibitorów cyklooksygenazy
Dlaczego to ważne dla zdrowia jelit i raka
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie, a wiele osób już przyjmuje leki przeciwbólowe wpływające na te same szlaki zaangażowane w tę chorobę. Badanie stawia praktyczne pytanie o dalekosiężnych implikacjach: gdy leki zwane inhibitorami COX wydają się hamować lub zapobiegać nowotworom jelita, czy rzeczywiście dzieje się tak za sprawą ich głównego zamierzonego działania, czy raczej z powodu innych, „pozaprzeznaczeniowych” efektów wewnątrzkomórkowych? Budując szczegółowy cyfrowy model komórek okrężnicy i ich zapalnego otoczenia, autorzy badają, kiedy i jak te leki mogą rzeczywiście przechylić równowagę z niekontrolowanego wzrostu z powrotem ku normalnej wymianie komórkowej.
Rozplątywanie zatłoczonego krajobrazu sygnałowego
Nowotwory jelita grubego nie powstają wskutek pojedynczego uszkodzonego genu, lecz z uwikłanej sieci sygnałów między komórkami jelitowymi, komórkami układu odpornościowego i cząsteczkami zapalnymi. Badacze złożyli dużą sieć binarną (Boolean), obejmującą 87 kluczowych graczy w obrębie typowej komórki jelitowej i jej pobliskiego środowiska immunologicznego. Wśród nich znalazły się dobrze znane czynniki napędzające wzrost, hamulce śmierci komórkowej oraz molekuły uwalniane podczas zapalenia. Następnie pozwolili tej wirtualnej sieci działać tysiące razy, śledząc, jak często węzeł „proliferacja” (podział komórkowy) i węzeł „apoptoza” (programowana śmierć komórki) kończyły w stanie włączonym. To podejście pozwoliło im przetestować, jak różne warunki — takie jak przewlekłe zapalenie czy powszechne zmiany genetyczne związane z rakiem — przesuwają ogólne zachowanie systemu.
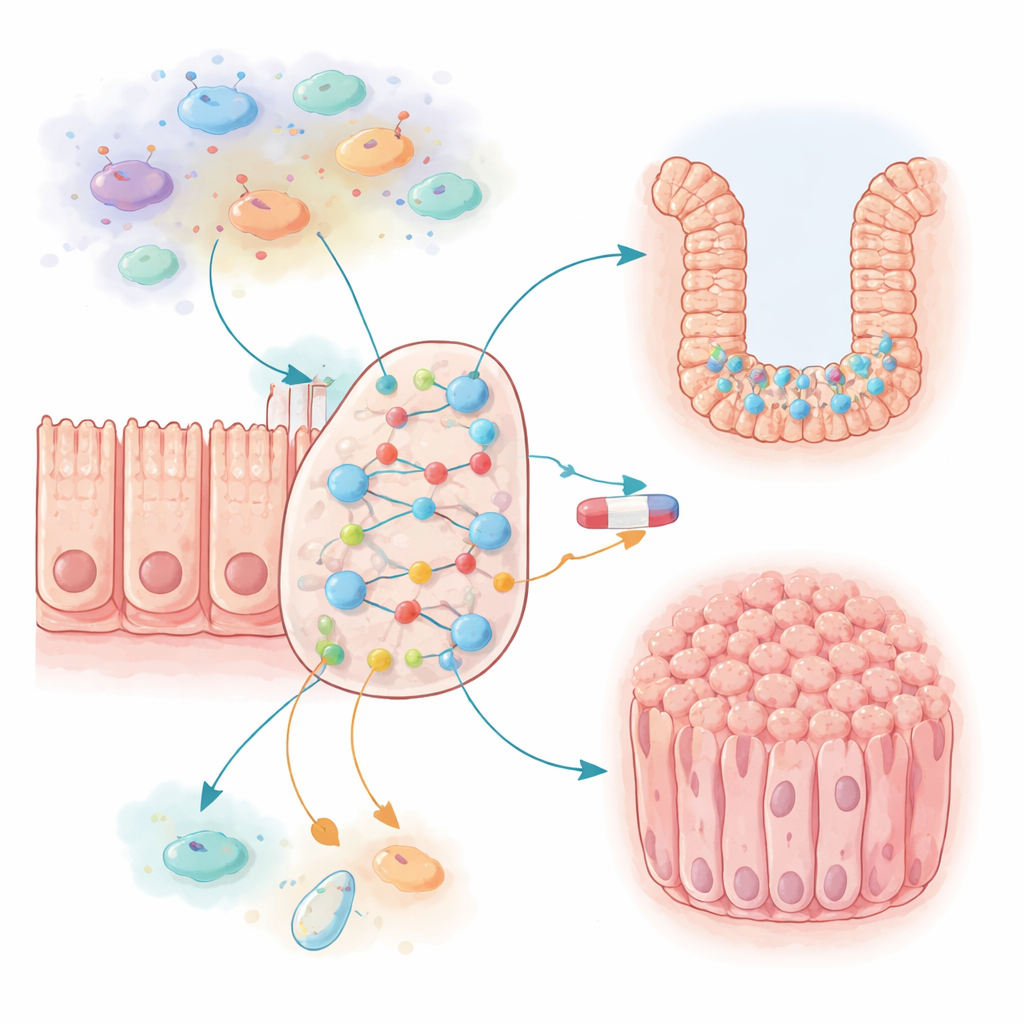
Gdy zapalenie blokuje komórki w trybie wzrostu
Pierwsze zaskoczenie pojawiło się, gdy zespół włączył w modelu środowisko zapalne. Sygnały takie jak IL6 i CCL2, wytwarzane przez komórki odpornościowe i nabłonkowe, utworzyły dwa wzajemnie wzmacniające się sprzężenia zwrotne, które silnie pobudzały szlaki wzrostu i wyłączały śmierć komórkową. Jeśli te sygnały działały pełną siłą, modelowe komórki okrężnicy stały się niemal nieograniczenie proliferujące i niemal niemożliwe do zabicia — dalekie od stanu zdrowej tkanki. Ograniczając prawdopodobieństwo, że IL6 i CCL2 się włączą, autorzy znaleźli punkt, w którym komórki utrzymywały niski, normalny poziom wzrostu, ale wciąż mogły reagować na bodźce zapalne. Utrzymująca się aktywacja niektórych komórek odpornościowych wygenerowała przewlekły stan, który obniżał śmierć komórkową i nieco podnosił proliferację, naśladując to, jak długotrwałe zapalenie może uczynić wyściółkę jelita bardziej podatną na raka.
Jak powszechne zmiany genetyczne popychają komórki za krawędź
Następnie badacze wprowadzili zmiany genetyczne często obserwowane w sporadycznym raku jelita grubego, takie jak utrata „strażnika” APC, zmiany aktywujące RAS oraz utrata genu strażniczego p53. W modelu każda z tych zmian, na swój sposób, włączała te same dwa dodatnie sprzężenia zwrotne. Skutkiem był wyraźny przesuw w kierunku przeżycia i proliferacji: sygnały śmierci komórkowej spadły, podczas gdy sygnały wzrostu gwałtownie wzrosły. Dla porównania, symulowana utrata regionu chromosomu zawierającego SMAD i DCC — zmiany powiązane z gorszym rokowaniem u pacjentów — ledwie zmieniła proliferację czy apoptozę w modelu, co sugeruje, że szlaki kontrolowane przez te geny były w modelu niedostatecznie reprezentowane i mogą wymagać bardziej szczegółowego odwzorowania, aby odpowiadać rzeczywistości klinicznej.
Działania pozaprzeznaczeniowe decydują o korzyści leku
Rdzeń badania polegał na sprawdzeniu, jak blokowanie różnych celów lekowych wpłynie na tę sieć, w szczególności celów trafianych przez powszechne inhibitory COX, takie jak celekoksyb i sulindak. Gdy jedynym problemem w symulowanej komórce była utrata APC, bezpośrednie blokowanie COX2 lub pokrewnego enzymu (PDE5) w pełni przywracało zdrową równowagę: proliferacja spadała, a śmierć komórkowa wzrastała powyżej normy, przerywając sprzężenia zwrotne na wczesnym etapie. Jednak w miarę nakładania się dodatkowych mutacji w RAS i p53 — odpowiadających stadium pośredniemu i zaawansowanemu guza — samo blokowanie COX2 miało niewielki efekt. W tych późniejszych ustawieniach hamowanie szlaku wzrostu skoncentrowanego na AKT, lub w mniejszym stopniu NF-κB, było znacznie skuteczniejsze w spowalnianiu proliferacji, chociaż nadal nie przywracało w pełni śmierci komórkowej. Model zasugerował także, że celekoksyb, który może oddziaływać na AKT jak i COX2, powinien przewyższać sulindak w powstrzymywaniu wzrostu komórek nowotworowych, gdy obecnych jest wiele mutacji.
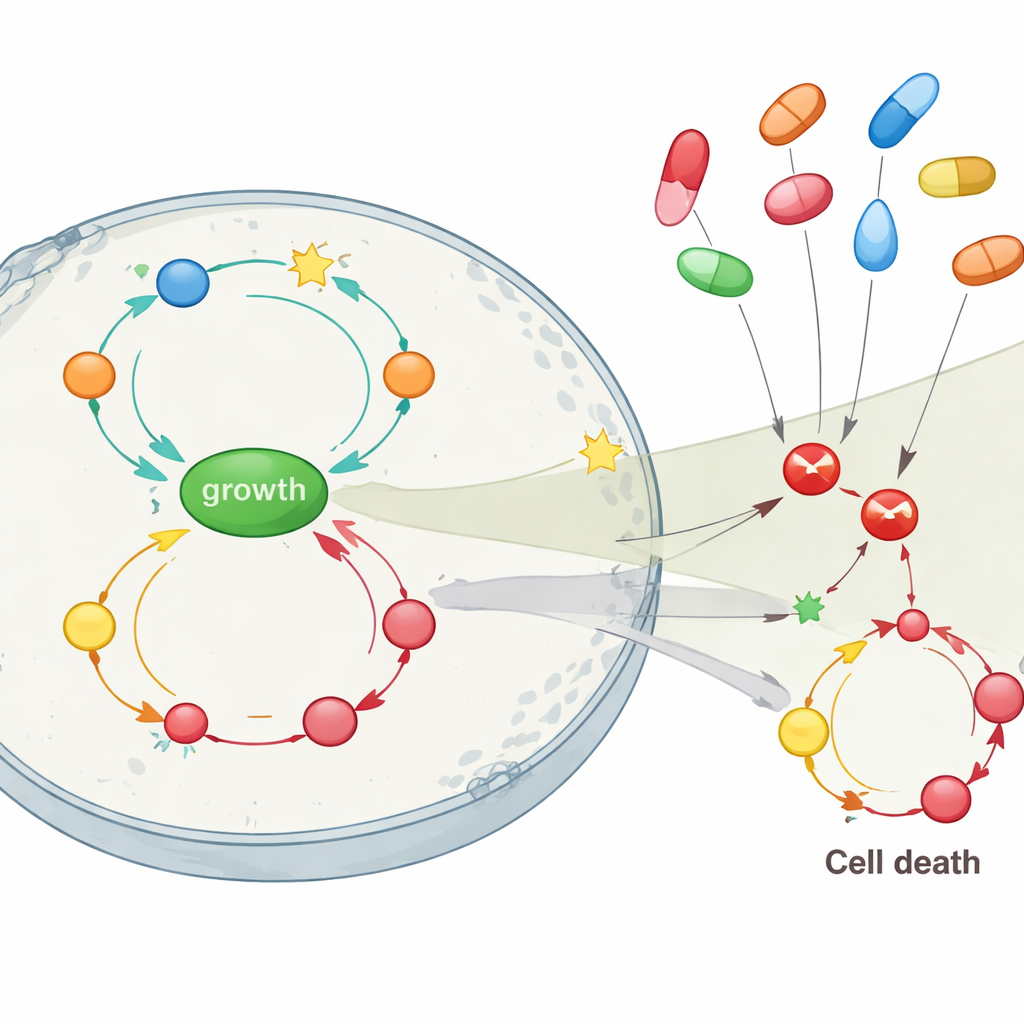
Co to oznacza dla zapobiegania i leczenia
Dla laika kluczowy przekaz jest taki, że inhibitory COX nie działają jako proste leki jednosesyjne przeciw rakowi jelita. Ich korzystne efekty, szczególnie we wczesnej chorobie, mogą w dużej mierze opierać się na dodatkowych działaniach przeciw innym szlakom wzrostu. Symulacje z badania sugerują, że te leki są najskuteczniejsze, gdy stosuje się je zanim guzy zgromadzą wiele mutacji — szczególnie gdy kluczowy gen strażniczy APC jest utracony, ale inne zmiany nie zablokowały jeszcze w pełni obwodów wzrostu. W bardziej zaawansowanych nowotworach samo blokowanie COX2 prawdopodobnie nie wystarczy, a uwaga może być skierowana na ścieżki takie jak AKT. Mapując te złożone sprzężenia zwrotne in silico, praca wspiera bardziej spersonalizowane podejście: wykorzystanie informacji genetycznych i statusu zapalnego do decydowania, kto może skorzystać z prewencyjnego stosowania inhibitorów COX oraz kiedy mogą być potrzebne strategie łączone ukierunkowane na wiele węzłów sieci.
Cytowanie: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Słowa kluczowe: rak jelita grubego, zapalenie, inhibitory COX, sieci sygnałowe, ścieżka AKT