Clear Sky Science · ar
نمذجة الشبكات لسرطان القولون المستقطع تكشف أهمية التأثيرات خارج الهدف لمثبطات السيكلوأكسجيناز
لماذا يهم هذا لصحة الأمعاء والسرطان
يُعد سرطان القولون والمستقيم من أكثر أنواع السرطان شيوعًا في العالم، ويتناول الكثير من الناس بالفعل مسكنات تؤثر على نفس المسارات المشاركة في هذا المرض. يطرح هذا البحث سؤالًا عمليًا ذو تداعيات كبيرة: عندما تبدو أدوية تُعرف بمثبطات COX أنها تبطئ أو تمنع أورام الأمعاء، هل يعود ذلك فعلاً إلى فعلها المقصود الرئيسي، أم إلى تأثيرات أخرى «خارج الهدف» داخل الخلايا؟ من خلال بناء نموذج رقمي مفصّل لخلايا القولون وبيئتها الملتهبة المحيطة، يستكشف المؤلفون متى وكيف يمكن لهذه الأدوية أن تُرجح الميزان فعليًا من النمو السريع إلى دوران خلوي طبيعي.
فك تشابك مشهد إشارات مزدحم
لا تنشأ أورام القولون من جين واحد تالف بل من شبكة معقّدة من الإشارات بين خلايا الأمعاء والخلايا المناعية والجزيئات الالتهابية. جمع الباحثون شبكة كبيرة منطقية (بوليانية) تمثل 87 عنصرًا رئيسيًا داخل خلية معوية نموذجية وبيئتها المناعية القريبة. تشمل هذه العناصر سائقات النمو المعروفة، ومكابح موت الخلايا، وجزيئات تُفرز أثناء الالتهاب. سمحوا بعد ذلك لهذه الشبكة الافتراضية بالعمل آلاف المرات، متتبعين كم مرة انتهى الأمر بعقدة «الانقسام» (التكاثر الخلوي) وعقدة «الاستماتة» (موت الخلايا المبرمج) إلى حالة التشغيل. مكنهم هذا النهج من اختبار كيف تحوّل ظروف مختلفة—مثل الالتهاب المزمن أو التغيرات الوراثية الشائعة المرتبطة بالسرطان—سلوك النظام ككل.
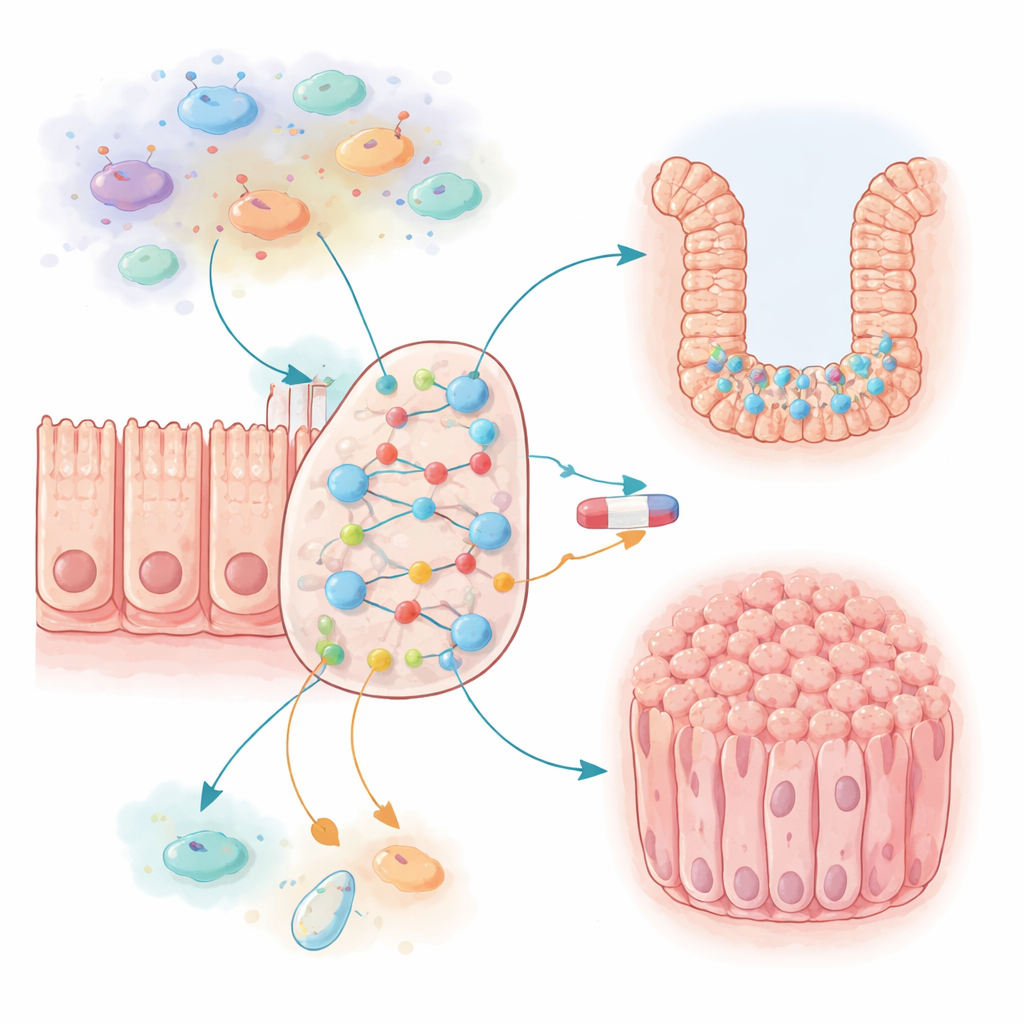
عندما يقفل الالتهاب الخلايا في وضع النمو
جاءت المفاجأة الأولى عندما فعّل الفريق البيئة الالتهابية في نموذجهم. تكونت إشارات مثل IL6 وCCL2، التي تُنتجها الخلايا المناعية والظهارية، على شكل حلقتي تغذية راجعة معزّزتين عززتا بشدة مسارات النمو وأغلقتا موت الخلايا. إذا سُمح لهذه الإشارات أن تعمل بكامل قوتها، أصبحت خلايا القولون النموذجية متكاثرة تقريبًا إلى ما لا نهاية ومن الصعب جدًا القضاء عليها—بعيدًا عن ما يُرى في الأنسجة السليمة. عبر تخفيف احتمال تشغيل IL6 وCCL2، وجد المؤلفون نقطة توازن حيث حافظت الخلايا على معدل نمو منخفض وطبيعي لكنها ظلت قادرة على الاستجابة لمحفزات الالتهاب. أدى التنشيط المستمر لبعض الخلايا المناعية إلى حالة مزمنة خفّضت موت الخلايا ورفعت النمو قليلًا، مقلّدةً كيف يمكن للالتهاب طويل الأمد أن يجعل بطانة الأمعاء أكثر عرضة للسرطان.
كيف تدفع التغيرات الجينية الشائعة الخلايا إلى الانهيار
بعد ذلك، أدخل الباحثون تغيرات جينية تُرى غالبًا في سرطان القولون العابر، مثل فقدان جين الحارس APC، وتغيرات منشِّطة في RAS، وفقدان الجين الحارس p53. في النموذج، غذّت كل واحدة من هذه التغيرات، بطريقتها الخاصة، نفس حلقتي التغذية الراجعة الإيجابية. وكانت النتيجة تحولًا واضحًا نحو البقاء والتكاثر: انخفضت إشارات موت الخلايا، بينما ارتفعت إشارات النمو. بالمقابل، لم يُحدث المحاكاة لفقدان منطقة كروموسومية تحتوي SMAD وDCC—تغييرات مرتبطة بسوء النتيجة لدى المرضى الحقيقيين—تغيرًا يُذكر في التكاثر أو الاستماتة في النموذج، مما يوحي بأن المسارات التي تتحكم بها هذه الجينات كانت ممثلة بشكل ناقص وقد تحتاج إلى نمذجة أكثر تفصيلًا لمطابقة الواقع السريري.
التأثيرات خارج الهدف تُحدّد فائدة الدواء
كان جوهر الدراسة هو مشاهدة كيف سيؤثر حجب أهداف دوائية مختلفة على هذه الشبكة، خاصة الأهداف التي تستهدفها مثبطات COX الشائعة مثل سيليكوكسِب وسولينداك. عندما كانت المشكلة الوحيدة في الخلية المحاكاة هي فقدان APC، أدى الحجب المباشر لـ COX2 أو إنزيم ذو صلة (PDE5) إلى استعادة توازن صحي تمامًا: انخفض النمو وارتفع معدل موت الخلايا فوق الطبيعي، ومعاكسًا حلقات التغذية الراجعة في مراحل مبكرة. لكن مع تراكب طفرات إضافية في RAS وp53—ممثلًا المراحل الوسطى والمتأخرة للورم—لم يفعل حجب COX2 وحده الكثير. في تلك المراحل اللاحقة، كان تثبيط مسار النمو المتمركز حول AKT، أو بدرجة أقل NF-κB، أكثر فاعلية بكثير في إبطاء التكاثر، رغم أنه لم يتمكن من إحياء موت الخلايا بالكامل. كما اقترح النموذج أن سيليكوكسِب، الذي يمكن أن يؤثر على AKT بالإضافة إلى COX2، قد يتفوق على سولينداك في كبح نمو خلايا الورم عندما تكون طفرات متعددة موجودة.
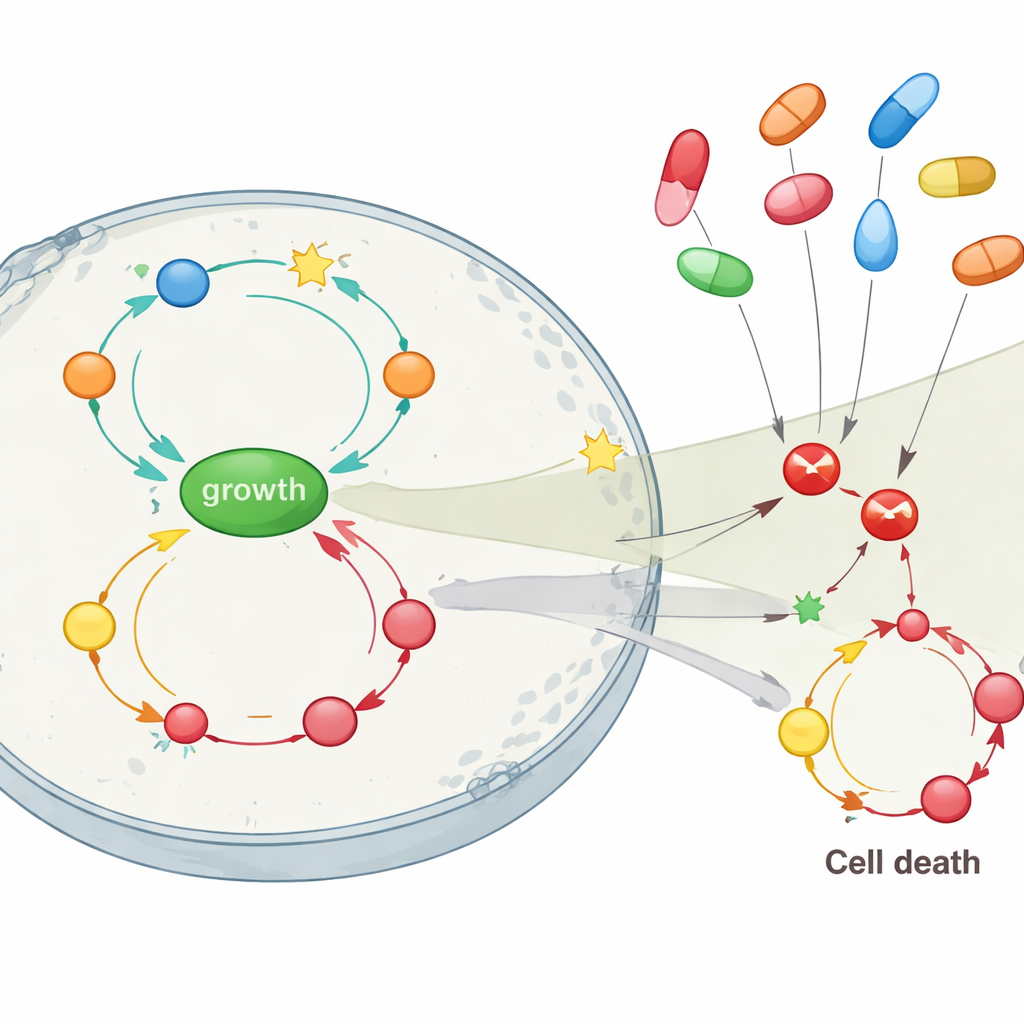
ما الذي يعنيه هذا للوقاية والعلاج
بالنسبة للقارئ العادي، الرسالة الأساسية هي أن مثبطات COX ليست أدوية بسيطة ذات هدف واحد ضد سرطان القولون. قد تعتمد فوائدها، وخصوصًا في المراحل المبكرة من المرض، اعتمادًا كبيرًا على أعمال إضافية ضد مسارات نمو أخرى. تشير محاكاة الدراسة إلى أن هذه الأدوية تكون أقوى عندما تُستخدم قبل أن تتراكم لدى الأورام العديد من الطفرات—لا سيما عندما يُفقد جين البوابة الحاسم APC ولكن لم تُؤمَّن الدوائر النمائية الأخرى بالكامل بعد. في السرطانات الأكثر تقدمًا، من غير المرجح أن يكون حجب COX2 بمفرده كافيًا، وقد يتطلب الأمر تحويل الانتباه نحو مسارات مثل AKT. من خلال رسم هذه الحلقات الراجعة المعقدة رقميًا، يدعم العمل نهجًا أكثر تفصيلًا: استخدام المعلومات الجينية وحالة الالتهاب لتقرير من قد يستفيد من استخدام مثبطات COX الوقائية، ومتى قد تكون الاستراتيجيات التركيبية التي تستهدف عدة عقد في الشبكة مطلوبة.
الاستشهاد: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
الكلمات المفتاحية: سرطان القولون والمستقيم, الالتهاب, مثبطات COX, شبكات الإشارات, مسار AKT