Clear Sky Science · ru
Сетевое моделирование спорадического колоректального рака показывает важность побочных эффектов ингибиторов циклооксигеназы
Почему это важно для здоровья кишечника и рака
Колоректальный рак — одно из самых распространённых злокачественных заболеваний в мире, и многие люди уже принимают обезболивающие, затрагивающие те же пути, которые участвуют в этом заболевании. В этом исследовании поставлен прагматичный вопрос с существенными последствиями: когда препараты из группы ингибиторов ЦОГ, по-видимому, замедляют или предотвращают образование опухолей в кишечнике, действительно ли это происходит за счёт их основного целевого действия или из-за других, «внецелевых» эффектов внутри клетки? Создав детальную цифровую модель клеток толстой кишки и их воспалённого окружения, авторы исследуют, когда и как эти препараты могут действительно сместить баланс от неконтролируемого роста обратно к нормальному клеточному обновлению.
Разгадка запутанного ландшафта сигналов
Опухоли толстой кишки не возникают из-за одной повреждённой гены, а из запутанной сети сигналов между эпителиальными клетками, иммунными клетками и молекулами воспаления. Исследователи собрали большую он–офф (булеву) сеть, включающую 87 ключевых участников внутри типичной кишечной клетки и в её ближайшем иммунном окружении. Сюда вошли хорошо известные драйверы роста, тормоза программируемой смерти клетки и молекулы, выделяющиеся при воспалении. Затем они прогнали эту виртуальную сеть тысячи раз, отслеживая, как часто узел «пролиферация» (деление клеток) и узел «апоптоз» (программируемая гибель) оказывались включёнными. Такой подход позволил протестировать, как разные условия — например хроническое воспаление или общие для рака генетические изменения — сдвигают поведение системы в целом.
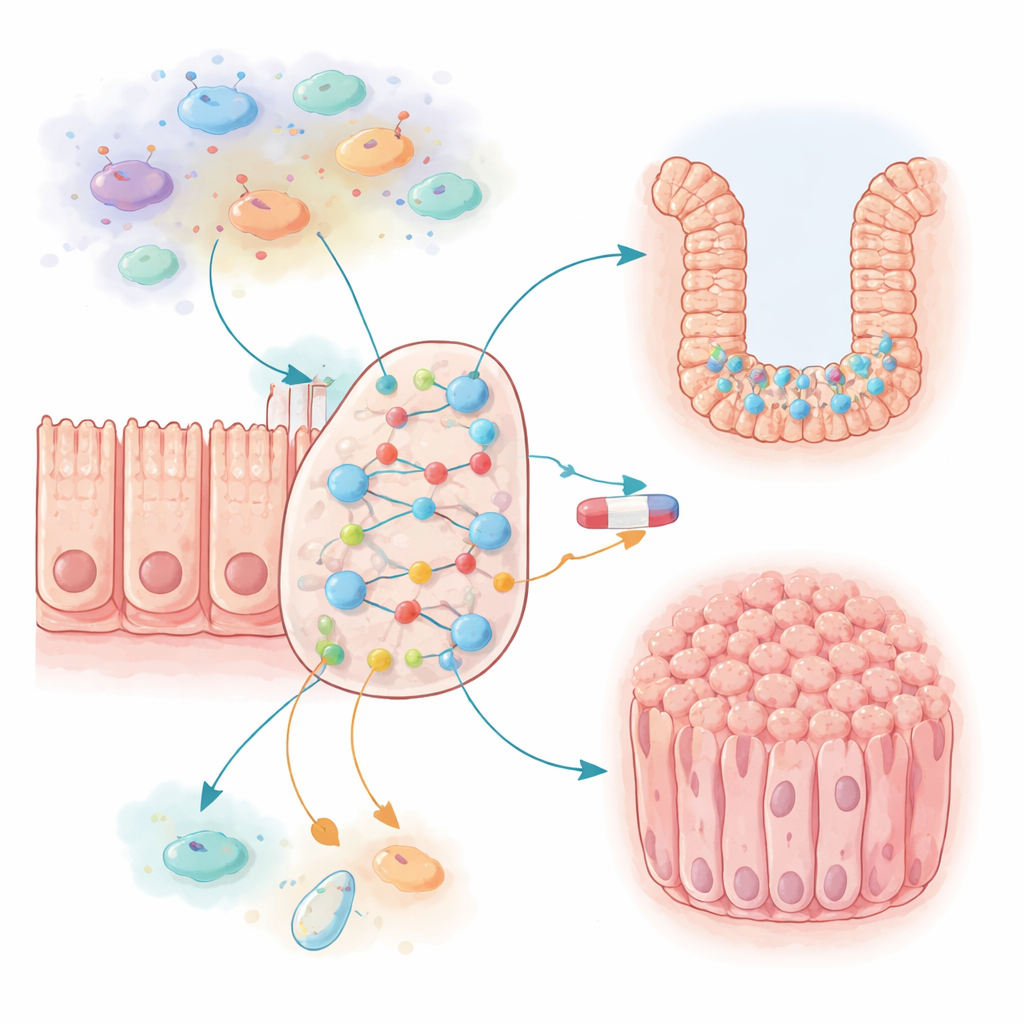
Когда воспаление запирает клетки в режиме роста
Первым сюрпризом стало то, что произошло при включении воспалительного окружения в модели. Сигналы, такие как IL6 и CCL2, вырабатываемые иммунными и эпителиальными клетками, образовали два укрепляющих друг друга петлевых механизма, которые сильно усиливали пути роста и подавляли гибель клеток. Если эти сигналы действовали в полной силе, модельные клетки толстой кишки становились почти бесконечно пролиферирующими и практически неуязвимыми для гибели — далеко от состояния здоровой ткани. Путём уменьшения вероятности включения IL6 и CCL2 авторы выявили «золотую середину», при которой клетки сохраняли низкий, нормальный уровень роста, но оставались чувствительными к воспалительным триггерам. Постоянная активация некоторых иммунных клеток приводила к хроническому состоянию, снижавшему апоптоз и слегка повышавшему пролиферацию, имитируя то, как длительное воспаление делает слизистую кишечника более уязвимой для рака.
Как распространённые генетические изменения подталкивают клетки за край
Далее исследователи ввели генетические изменения, часто встречающиеся при спорадическом колоректальном раке, такие как потеря «стража ворот» APC, активирующие изменения в RAS и потерю «опекуна» p53. В модели каждое из этих изменений по‑своему подпитывало те же два положительных петлевых механизма. В результате наблюдался явный сдвиг в сторону выживания и пролиферации: сигналы гибели клеток падали, а сигналы роста резко возрастали. В отличие от этого, имитируемая потеря хромосомного региона с SMAD и DCC — изменения, связанные с худшим прогнозом у реальных пациентов — едва влияла на пролиферацию или апоптоз в модели, что указывает на то, что пути, контролируемые этими генами, были недостаточно представлены и, возможно, требуют более детального моделирования для соответствия клинической реальности.
Внецелевые действия решают вопрос о пользе препаратов
Ключевая часть работы заключалась в том, чтобы выяснить, как блокирование различных лекарственных мишеней повлияет на эту сеть, особенно тех мишеней, на которые воздействуют обычные ингибиторы ЦОГ, такие как целекоксиб и суліндак. Когда в смоделированной клетке единственной проблемой была потеря APC, прямое блокирование COX2 или связанного фермента (PDE5) полностью восстанавливало здоровый баланс: рост снижался, а гибель клеток повышалась выше нормы, разрывая петлевые механизмы на ранней стадии. Но по мере накопления дополнительных мутаций в RAS и p53 — что соответствует промежуточным и поздним стадиям опухоли — простое блокирование COX2 мало что давало. В таких поздних состояниях более эффективно замедляло пролиферацию ингибирование пути роста, сосредоточенного вокруг AKT, или в меньшей степени NF-κB, хотя это всё ещё не могло полностью восстановить апоптоз. Модель также предполагала, что целекоксиб, который может воздействовать на AKT помимо COX2, должен превосходить суліндак в сдерживании роста опухолевых клеток при наличии нескольких мутаций.
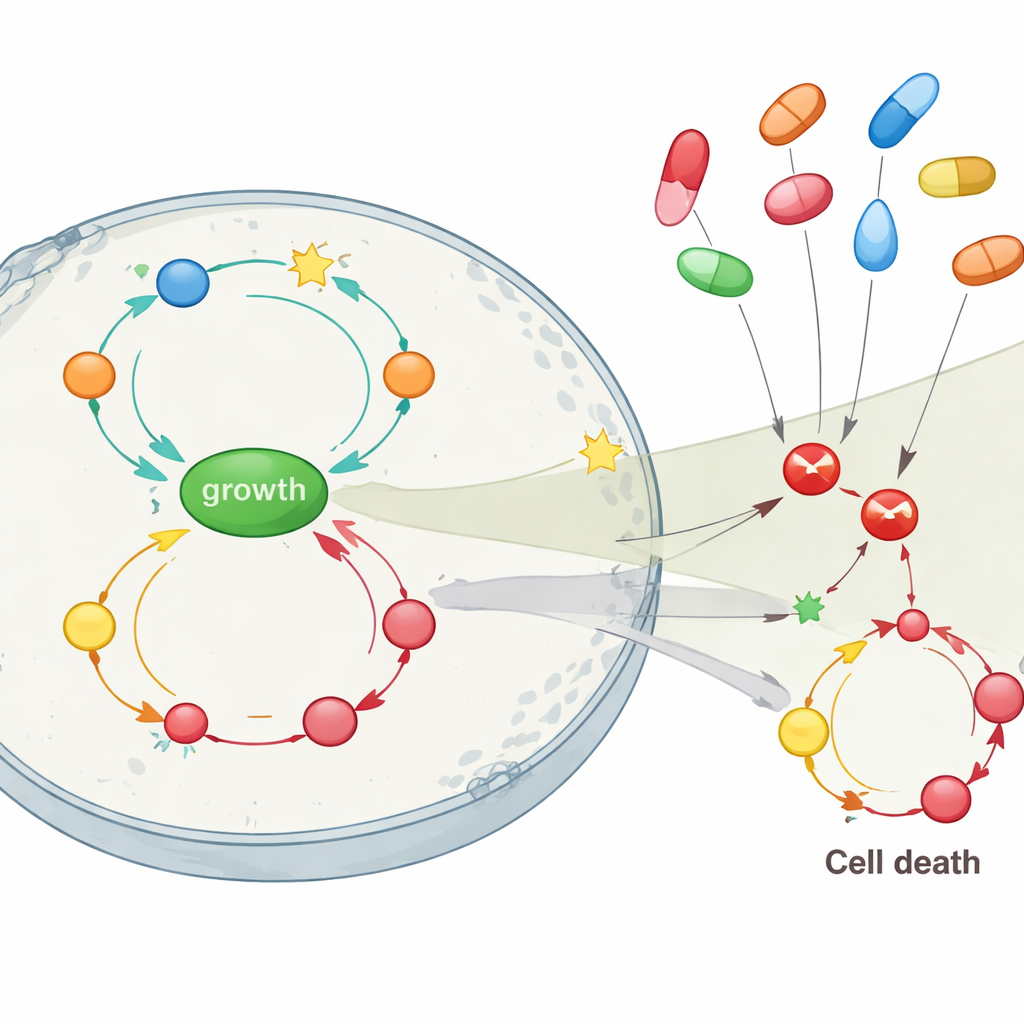
Что это значит для профилактики и лечения
Для неспециалиста ключевое послание таково: ингибиторы ЦОГ не действуют как простые одноцелевые препараты против рака толстой кишки. Их полезные эффекты, особенно на ранних стадиях заболевания, во многом могут опираться на дополнительные действия против других путей роста. Симуляции в исследовании показывают, что эти лекарства наиболее эффективны при применении до того, как опухоли накопят множество мутаций — особенно когда утрачен критический ген‑«страж» APC, но другие изменения ещё не замкнули цепи роста окончательно. При более поздних стадиях рака один только блок COX2 вряд ли будет достаточен, и внимание, возможно, придётся переключить на такие пути, как AKT. Карта этих сложных петлевых взаимодействий in silico поддерживает более индивидуализированный подход: использование генетической информации и статуса воспаления для решения, кто может получить пользу от профилактического применения ингибиторов ЦОГ, и когда могут потребоваться комбинированные стратегии, направленные на несколько узлов сети.
Цитирование: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Ключевые слова: колоректальный рак, воспаление, ингибиторы ЦОГ, сигнальные сети, путь AKT