Clear Sky Science · fr
Modélisation en réseau du cancer colorectal sporadique révèle l’importance des effets hors cible des inhibiteurs de la cyclooxygénase
Pourquoi cela compte pour la santé intestinale et le cancer
Le cancer colorectal est l’un des cancers les plus fréquents au monde, et de nombreuses personnes prennent déjà des analgésiques qui influent sur les mêmes voies impliquées dans cette maladie. Cette étude pose une question pragmatique aux grandes implications : lorsque des médicaments appelés inhibiteurs de la COX semblent ralentir ou prévenir les tumeurs du côlon, est-ce vraiment à cause de leur action principale prévue, ou bien d’autres effets « hors cible » à l’intérieur des cellules ? En construisant un modèle numérique détaillé des cellules du côlon et de leur environnement inflammatoire, les auteurs explorent quand et comment ces médicaments peuvent réellement faire basculer l’équilibre d’une croissance incontrôlée vers un renouvellement cellulaire normal.
Démêler un paysage de signaux encombré
Les tumeurs du côlon n’émergent pas d’un seul gène endommagé mais d’un réseau embrouillé de signaux entre cellules intestinales, cellules immunitaires et molécules inflammatoires. Les chercheurs ont assemblé un large réseau binaire (booléen) qui capture 87 acteurs clés au sein d’une cellule intestinale typique et de son environnement immunitaire proche. On y trouve des moteurs de croissance bien connus, des freins à la mort cellulaire et des molécules libérées pendant l’inflammation. Ils ont ensuite laissé ce réseau virtuel fonctionner des milliers de fois, en suivant la fréquence d’activation du nœud « prolifération » (division cellulaire) et du nœud « apoptose » (mort cellulaire programmée). Cette approche leur a permis de tester comment différentes conditions — comme une inflammation chronique ou des altérations génétiques courantes associées au cancer — modifient le comportement global du système.
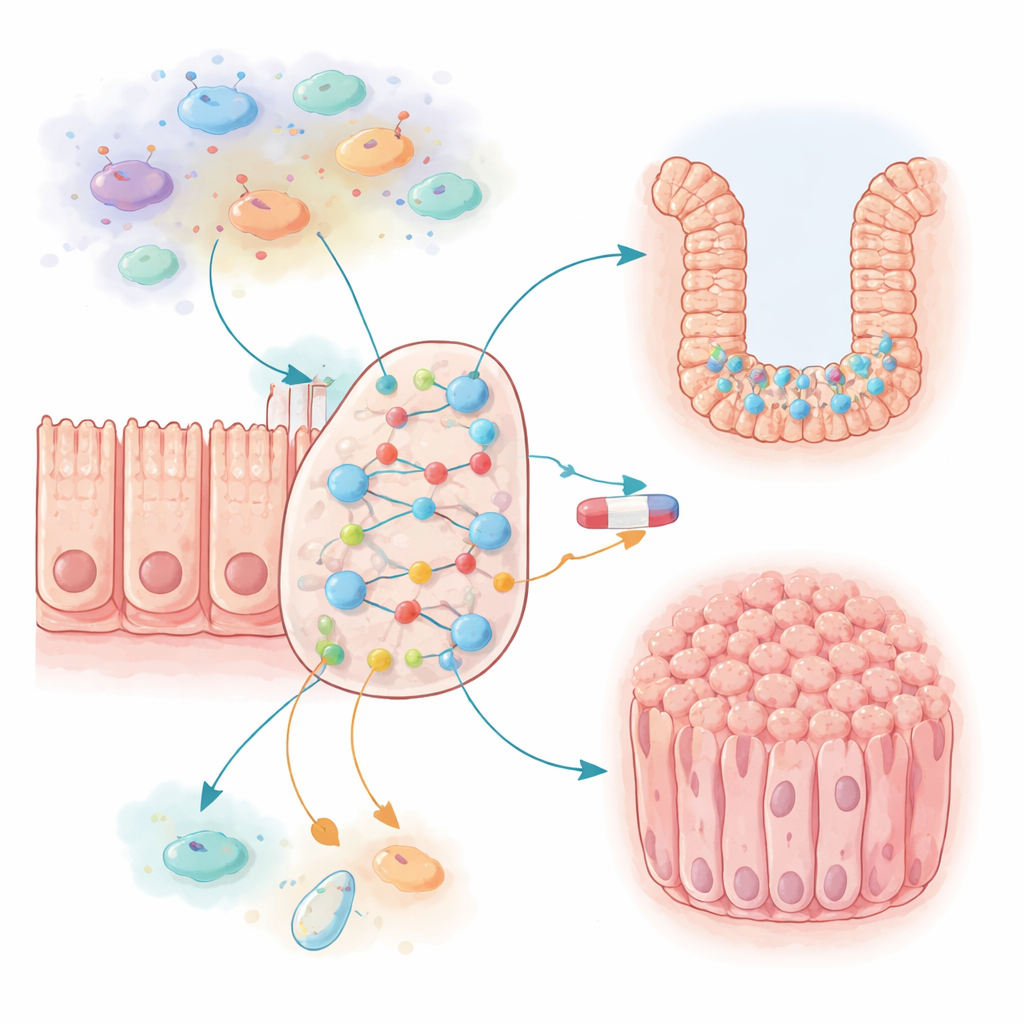
Quand l’inflammation verrouille les cellules en mode croissance
La première surprise est venue lorsque l’équipe a activé l’environnement inflammatoire dans son modèle. Des signaux tels que l’IL6 et la CCL2, produits par les cellules immunitaires et épithéliales, formaient deux boucles de rétroaction réciproques qui renforçaient fortement les voies de croissance et réduisaient l’apoptose. Si ces signaux agissaient à pleine intensité, les cellules coliques modélisées devenaient presque indéfiniment prolifératives et pratiquement impossibles à éliminer — bien loin de ce qui est observé dans un tissu sain. En diminuant la probabilité d’activation de l’IL6 et de la CCL2, les auteurs ont identifié une zone où les cellules conservaient un faible taux de croissance normal tout en restant réactives aux déclencheurs inflammatoires. L’activation persistante de certains types cellulaires immunitaires induisait un état chronique qui abaissait la mort cellulaire et augmentait légèrement la croissance, mimant la manière dont l’inflammation prolongée rend la muqueuse intestinale plus vulnérable au cancer.
Comment des altérations génétiques courantes poussent les cellules au-delà du seuil
Puis, les chercheurs ont introduit des altérations génétiques souvent observées dans le cancer colorectal sporadique, comme la perte du gène « gardien » APC, des mutations activatrices de RAS et la perte du gène protecteur p53. Dans le modèle, chacune de ces modifications alimentait, à sa manière, les mêmes deux boucles de rétroaction positive. Le résultat fut un déplacement net vers la survie et la prolifération : les signaux de mort cellulaire diminuaient tandis que les signaux de croissance augmentaient. En revanche, la perte simulée d’une région chromosomique contenant SMAD et DCC — altérations associées à un mauvais pronostic chez de vrais patients — modifiait à peine la prolifération ou l’apoptose dans le modèle, ce qui suggère que les voies contrôlées par ces gènes étaient sous-représentées et pourraient nécessiter une modélisation plus détaillée pour correspondre à la réalité clinique.
Les actions hors cible déterminent l’efficacité des médicaments
Le cœur de l’étude consistait à évaluer comment le blocage de différentes cibles médicamenteuses affectait ce réseau, en particulier les cibles visées par des inhibiteurs de COX courants comme le célécoxib et le sulindac. Lorsque le seul problème dans la cellule simulée était la perte d’APC, bloquer directement la COX2 ou une enzyme connexe (PDE5) rétablissait complètement l’équilibre sain : la croissance diminuait et la mort cellulaire augmentait au-delà de la normale, rompant précocement les boucles de rétroaction. Mais à mesure que des mutations supplémentaires de RAS et p53 s’ajoutaient — représentant des stades tumoraux intermédiaires et avancés — bloquer simplement la COX2 avait peu d’effet. Dans ces contextes tardifs, inhiber la voie de croissance centrée sur AKT, ou dans une moindre mesure NF-κB, était bien plus efficace pour ralentir la prolifération, quoique sans parvenir complètement à restaurer l’apoptose. Le modèle suggérait également que le célécoxib, qui peut cibler AKT en plus de la COX2, devrait surpasser le sulindac pour limiter la croissance des cellules tumorales lorsque plusieurs mutations sont présentes.
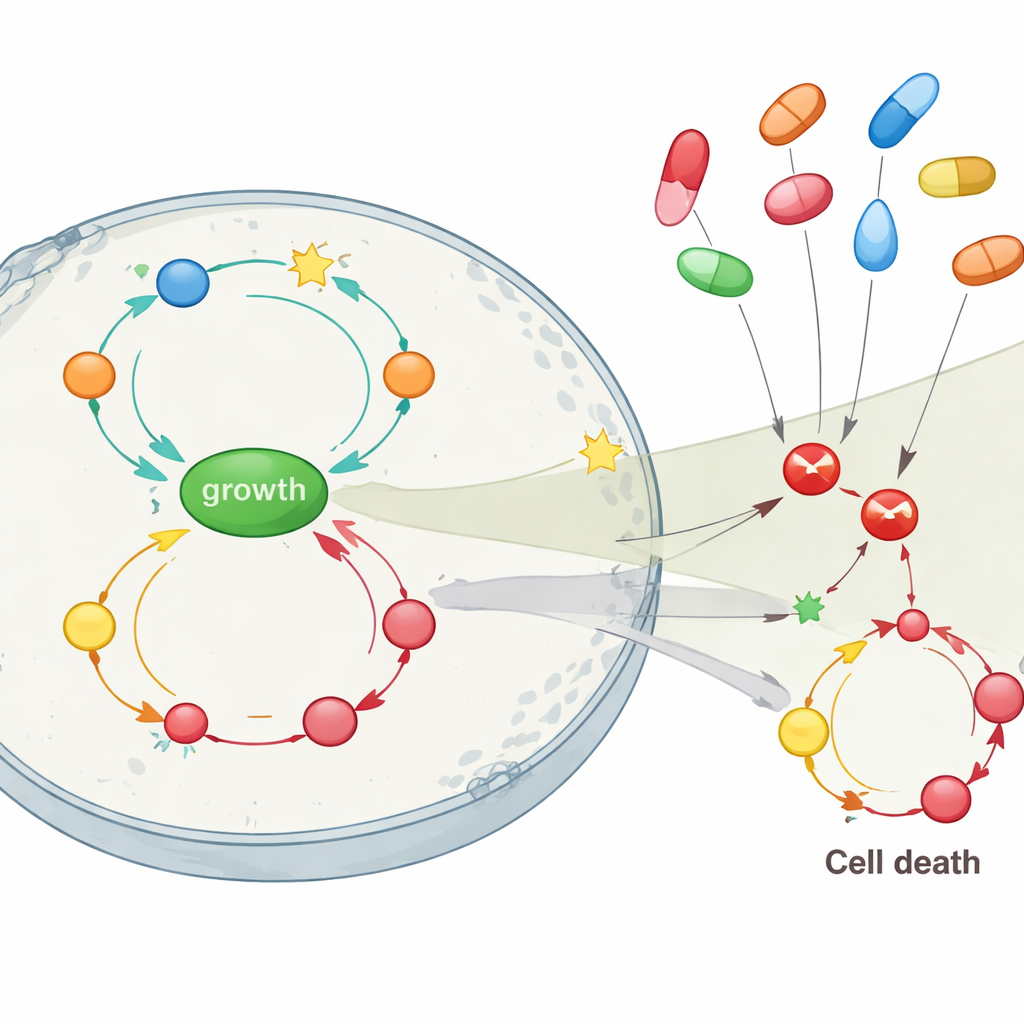
Ce que cela signifie pour la prévention et le traitement
Pour un non-spécialiste, le message clé est que les inhibiteurs de la COX ne fonctionnent pas comme des médicaments simples à cible unique contre le cancer du côlon. Leurs effets bénéfiques, notamment en phase précoce, peuvent dépendre fortement d’actions supplémentaires contre d’autres voies de croissance. Les simulations de l’étude suggèrent que ces médicaments sont les plus puissants lorsqu’ils sont utilisés avant que les tumeurs n’accumulent de nombreuses mutations — en particulier lorsque le gène gardien crucial APC est perdu mais que d’autres altérations n’ont pas encore complètement activé les circuits de croissance. Dans les cancers plus avancés, bloquer la COX2 seul sera probablement insuffisant, et l’attention devra peut-être se porter sur des voies comme AKT. En cartographiant in silico ces boucles de rétroaction complexes, le travail soutient une approche plus personnalisée : utiliser l’information génétique et le statut inflammatoire pour décider qui pourrait bénéficier d’un usage préventif d’inhibiteurs de COX, et quand des stratégies combinées ciblant plusieurs nœuds du réseau peuvent être nécessaires.
Citation: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Mots-clés: cancer colorectal, inflammation, inhibiteurs de la COX, réseaux de signalisation, voie AKT