Clear Sky Science · sv
Nätverksmodellering av sporadisk kolorektalcancer avslöjar vikten av off-target-effekter av cyklooxygenashämmare
Varför detta spelar roll för tarmhälsa och cancer
Kolorektalcancer är en av de vanligaste cancerformerna i världen, och många människor tar redan värkmediciner som påverkar samma vägar som är involverade i denna sjukdom. Denna studie ställer en praktisk fråga med stora följder: när läkemedel som kallas COX‑hämmare verkar sakta ner eller förebygga tarmtumörer, beror det verkligen på deras huvudverkan, eller på andra «off‑target»-effekter inne i cellerna? Genom att bygga en detaljerad digital modell av koloncellernas och deras inflammerade omgivnings beteende undersöker författarna när och hur dessa läkemedel verkligen kan vrida tillbaka balansen från okontrollerad tillväxt till normal cellomsättning.
Att reda ut ett trångt signalsystem
Kolontumörer uppstår inte av en enda skadad gen utan av ett invecklat nät av signaler mellan tarmsceller, immunceller och inflammatoriska molekyler. Forskarna satte samman ett stort av‑/på (Boolean) nätverk som fångar 87 centrala aktörer inne i en typisk tarmcell och i dess närliggande immiljö. Dessa inkluderar välkända tillväxtdrivkrafter, bromsar för celldöd och molekyler som frigörs vid inflammation. De lät sedan detta virtuella nätverk köras tusentals gånger och följde hur ofta noden «proliferation» (celldelning) och noden «apoptos» (programmerad celldöd) slutade i på‑läge. Detta tillvägagångssätt gjorde det möjligt att testa hur olika förutsättningar — såsom kronisk inflammation eller vanliga cancerkopplade genförändringar — förskjuter systemets övergripande beteende.
När inflammation låser celler i tillväxtläge
Den första överraskningen kom när teamet slog på den inflammatoriska miljön i sin modell. Signaler som IL6 och CCL2, som produceras av immunceller och epitelceller, bildade två självförstärkande återkopplingsslingor som kraftigt ökade tillväxtvägar och stängde ner celldöd. Om dessa signaler fick verka fullt ut blev modellens kolon‑celler nästan ändlöst proliferativa och nästintill omöjliga att döda — långt ifrån vad som ses i frisk vävnad. Genom att skala ner sannolikheten att IL6 och CCL2 aktiverades fann författarna en balanspunkt där cellerna bibehöll en låg, normal tillväxthastighet men fortfarande kunde reagera på inflammatoriska stimuli. Bestående aktivering av vissa immunceller skapade ett kroniskt tillstånd som sänkte celldöd och något ökade tillväxten, vilket efterliknar hur långvarig inflammation kan göra tarmens slemhinna mer mottaglig för cancer.
Hur vanliga genförändringar pushar celler över gränsen
Därefter införde forskarna genetiska förändringar som ofta ses i sporadisk kolorektalcancer, såsom förlust av portvaktsgenen APC, aktiverande förändringar i RAS och förlust av skyddsgenen p53. I modellen matade var och en av dessa förändringar, på sitt sätt, in i samma två positiva återkopplingsslingor. Resultatet blev en tydlig förskjutning mot överlevnad och proliferation: signaler för celldöd minskade medan tillväxtsignalerna ökade. I kontrast förändrade simuleringar av förlust av ett kromosomområde med SMAD och DCC — förändringar kopplade till dålig prognos hos verkliga patienter — knappt proliferation eller apoptos i modellen, vilket tyder på att vägarna som kontrolleras av dessa gener var underrepresenterade och kan behöva modelleras mer detaljerat för att överensstämma med klinisk verklighet.
Off‑target‑effekter avgör läkemedelsnyttan
Studien fokuserade på att se hur blockering av olika läkemedelsmål skulle påverka detta nätverk, särskilt mål som nås av vanliga COX‑hämmare som celecoxib och sulindac. När det enda felet i den simulerade cellen var förlust av APC återställde direkt blockering av COX2 eller ett närliggande enzym (PDE5) helt balansen: tillväxten sjönk och celldöden ökade över det normala, vilket bröt återkopplingsslingorna tidigt. Men när ytterligare mutationer i RAS och p53 lagts till — vilket representerar intermediära och sena tumörstadier — gjorde enkel COX2‑blockad väldigt lite nytta. I dessa senare situationer var hämning av tillväxtvägen centrerad kring AKT, eller i mindre utsträckning NF‑κB, betydligt effektivare för att bromsa proliferation, även om den fortfarande inte fullt ut kunde återuppliva celldöd. Modellen antydde också att celecoxib, som kan påverka AKT såväl som COX2, bör prestera bättre än sulindac när flera mutationer är närvarande.
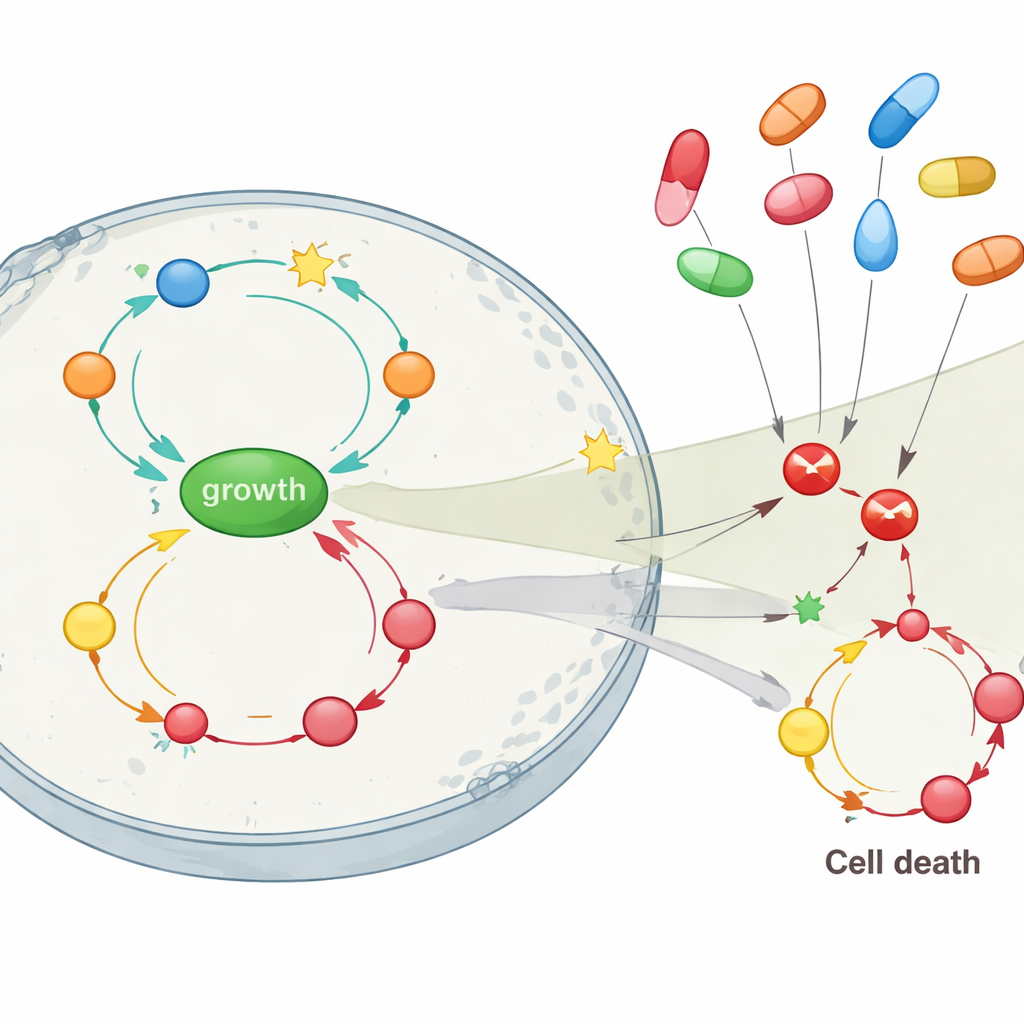
Vad detta betyder för prevention och behandling
För en icke‑expert är huvudbudskapet att COX‑hämmare inte fungerar som enkla, entydiga en‑målsläkemedel mot koloncancer. Deras gynnsamma effekter, särskilt i tidig sjukdom, kan i hög grad bero på ytterligare verkan mot andra tillväxtvägar. Studieresultaten tyder på att dessa läkemedel är mest kraftfulla när de används innan tumörer ackumulerat många mutationer — särskilt när den avgörande APC‑portvaktsgenen gått förlorad men andra förändringar ännu inte fullt ut låst fast tillväxtkretsarna. I mer avancerad cancer är det osannolikt att enbart COX2‑blockad räcker, och fokus kan behöva skifta mot vägar som AKT. Genom att kartlägga dessa komplexa återkopplingsslingor in silico stödjer arbetet en mer skräddarsydd strategi: att använda genetisk information och inflammationsstatus för att avgöra vem som kan ha nytta av förebyggande COX‑hämmarbehandling och när kombinationsstrategier som riktar flera noder i nätverket kan vara nödvändiga.
Citering: Gebhart, A.R., Berns, M.M.M., Snoeys, J. et al. Network modeling of sporadic colorectal cancer reveals the importance of off-target effects of Cyclooxygenase inhibitors. npj Syst Biol Appl 12, 50 (2026). https://doi.org/10.1038/s41540-025-00622-x
Nyckelord: kolorektalcancer, inflammation, COX-hämmare, signalsystem, AKT‑vägen