Clear Sky Science · zh
发现一种抑制 Endonuclease G 的 Ku80 肽,可保护 MLL 断点簇处免遭致白血病重排
保护患者免受隐性副作用伤害
化疗能挽救生命,但对少数患者而言,其会带来一个危险的晚期后果:治疗数年后,他们可能因一段易损的微小 DNA 区域受到损伤而发展成侵袭性血液癌。该研究揭示了一种天然切割 DNA 的酶如何促成这种损伤,并介绍了一种小型设计肽,能在不削弱化疗杀癌能力的前提下保护该危险 DNA 段。
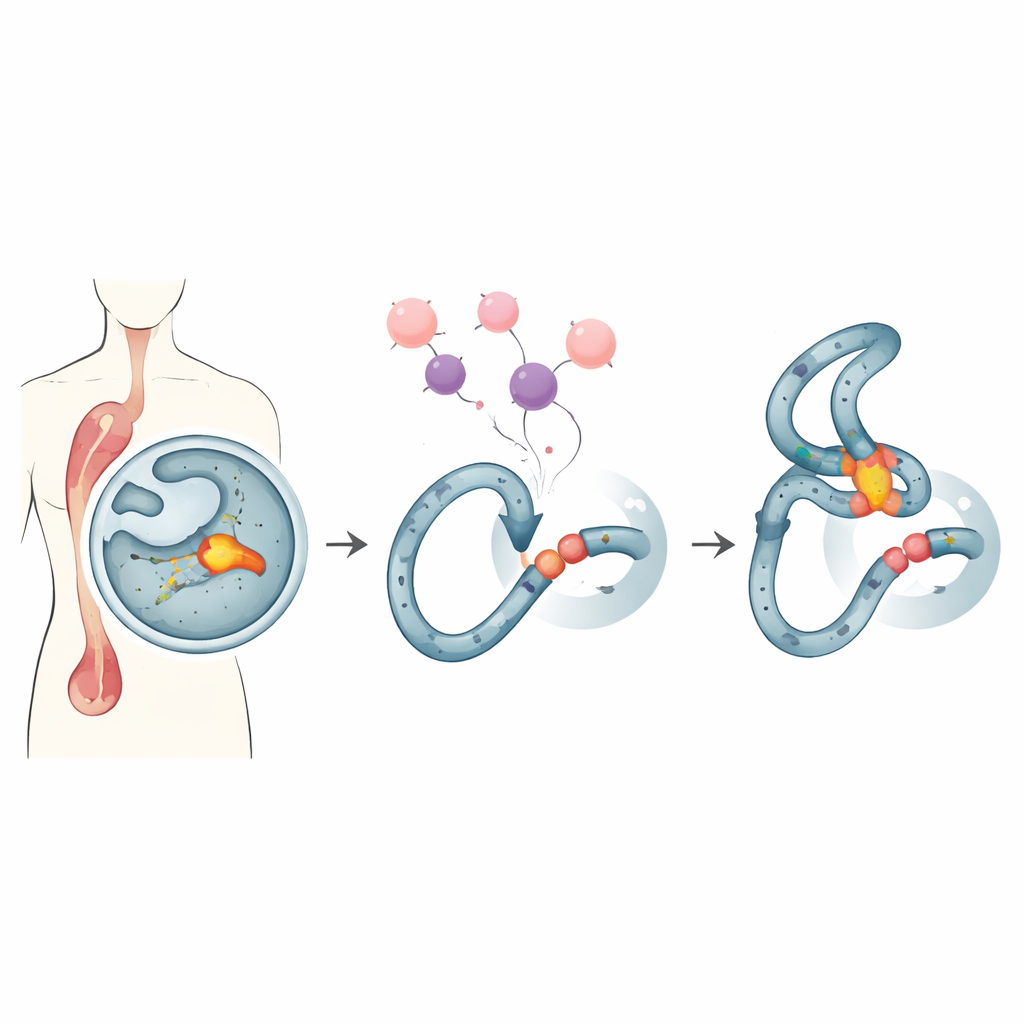
造血细胞中的脆弱位点
接受强效抗癌药物治疗的人中,有些随后会出现“治疗相关”白血病,这是一种难治的血液恶性肿瘤。这类病例中常见一个共同特征:MLL 基因的一个狭窄热点发生断裂与重排,该区域称为 MLL 断点簇。这个热点位于一段容易形成非典型构象并对某些药物特别敏感的 DNA 序列中。当像常用药阿霉素(doxorubicin)这样的标准治疗在分裂的细胞中产生应激时,该脆弱区域可能发生断裂并错误重连,产生驱动癌变的 DNA 融合。
一种古老的酶成为风险因子
研究团队聚焦于 Endonuclease G(简称 EndoG),这是一种进化上古老的酶,通常位于线粒体,但可迁移到细胞核内。EndoG 以在细胞凋亡过程中切割 DNA 而闻名,但在较低、非致死的水平下,它也能以促成突变的方式切割基因组。早期研究显示,在复制应激——由像阿霉素这样的药物引起的条件下——EndoG 会被招募到 MLL 热点并帮助启动那些先于白血病重排的断裂。鉴于 EndoG 的双重性,科学家们一直在寻求一种方法,在不阻断其杀死癌细胞的有益作用的情况下,限制其在该热点处的有害活性。
将修复蛋白转变为防护屏障
在果蝇中,EndoG 受到一种天然抑制蛋白的控制。人类中尚未发现对应的抑制物,但研究人员注意到,人类一种称为 Ku80 的 DNA 修复因子的一部分在结构上类似于果蝇的抑制子。Ku80 通常与 Ku70 配对以封堵断裂的 DNA 末端,然而其松散的尾部区域看起来能够与 EndoG 结合。通过生化试验和结构建模,作者表明 EndoG 确实附着于 Ku80 的尾部,并且 Ku80 的特定片段——称为 C 端结构域——可以与 EndoG 发生物理相互作用。当他们在人体细胞中仅表达该尾部片段时,MLL 热点处类似治疗引发的重排频率下降了一半,而正常 DNA 修复或化疗后细胞存活率并未改变。
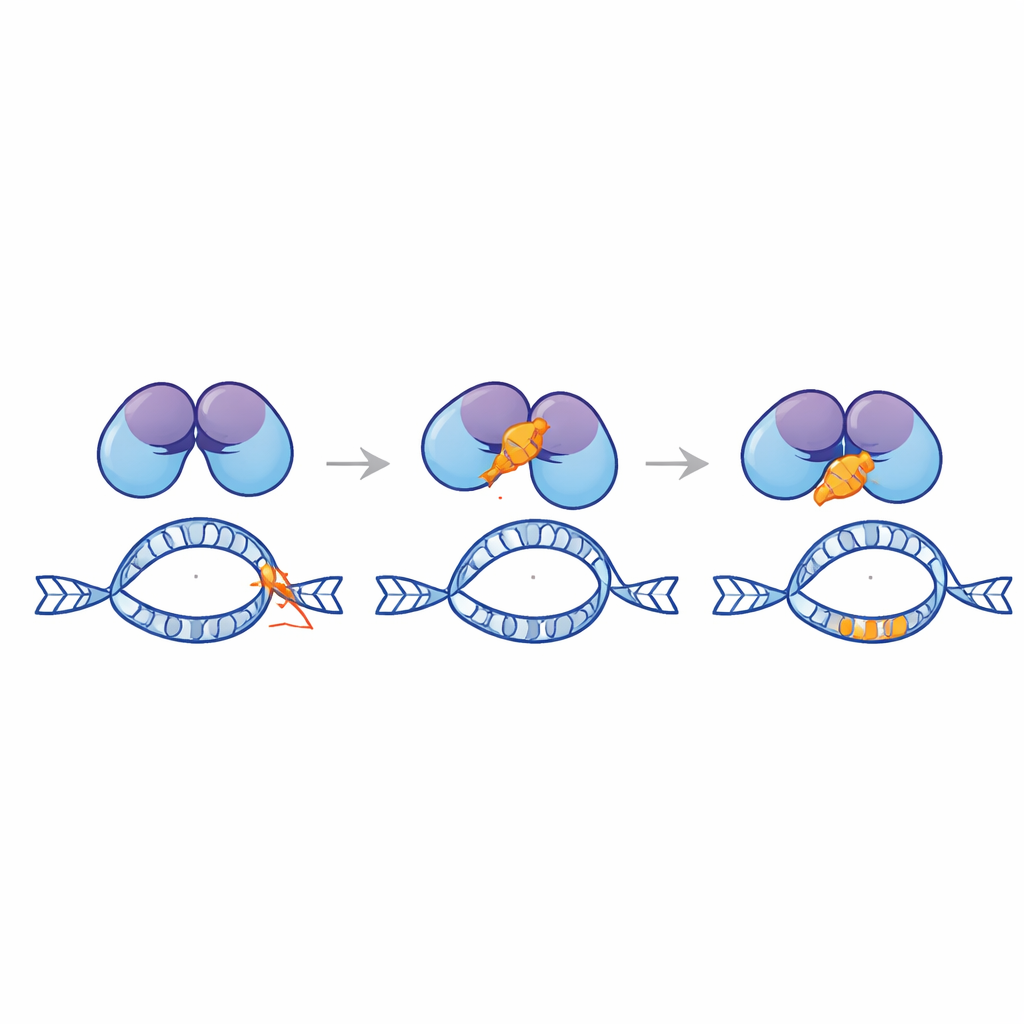
设计一种保护性肽
在计算建模的指导下,团队将 Ku80 的尾部切割成数千个候选短肽,并筛选出在模拟中对 EndoG 具有强结合预测的肽。从这个库中他们挑选出一个由 28 个氨基酸组成的肽,命名为 Ku3,在模拟中与 EndoG 紧密对接。将 Ku3 递送到携带工程化 MLL 报告系统的白血病和宫颈癌细胞系中时,它减少了阿霉素诱导的重排并保护了该热点的完整性,同样没有降低该药物杀伤细胞的能力。基于显微镜的邻近测定显示,Ku3 干扰了细胞核内 EndoG 与 Ku80 复合体的形成。单分子追踪进一步表明,Ku3 改变了 EndoG 与染色质的相互作用,这与在易损 DNA 位点上对 EndoG 实施直接物理制动一致。
从机制走向未来疗法
这项工作提出了一种精准的方式以减弱化疗的一个危险副作用:一种源自天然修复蛋白的定制肽可锁定 EndoG,阻止其攻击脆弱的 DNA 热点,从而降低发生致白血病重排的几率,同时保留化疗的致癌伤害作用。从长远看,此类肽——或基于相同基序开发的改良版本——可以与常规产 genotoxic 的药物联合使用,以保护患者的造血细胞,减少目前在成功癌症治疗后仍潜伏的继发性白血病风险。
引用: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
关键词: 治疗相关白血病, DNA 断裂热点, Endonuclease G, Ku80 肽抑制剂, 化疗副作用