Clear Sky Science · nl
Ontdekking van een Endonuclease G‑remmend Ku80‑peptide dat beschermt tegen leukemogene rearrangementen bij de MLL‑breekpuntcluster
Patienten beschermen tegen een verborgen bijwerking
Chemotherapie kan levens redden, maar bij een klein aantal patiënten heeft het een gevaarlijke late consequentie: jaren na de behandeling ontwikkelen zij agressieve bloedkankers die worden veroorzaakt door schade in een klein kwetsbaar stuk DNA. Deze studie onthult hoe een natuurlijk DNA‑knipend enzym bijdraagt aan die schade en introduceert een klein, ontworpen peptide dat dat risicovolle DNA‑segment beschermt zonder de kankerdodende kracht van de chemotherapie te verzwakken.
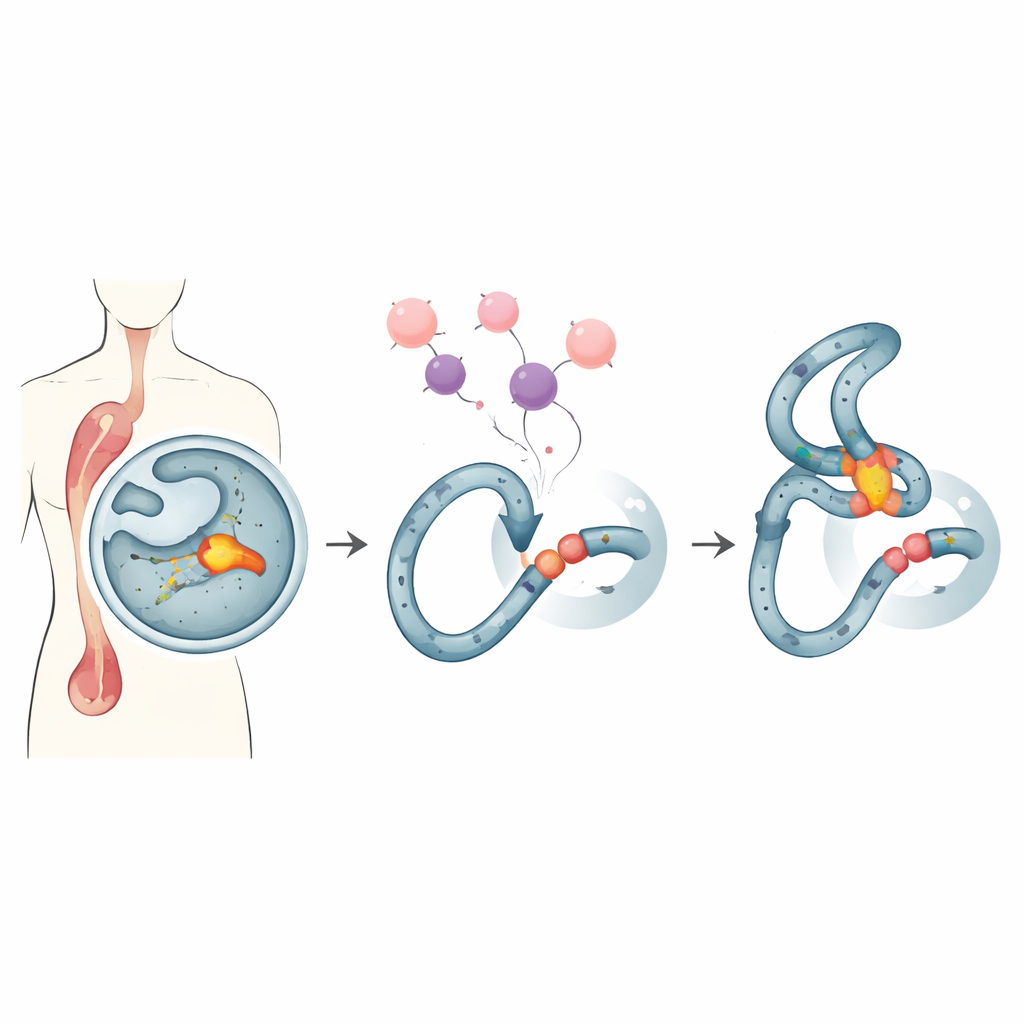
Een broos plekje in onze bloedvormende cellen
Sommige mensen die met krachtige kankermedicijnen zijn behandeld, ontwikkelen later een “therapie‑gerelateerde” leukemie, een moeilijk te behandelen bloedkanker. Veel van deze gevallen delen hetzelfde kenmerk: breuken en herschikkingen in een smal hotspot van het MLL‑gen, een gebied dat bekendstaat als de MLL‑breekpuntcluster. Dit hotspot ligt in een DNA‑stuk dat de neiging heeft ongebruikelijke vormen aan te nemen en is bijzonder gevoelig voor bepaalde medicijnen. Wanneer standaardbehandelingen zoals het veelgebruikte middel doxorubicine delende cellen belasten, kan dat fragiele gebied barsten en verkeerd weer aan elkaar voegen, wat DNA‑fusies creëert die kanker aanwakkeren.
Een oeroud enzym wordt een risicofactor
Het team richt zich op Endonuclease G, of EndoG, een evolutionair oud enzym dat normaal in mitochondriën huist maar naar de kern kan migreren. EndoG staat bekend om het knippen van DNA tijdens celdood, maar op lagere, niet‑dodelijke niveaus kan het ook het genoom insnijden op manieren die mutaties bevorderen. Eerder onderzoek liet zien dat onder replicatiestress — condities die door middelen zoals doxorubicine worden veroorzaakt — EndoG naar het MLL‑hotspot wordt gerekruteerd en helpt bij het initiëren van de breuken die aan leukemogene herschikkingen voorafgaan. Vanwege deze dubbele aard hebben wetenschappers gezocht naar een manier om EndoG’s schadelijke activiteit op dit hotspot te beperken zonder zijn nuttige rollen bij het doden van kankercellen te blokkeren.
Een reparatie‑eiwit omzetten in een schild
Bij fruitvliegen wordt EndoG onder controle gehouden door een natuurlijk remmend eiwit. Een dergelijke remmer was bij mensen niet bekend, maar de onderzoekers zagen dat een deel van een menselijk DNA‑reparatiefactor genaamd Ku80 structureel leek op de vliegremmer. Ku80 werkt meestal samen met Ku70 om gebroken DNA‑einden te sluiten, maar zijn losse staartregio leek in staat EndoG te binden. Met biochemische tests en structurele modellering toonden de auteurs aan dat EndoG inderdaad aan de staart van Ku80 hecht en dat een specifieke stretch van Ku80, het C‑terminale domein genoemd, fysiek met EndoG kan interacteren. Toen ze alleen dit staartfragment in menselijke cellen tot expressie brachten, halveerde dat de frequentie van therapie‑achtige herschikkingen bij het MLL‑hotspot, zonder normale DNA‑reparatie of celoverleving na chemotherapie te beïnvloeden.
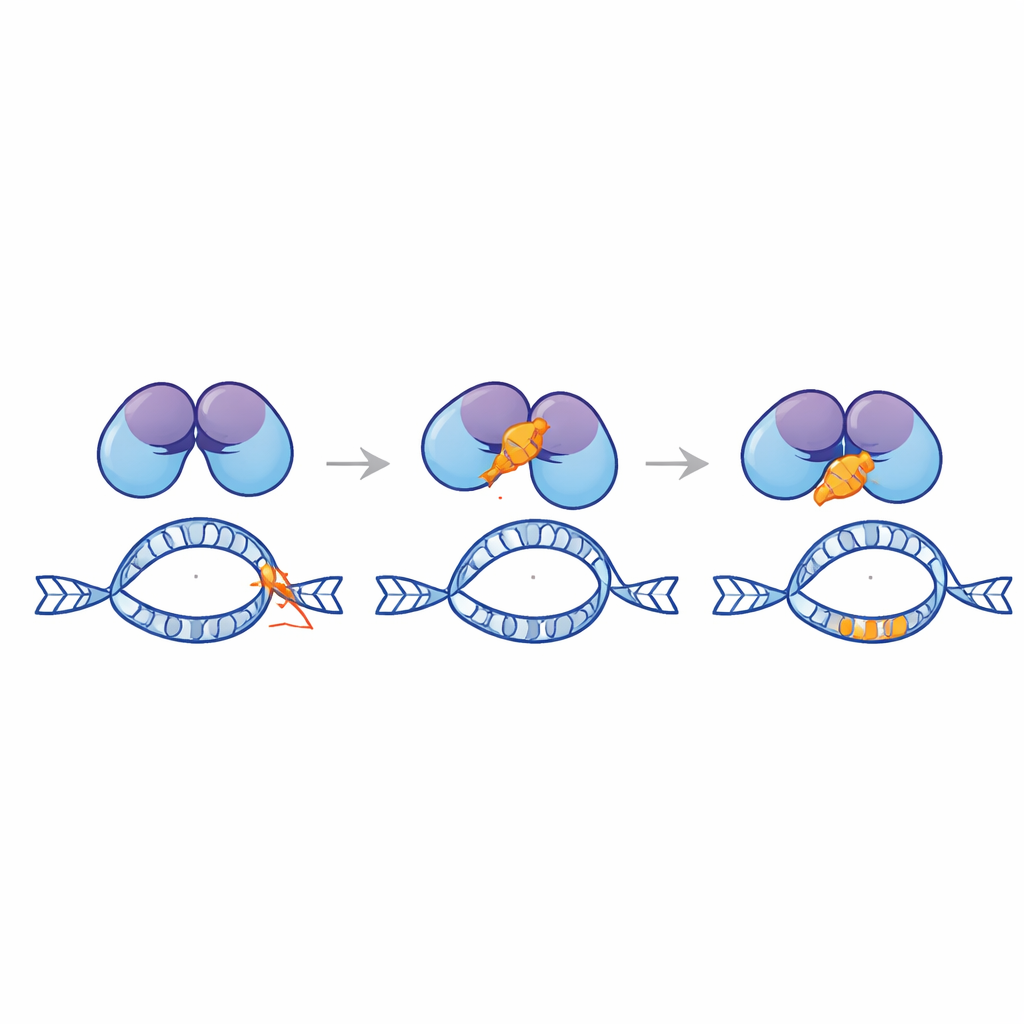
Ontwerpen van een beschermend peptide
Aan de hand van computermodellering hakte het team Ku80’s staart in duizenden kandidaat‑korte peptiden en screenede deze op sterke voorspelde binding aan EndoG. Uit deze bibliotheek selecteerden ze een 28‑aminozuurpeptide, genoemd Ku3, dat in simulaties stevig op EndoG aanpakte. Toen Ku3 in leukemie‑ en cervixkankercellijnen met een geconstrueerde MLL‑reporter werd gebracht, verminderde het de door doxorubicine geïnduceerde herschikkingen en beschermde het de integriteit van het hotspot, wederom zonder het vermogen van het medicijn om cellen te doden te verminderen. Microscopie‑gebaseerde nabijheidsassays toonden aan dat Ku3 de vorming van complexen tussen EndoG en Ku80 in de kern verstoort. Single‑molecule tracking liet verder zien dat Ku3 verandert hoe EndoG met chromatine interageert, wat overeenkomt met een directe fysieke rem op EndoG op kwetsbare DNA‑plaatsen.
Van mechanisme naar toekomstige therapie
Dit werk stelt een precieze manier voor om een gevaarlijke bijwerking van chemotherapie af te zwakken: een op maat gemaakt peptide afgeleid van een natuurlijk reparatieeiwit hecht zich aan EndoG, voorkomt dat het een fragiel DNA‑hotspot aanvalt en verlaagt daardoor de kans op leukemogene herschikkingen, terwijl de kankerdodende schade intact blijft. Op de lange termijn zouden zulke peptiden — of verbeterde versies gebaseerd op hetzelfde motief — samen met standaard genotoxische geneesmiddelen kunnen worden toegediend om de bloedvormende cellen van patiënten te beschermen en het risico op secundaire leukemieën te verminderen dat momenteel succesvolle kankerbehandelingen overschaduwt.
Bronvermelding: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Trefwoorden: therapie‑gerelateerde leukemie, DNA‑breuk hotspots, endonuclease G, Ku80 peptideremmer, bijwerkingen van chemotherapie