Clear Sky Science · es
Descubrimiento de un péptido inhibidor de Endonuclease G derivado de Ku80 que protege frente a reordenamientos leucemógenos en el clúster de ruptura de MLL
Protegiendo a los pacientes de un efecto secundario oculto
La quimioterapia puede salvar vidas, pero para un pequeño número de pacientes tiene una consecuencia tardía peligrosa: años después del tratamiento desarrollan cánceres sanguíneos agresivos desencadenados por daños en un tramo minúsculo y vulnerable del ADN. Este estudio revela cómo una enzima natural que corta el ADN contribuye a ese daño e introduce un pequeño péptido diseñado que protege el segmento de ADN de riesgo sin debilitar el poder para matar al cáncer de la quimioterapia.
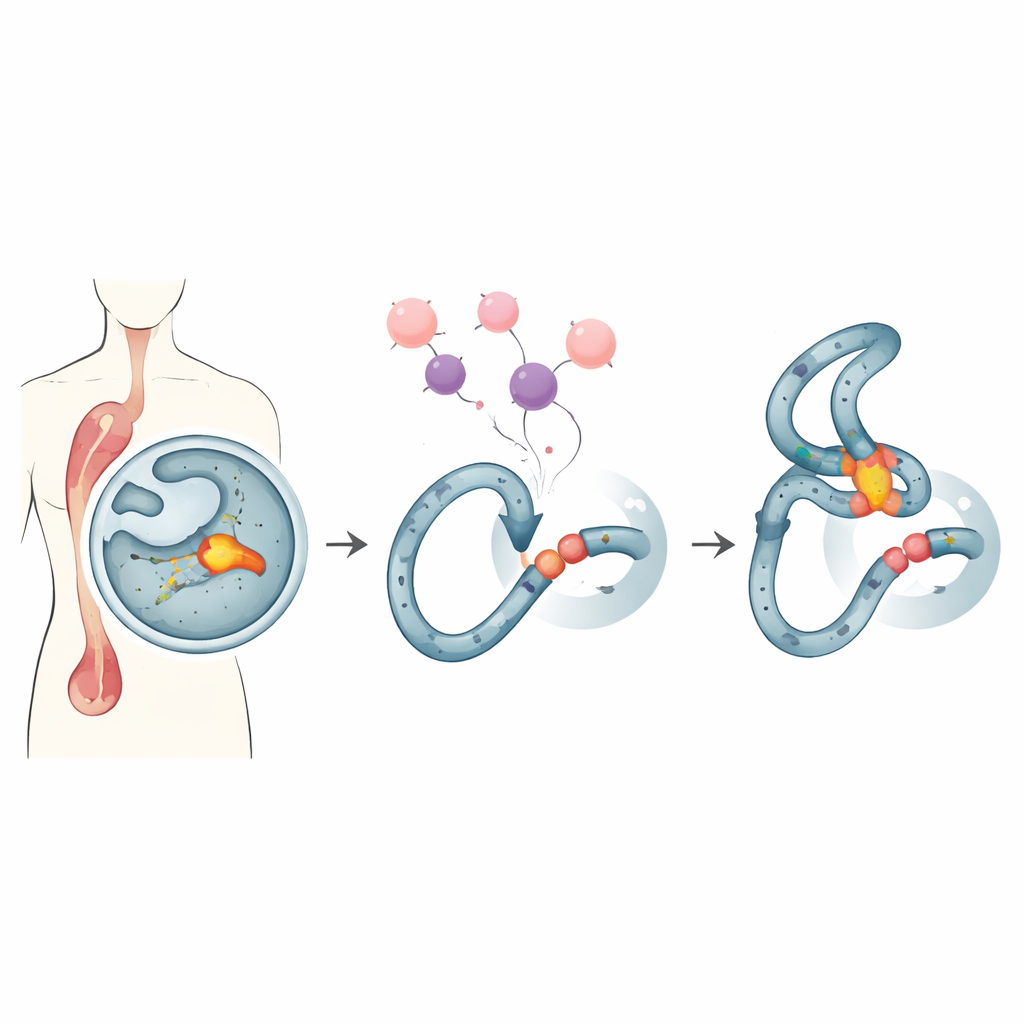
Un punto frágil en nuestras células formadoras de sangre
Algunas personas tratadas con fármacos contra el cáncer de gran potencia desarrollan más tarde una leucemia «relacionada con la terapia», un cáncer sanguíneo difícil de tratar. Muchos de estos casos comparten la misma señal: roturas y reordenamientos en un estrecho punto caliente del gen MLL, una región conocida como el clúster de ruptura de MLL. Este punto caliente se localiza en un tramo de ADN que tiende a formar estructuras inusuales y es especialmente sensible a ciertos fármacos. Cuando tratamientos estándar, como el ampliamente usado doxorrubicina, estresan a las células en división, esa región frágil puede romperse y volverse a unir incorrectamente, creando fusiones de ADN que impulsan el cáncer.
Una enzima ancestral se convierte en factor de riesgo
El equipo se centra en la Endonucleasa G, o EndoG, una enzima evolutivamente antigua que normalmente reside en las mitocondrias pero que puede trasladarse al núcleo. Se conoce a EndoG por cortar el ADN durante la muerte celular, sin embargo, a niveles más bajos y no letales también puede provocar muescas en el genoma que favorecen mutaciones. Trabajos previos mostraron que bajo estrés de replicación —condiciones creadas por fármacos como la doxorrubicina— EndoG es reclutada al punto caliente de MLL y ayuda a iniciar las roturas que preceden a los reordenamientos leucémicos. Debido a esta naturaleza dual, los científicos han buscado una forma de contener la actividad dañina de EndoG en este punto caliente sin bloquear sus funciones útiles en la eliminación de células cancerosas.
Convertir una proteína reparadora en un escudo
En moscas, EndoG está controlada por una proteína inhibidora natural. No se conocía un inhibidor similar en humanos, pero los investigadores observaron que parte de un factor humano de reparación del ADN llamado Ku80 se parece estructuralmente al inhibidor de la mosca. Ku80 normalmente forma pareja con Ku70 para sellar extremos rotos del ADN, sin embargo su región terminal flexible parecía capaz de unirse a EndoG. Mediante ensayos bioquímicos y modelado estructural, los autores demostraron que EndoG se une efectivamente a la cola de Ku80 y que un tramo específico de Ku80, denominado dominio C-terminal, puede interactuar físicamente con EndoG. Cuando expresaron solo este fragmento de la cola en células humanas, redujo a la mitad la frecuencia de reordenamientos tipo terapia en el punto caliente de MLL, sin alterar la reparación normal del ADN ni la supervivencia celular tras la quimioterapia.
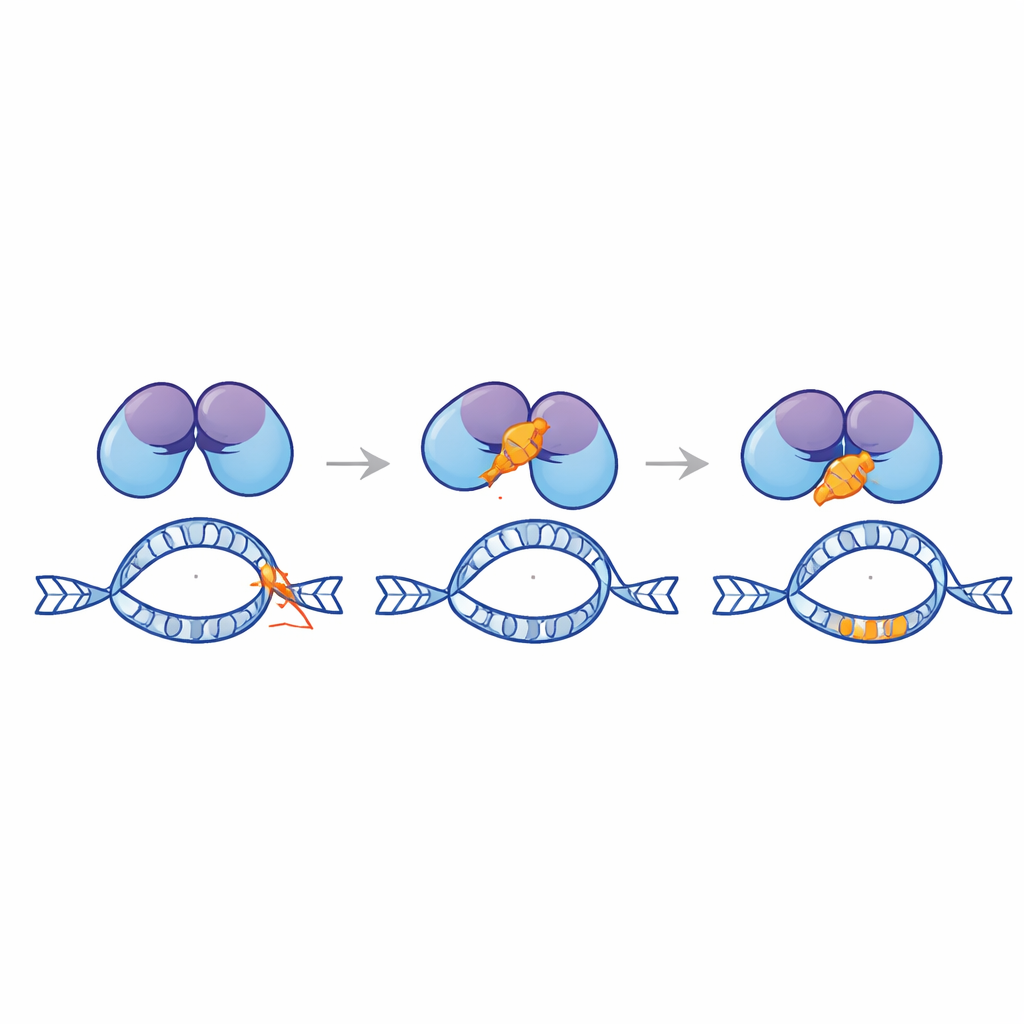
Diseñando un péptido protector
Guiado por modelado por ordenador, el equipo fragmentó la cola de Ku80 en miles de péptidos cortos candidatos y los examinó en busca de fuerte afinidad predicha por EndoG. De esta biblioteca seleccionaron un péptido de 28 aminoácidos, denominado Ku3, que se acoplaba de forma estrecha a EndoG en las simulaciones. Cuando Ku3 se introdujo en líneas celulares de leucemia y de cáncer de cuello uterino que portaban un reportero MLL diseñado, redujo los reordenamientos inducidos por doxorrubicina y protegió la integridad del punto caliente, de nuevo sin disminuir la capacidad del fármaco para matar células. Ensayos de proximidad basados en microscopía mostraron que Ku3 interrumpe la formación de complejos entre EndoG y Ku80 en el núcleo. El seguimiento de moléculas individuales reveló además que Ku3 cambia la interacción de EndoG con la cromatina, coherente con un freno físico directo sobre EndoG en sitios de ADN vulnerables.
Del mecanismo a una terapia futura
Este trabajo propone una forma precisa de mitigar un efecto secundario peligroso de la quimioterapia: un péptido hecho a medida derivado de una proteína reparadora natural se une a EndoG, le impide atacar un punto caliente de ADN frágil y así reduce la probabilidad de reordenamientos leucemógenos, todo ello dejando intacto el daño que mata al cáncer. A largo plazo, tales péptidos —o versiones mejoradas basadas en el mismo motivo— podrían administrarse conjuntamente con fármacos genotóxicos estándar para proteger las células formadoras de sangre de los pacientes y reducir el riesgo de leucemias secundarias que actualmente acompañan a tratamientos contra el cáncer que, por lo demás, tienen éxito.
Cita: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Palabras clave: leucemia relacionada con la terapia, puntos calientes de rotura del ADN, endonucléasa G, péptido inhibidor de Ku80, efectos secundarios de la quimioterapia