Clear Sky Science · pt
Descoberta de um peptídeo inibidor da endonuclease G derivado de Ku80 que protege contra rearranjos leucemogênicos no aglomerado de quebras do MLL
Protegendo pacientes de um efeito colateral oculto
A quimioterapia pode salvar vidas, mas para um pequeno número de pacientes ela tem uma consequência tardia perigosa: anos após o tratamento, desenvolvem cânceres sanguíneos agressivos desencadeados por danos em um pequeno trecho vulnerável do DNA. Este estudo revela como uma enzima natural que corta DNA contribui para esse dano e apresenta um pequeno peptídeo projetado que protege o segmento de DNA de risco sem enfraquecer o poder de eliminação de células cancerígenas da quimioterapia.
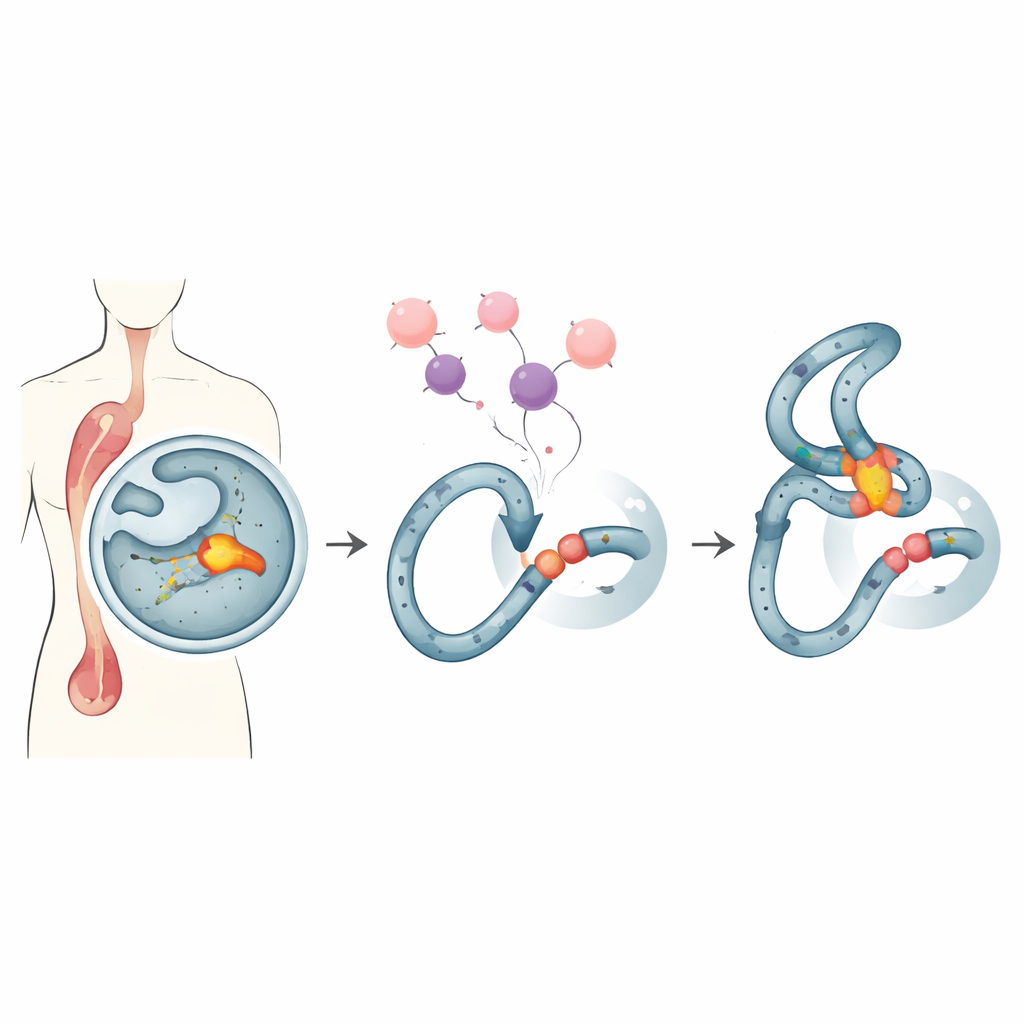
Um ponto frágil nas nossas células formadoras de sangue
Algumas pessoas tratadas com drogas anticâncer potentes desenvolvem mais tarde uma leucemia “relacionada à terapia”, um câncer sanguíneo de difícil tratamento. Muitos desses casos compartilham a mesma marca registrada: quebras e rearranjos em um ponto estreito do gene MLL, uma região conhecida como o aglomerado de quebras do MLL. Esse ponto sensível fica em um trecho de DNA que tende a formar estruturas incomuns e é especialmente suscetível a certos fármacos. Quando tratamentos padrão, como a amplamente utilizada doxorrubicina, estressam células em divisão, essa região frágil pode rachar e se religar de forma incorreta, criando fusões de DNA que dirigem o câncer.
Uma enzima ancestral torna-se um fator de risco
A equipe concentra-se na Endonuclease G, ou EndoG, uma enzima evolutivamente antiga que normalmente reside nas mitocôndrias, mas pode deslocar‑se para o núcleo. A EndoG é conhecida por fragmentar DNA durante a morte celular, mas em níveis mais baixos, não letais, também pode provocar incisões no genoma que favorecem mutações. Trabalhos anteriores mostraram que sob estresse de replicação — condições criadas por fármacos como a doxorrubicina — a EndoG é recrutada para o ponto sensível do MLL e ajuda a iniciar as quebras que precedem os rearranjos leucêmicos. Por causa dessa natureza dupla, os cientistas buscaram uma forma de conter a atividade nociva da EndoG nesse ponto sem bloquear seus papéis úteis na eliminação de células cancerígenas.
Transformando uma proteína de reparo em um escudo
Em moscas, a EndoG é mantida sob controle por uma proteína inibidora natural. Não se conhecia um inibidor semelhante em humanos, mas os pesquisadores notaram que parte de um fator humano de reparo do DNA chamado Ku80 se assemelha estruturalmente ao inibidor da mosca. O Ku80 normalmente se associa ao Ku70 para selar extremidades de DNA quebrado, mas sua região terminal flexível parecia capaz de se ligar à EndoG. Usando testes bioquímicos e modelagem estrutural, os autores mostraram que a EndoG de fato se liga à cauda do Ku80 e que um trecho específico do Ku80, chamado domínio C‑terminal, pode interagir fisicamente com a EndoG. Quando expressaram apenas esse fragmento da cauda em células humanas, reduziram pela metade a frequência de rearranjos semelhantes aos induzidos por terapia no ponto sensível do MLL, sem alterar o reparo normal do DNA ou a sobrevivência celular após quimioterapia.
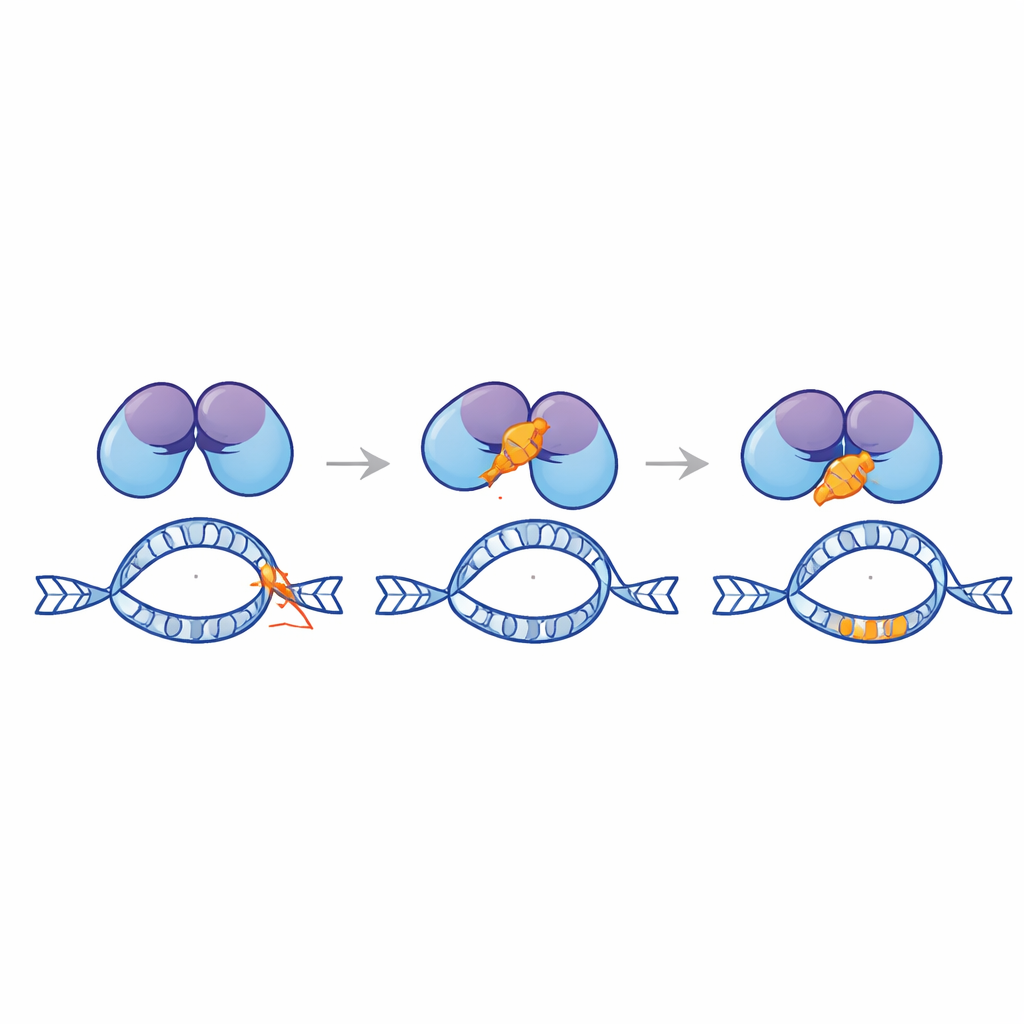
Desenhando um peptídeo protetor
Guiada por modelagem computacional, a equipe recortou a cauda do Ku80 em milhares de candidatos a peptídeos curtos e os triou quanto à forte ligação prevista à EndoG. Dessa biblioteca, destacou‑se um peptídeo de 28 aminoácidos, batizado de Ku3, que encaixou fortemente na EndoG nas simulações. Quando Ku3 foi entregue em linhas celulares de leucemia e câncer cervical contendo um repórter MLL construído, reduziu os rearranjos induzidos pela doxorrubicina e protegeu a integridade do ponto sensível, novamente sem diminuir a capacidade do fármaco de matar células. Ensaios de proximidade baseados em microscopia mostraram que Ku3 interrompe a formação de complexos entre EndoG e Ku80 no núcleo. Rastreamento de molécula única revelou ainda que Ku3 altera como a EndoG interage com a cromatina, consistente com um freio físico direto sobre a EndoG em sítios de DNA vulneráveis.
Do mecanismo à terapia futura
Este trabalho propõe uma forma precisa de atenuar um efeito colateral perigoso da quimioterapia: um peptídeo sob medida derivado de uma proteína natural de reparo liga‑se à EndoG, impede que ela ataque um ponto frágil do DNA e assim reduz a probabilidade de rearranjos leucemogênicos, sem comprometer o dano que mata o câncer. A longo prazo, tais peptídeos — ou versões aprimoradas baseadas no mesmo motivo — poderiam ser coadministrados com fármacos genotóxicos padrão para proteger as células formadoras de sangue dos pacientes e diminuir o risco de leucemias secundárias que hoje acompanham tratamentos bem‑sucedidos contra o câncer.
Citação: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Palavras-chave: leucemia relacionada à terapia, pontos quentes de quebra do DNA, endonuclease G, peptídeo inibidor de Ku80, efeitos colaterais da quimioterapia