Clear Sky Science · sv
Upptäckt av en Endonukleas G‑hämmande Ku80‑peptid som skyddar mot leukemogena omarrangemang vid MLL:s brytpunktssvärm
Skydda patienter från en dold biverkning
Kemoterapi kan rädda liv, men för ett litet antal patienter har den en farlig sen följd: år efter behandlingen utvecklar de aggressiva blodcancerformer som utlöses av skador i ett litet sårbart DNA‑stycke. Denna studie klargör hur ett naturligt DNA‑skärande enzym bidrar till den skadan och presenterar en liten designad peptid som skyddar det riskabla DNA‑segmentet utan att försvaga kemoterapins cancerdödande effekt.
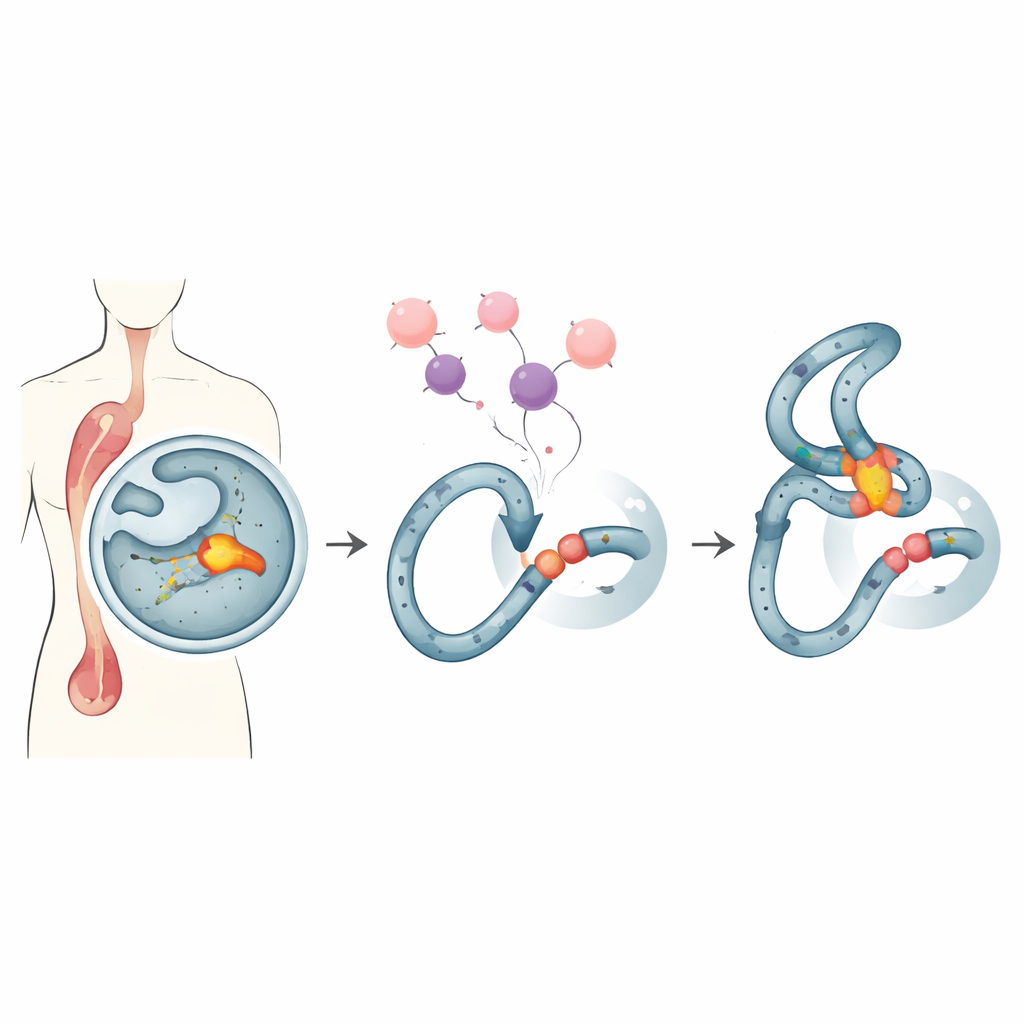
En skör plats i våra blodbildande celler
Vissa personer som behandlats med potenta cancermedel utvecklar senare så kallad ”terapirelaterad” leukemi, en svårbehandlad blodcancer. Många av dessa fall har samma kännetecken: brott och omarrangemang i en smal hotspot i MLL‑genen, ett område känt som MLL breakpoint cluster. Denna hotspot ligger i en DNA‑sekvens som tenderar att anta ovanliga former och är särskilt känslig för vissa läkemedel. När standardbehandlingar som det ofta använda läkemedlet doxorubicin stressar delande celler kan det sköra området spricka och återfogas felaktigt, vilket skapar DNA‑fusioner som driver cancer.
Ett uråldrigt enzym blir en riskfaktor
Forskargruppen fokuserar på Endonukleas G, eller EndoG, ett evolutionärt gammalt enzym som normalt finns i mitokondrier men som kan förflytta sig till cellkärnan. EndoG är känt för att klyva DNA under celldöd, men vid lägre, icke‑dödande nivåer kan det också skära i genomet på sätt som främjar mutationer. Tidigare arbete visade att under replikationsstress — förhållanden som skapas av läkemedel som doxorubicin — rekryteras EndoG till MLL‑hotspoten och hjälper till att initiera de brott som föregår leukemiska omarrangemang. På grund av denna dubbla natur har forskare sökt efter ett sätt att dämpa EndoG:s skadliga aktivitet vid denna hotspot utan att blockera dess nyttiga roller i att döda cancerceller.
Att förvandla ett reparationsprotein till en sköld
I fruktflugor hålls EndoG i schack av ett naturligt inhibitorprotein. Någon motsvarande inhibitor har inte varit känd hos människor, men forskarna noterade att en del av det humana DNA‑reparationsfaktorn Ku80 strukturellt liknar flugans inhibitor. Ku80 samarbetar vanligen med Ku70 för att täta brutna DNA‑ändar, men dess lösa svansregion verkade kunna binda EndoG. Med hjälp av biokemiska tester och strukturell modellering visade författarna att EndoG verkligen fäster vid Ku80:s svans och att en specifik del av Ku80, kallad C‑terminala domänen, kan interagera fysiskt med EndoG. När de uttryckte enbart denna svansfragment i humana celler halverades frekvensen av terapi‑lika omarrangemang vid MLL‑hotspoten, utan att påverka normal DNA‑reparation eller cells överlevnad efter kemoterapi.
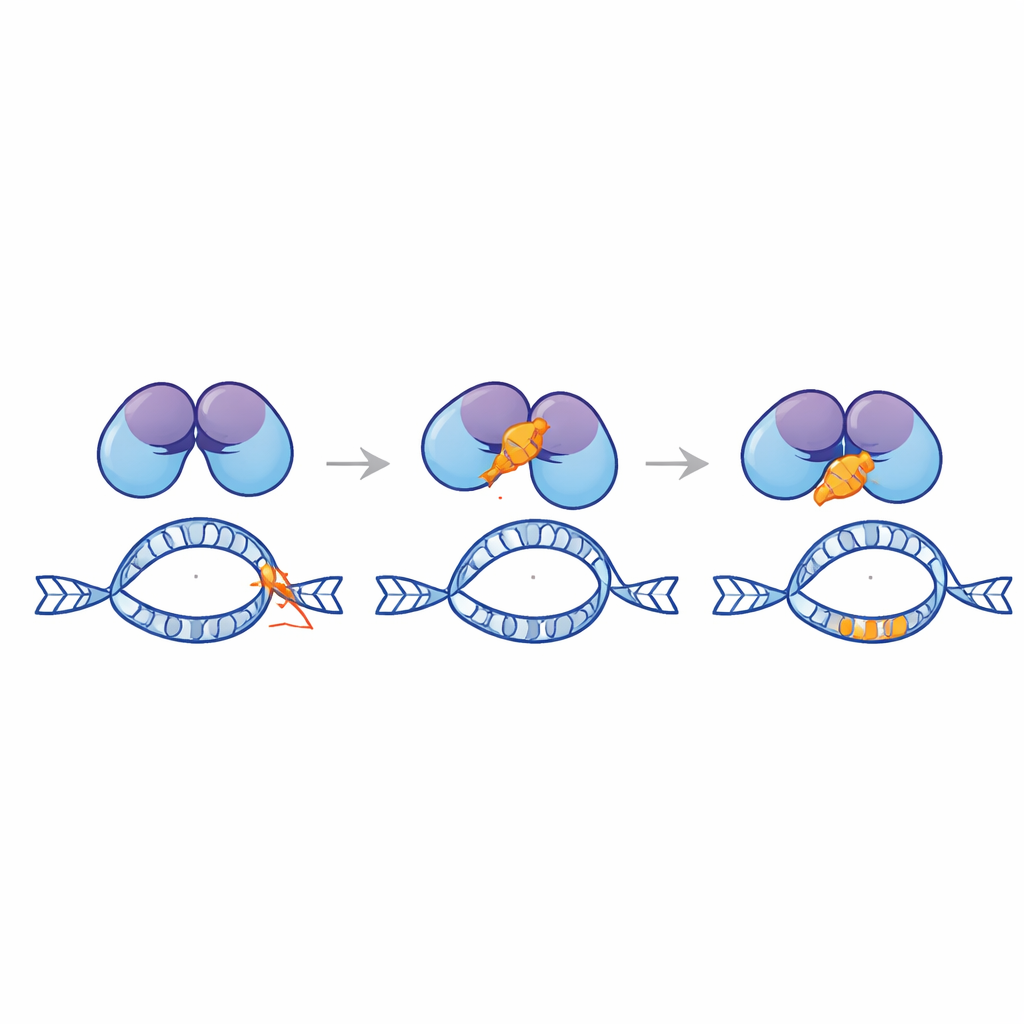
Design av en skyddande peptid
Med hjälp av datorbaserad modellering delade forskarna upp Ku80‑svansen i tusentals kandidatkortpeptider och screenade dem för starkt förutspått bindande till EndoG. Ur detta bibliotek valde de ut en 28‑aminosyra‑peptid, kallad Ku3, som i simuleringarna dockade tätt mot EndoG. När Ku3 levererades till leukemi‑ och livmoderhalscancercellinjer som bar en konstruerad MLL‑rapportör reducerade den doxorubicin‑inducerade omarrangemang och skyddade hotspotens integritet, återigen utan att minska läkemedlets förmåga att döda celler. Mikroskopibaserade proximetets‑tester visade att Ku3 stör bildandet av komplex mellan EndoG och Ku80 i kärnan. Enkelmolekylspårning avslöjade dessutom att Ku3 ändrar hur EndoG interagerar med kromatin, vilket stämmer med en direkt fysisk inbromsning av EndoG vid sårbara DNA‑platser.
Från mekanism till framtida terapi
Detta arbete föreslår ett precist sätt att dämpa en farlig biverkning av kemoterapi: en skräddarsydd peptid härledd från ett naturligt reparationsprotein låser fast vid EndoG, förhindrar att det angriper en skör DNA‑hotspot och minskar därigenom risken för leukemogena omarrangemang, samtidigt som det cancerdödande skadliga verkan bibehålls. På sikt skulle sådana peptider — eller förbättrade versioner baserade på samma motiv — kunna ges tillsammans med vanliga genotoxiska läkemedel för att skydda patienters blodbildande celler och minska risken för sekundära leukemier som idag följer i spåren av i övrigt framgångsrik cancerbehandling.
Citering: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Nyckelord: terapirelaterad leukemi, DNA‑brytpoints‑hotspots, endonukleas G, Ku80‑peptid‑inhibitor, kemoterapins biverkningar