Clear Sky Science · pl
Odkrycie inhibującego endonukleazę G peptydu Ku80 chroniącego przed leukemogennymi rekombinacjami w klastrze punktów złamania MLL
Ochrona pacjentów przed ukrytym skutkiem ubocznym
Chemioterapia może ratować życie, ale u niewielkiej liczby pacjentów ma niebezpieczne odległe następstwo: lata po leczeniu rozwijają agresywne nowotwory krwi wywołane uszkodzeniem w małym, podatnym fragmencie DNA. W tym badaniu wyjaśniono, jak naturalny enzym tnący DNA przyczynia się do tych uszkodzeń, oraz przedstawiono mały, zaprojektowany peptyd, który osłania ryzykowny odcinek DNA, nie osłabiając przy tym rakobójczego działania chemioterapii.
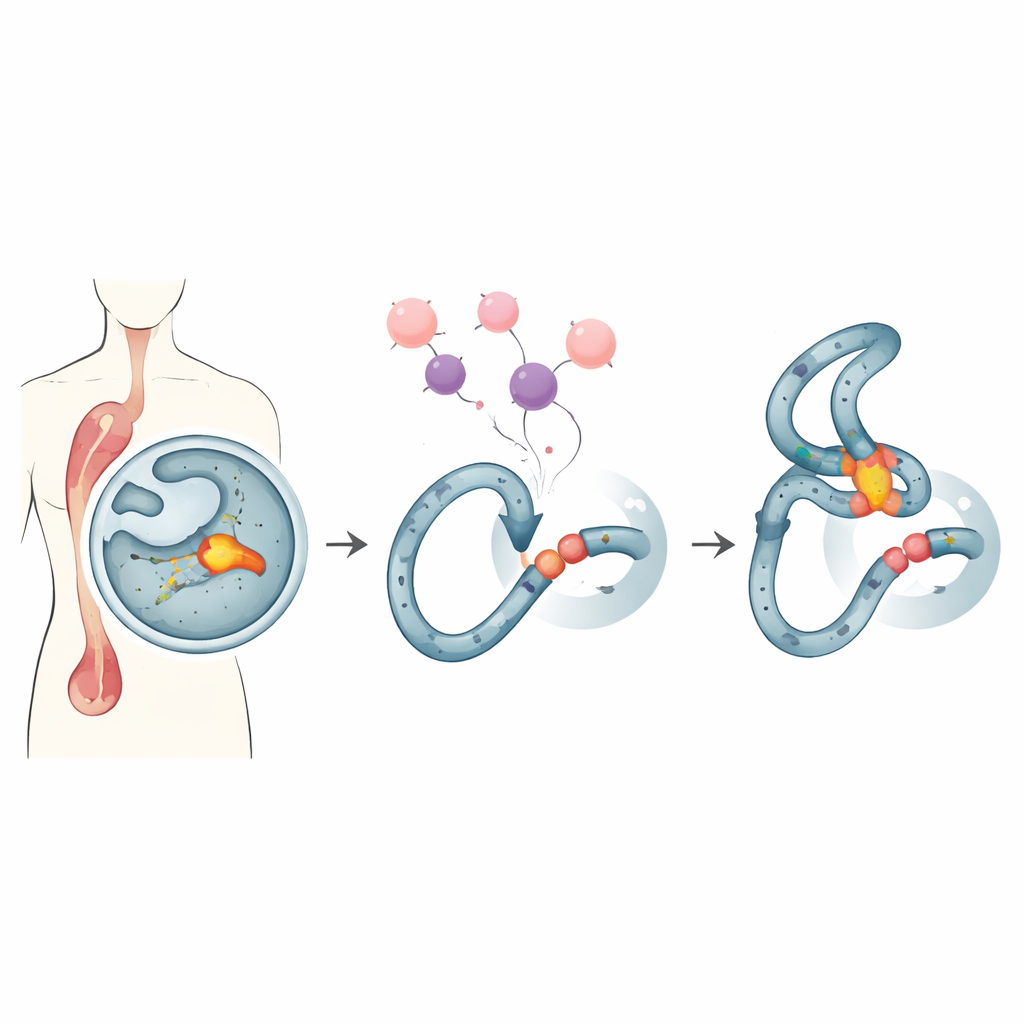
Kruchy punkt w naszych komórkach krwiotwórczych
Niektórzy pacjenci leczeni silnymi lekami przeciwnowotworowymi później rozwijają tzw. białaczkę związaną z terapią — trudny do leczenia nowotwór krwi. W wielu takich przypadkach występuje ten sam znak: pęknięcia i rekombinacje w wąskim gorącym punkcie genu MLL, regionie znanym jako klaster punktów złamania MLL. Ten punkt leży w odcinku DNA, który ma tendencję do przyjmowania nietypowych kształtów i jest szczególnie wrażliwy na niektóre leki. Gdy standardowe terapie, takie jak powszechnie stosowany doksorubicyna, wywołują stres replikacyjny w dzielących się komórkach, ten kruchy region może pękać i nieprawidłowo się łączyć, tworząc sprzyjające rakowi fuzje DNA.
Starożytny enzym staje się czynnikiem ryzyka
Zespół skoncentrował się na endonukleazie G, zwanej EndoG, ewolucyjnie starożytnym enzymie, który zwykle zamieszkuje mitochondria, ale może przemieścić się do jądra komórkowego. EndoG jest znana z rozcinania DNA podczas śmierci komórki, jednak przy niższych, nieśmiercionośnych poziomach potrafi też naciąć genom w sposób sprzyjający mutacjom. Wcześniejsze badania wykazały, że w warunkach stresu replikacyjnego — które wywołują leki takie jak doksorubicyna — EndoG jest rekrutowana do gorącego punktu MLL i pomaga zapoczątkować złamania poprzedzające leukemogenne rekombinacje. Z uwagi na tę dwoistość, naukowcy poszukiwali sposobu, by powstrzymać szkodliwą aktywność EndoG w tym hotspotcie bez blokowania jej użytecznych ról w zabijaniu komórek nowotworowych.
Przekształcenie białka naprawczego w tarczę
U muszek EndoG jest kontrolowana przez naturalne białko inhibitorowe. Nie znano takiego inhibitora u ludzi, ale badacze zauważyli, że część ludzkiego czynnika naprawy DNA o nazwie Ku80 strukturalnie przypomina inhibitor muszki. Ku80 zwykle współpracuje z Ku70, aby zasklepiać przerwane końce DNA, jednak jego luźny ogon wydawał się być zdolny do wiązania EndoG. Za pomocą testów biochemicznych i modelowania strukturalnego autorzy pokazali, że EndoG rzeczywiście przyłącza się do ogona Ku80 oraz że specyficzny fragment Ku80, nazywany domeną C‑terminalną, może fizycznie oddziaływać z EndoG. Gdy wyrazili tylko ten fragment ogona w ludzkich komórkach, częstość rekombinacji przypominających te po terapii w hotspotcie MLL zmniejszyła się o połowę, bez zmiany normalnej naprawy DNA ani przeżywalności komórek po chemioterapii.
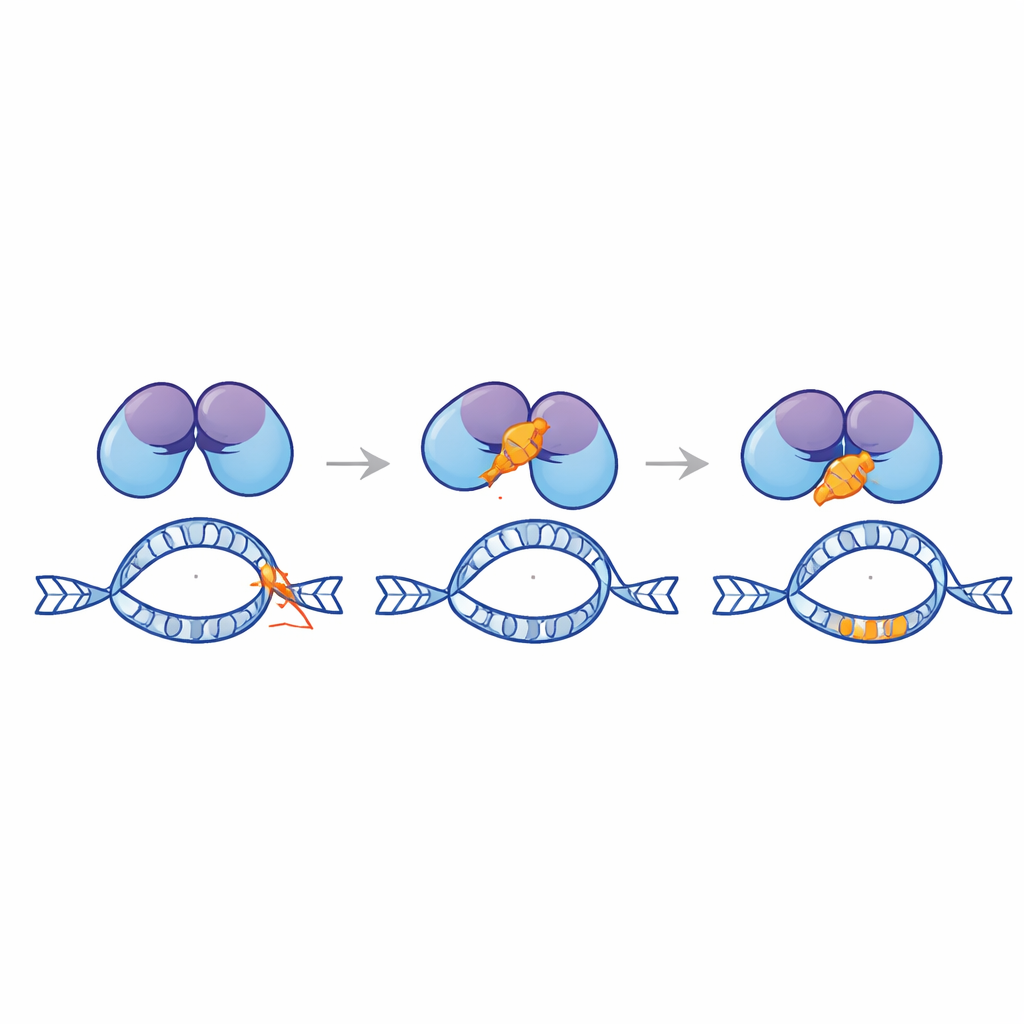
Projektowanie ochronnego peptydu
Kierowani modelowaniem komputerowym, naukowcy pocięli ogon Ku80 na tysiące kandydackich krótkich peptydów i przesiali je pod kątem silnego przewidywanego wiązania z EndoG. Z tej biblioteki wyodrębnili 28‑aminokwasowy peptyd nazwany Ku3, który w symulacjach mocno dokował do EndoG. Gdy Ku3 dostarczono do linii komórkowych białaczki i raka szyjki macicy niosących zkonstruowany reporter MLL, zmniejszył on rekombinacje indukowane doksorubicyną i chronił integralność hotspotu, ponownie bez osłabiania zdolności leku do zabijania komórek. Mikroskopowe testy bliskości pokazały, że Ku3 przerywa tworzenie kompleksów między EndoG a Ku80 w jądrze. Śledzenie pojedynczych cząsteczek ujawniło ponadto, że Ku3 zmienia sposób, w jaki EndoG oddziałuje z chromatyną, co jest zgodne z bezpośrednim fizycznym hamowaniem EndoG w podatnych miejscach DNA.
Od mechanizmu do przyszłej terapii
Ta praca proponuje precyzyjny sposób stłumienia niebezpiecznego skutku ubocznego chemioterapii: szyty na miarę peptyd wywodzący się z naturalnego białka naprawczego przyłącza się do EndoG, zapobiega jej atakom na kruchy hotspot DNA i w ten sposób obniża ryzyko leukemogennych rekombinacji, pozostawiając jednocześnie nietknięty rakobójczy uszkadzający efekt terapii. W dłuższej perspektywie takie peptydy — lub ulepszone wersje oparte na tym samym motywie — mogłyby być podawane łącznie ze standardowymi lekami genotoksycznymi, aby chronić komórki krwiotwórcze pacjentów i zmniejszać ryzyko wtórnych białaczek, które obecnie towarzyszą inaczej skutecznemu leczeniu nowotworów.
Cytowanie: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Słowa kluczowe: białaczka związana z leczeniem, gorące punkty złamań DNA, endonukleaza G, peptyd hamujący Ku80, skutki uboczne chemioterapii