Clear Sky Science · it
Scoperta di un peptide di Ku80 inibitore di Endonuclease G che protegge dalle riarrangiamenti leukemogenici nel cluster di rottura MLL
Proteggere i pazienti da un effetto collaterale nascosto
La chemioterapia può salvare vite, ma per una piccola percentuale di pazienti ha una conseguenza tardiva e pericolosa: anni dopo il trattamento sviluppano tumori del sangue aggressivi innescati da danni in un tratto di DNA particolarmente vulnerabile. Questo studio svela come un enzima naturale che taglia il DNA contribuisca a quel danno e presenta un piccolo peptide progettato che schermia il segmento di DNA a rischio senza indebolire il potere antitumorale della chemioterapia.
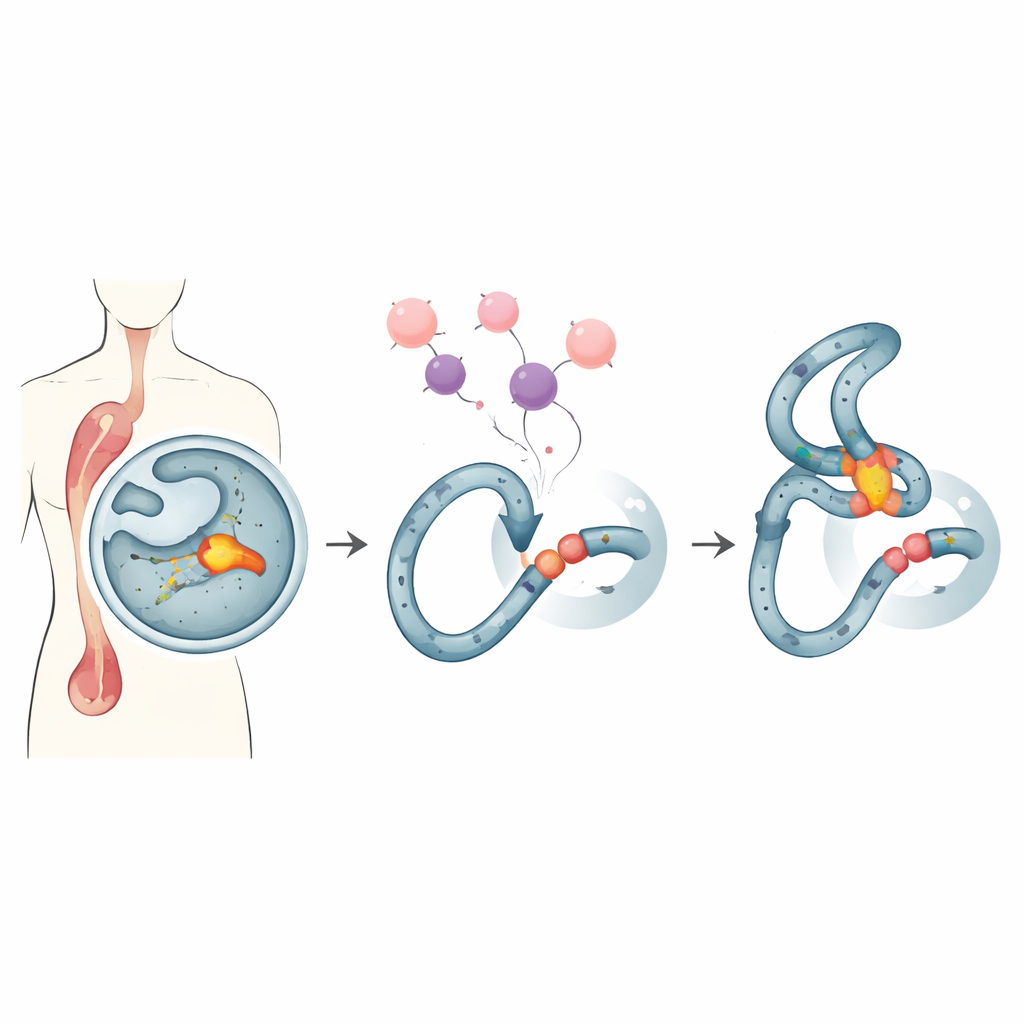
Un punto fragile nelle nostre cellule ematopoietiche
Alcune persone trattate con farmaci antitumorali potenti sviluppano in seguito una leucemia “correlata alla terapia”, un tumore del sangue difficile da trattare. Molti di questi casi condividono lo stesso segno distintivo: rotture e riarrangiamenti in un ristretto punto caldo del gene MLL, una regione nota come cluster di rottura MLL. Questo punto sensibile si trova in un tratto di DNA che tende a formare strutture insolite ed è particolarmente vulnerabile a certi farmaci. Quando trattamenti standard come la doxorubicina, ampiamente utilizzata, sottopongono a stress le cellule in divisione, quella regione fragile può rompersi e riunirsi in modo errato, creando fusioni del DNA che guidano il cancro.
Un enzima antico diventa un fattore di rischio
Il gruppo si concentra su Endonuclease G, o EndoG, un enzima evolutivamente antico che normalmente risiede nei mitocondri ma può spostarsi nel nucleo. EndoG è noto per tagliare il DNA durante la morte cellulare, tuttavia a livelli bassi, non letali, può anche incidere il genoma in modi che favoriscono le mutazioni. Lavori precedenti hanno mostrato che sotto stress da replicazione — condizioni indotte da farmaci come la doxorubicina — EndoG viene reclutato nel punto caldo MLL e contribuisce ad iniziare le rotture che precedono i riarrangiamenti leukemogenici. A causa di questa doppia natura, gli scienziati hanno cercato un modo per limitare l’attività dannosa di EndoG in questo punto senza bloccarne i ruoli utili nell’uccidere le cellule tumorali.
Trasformare una proteina di riparazione in uno scudo
Nei moscerini, EndoG è tenuto sotto controllo da una proteina inibitrice naturale. Un simile inibitore non era noto negli esseri umani, ma i ricercatori notarono che una parte di un fattore umano di riparazione del DNA chiamato Ku80 somiglia strutturalmente all’inibitore dei moscerini. Ku80 solitamente si associa a Ku70 per sigillare gli estremi del DNA spezzato, tuttavia la sua regione terminale flessibile sembrava in grado di legare EndoG. Utilizzando test biochimici e modellazione strutturale, gli autori dimostrarono che EndoG si attacca effettivamente alla coda di Ku80 e che un frammento specifico di Ku80, chiamato dominio C-terminale, può interagire fisicamente con EndoG. Quando hanno espresso solo questo frammento della coda in cellule umane, la frequenza dei riarrangiamenti simili a quelli da terapia nel punto caldo MLL si è dimezzata, senza alterare la riparazione normale del DNA o la sopravvivenza cellulare dopo la chemioterapia.
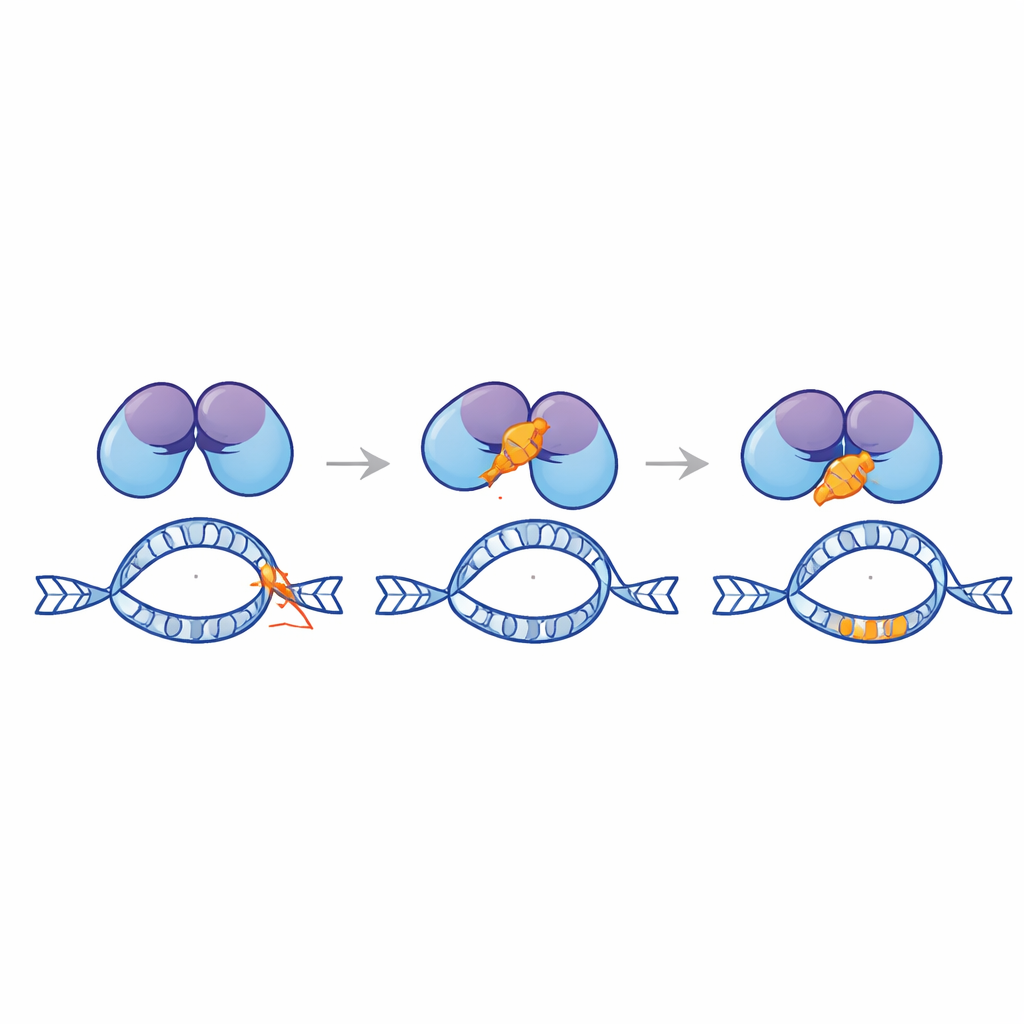
Progettare un peptide protettivo
Guidato dalla modellazione al computer, il team ha sezionato la coda di Ku80 in migliaia di brevi peptide candidati e li ha selezionati per un forte legame predetto con EndoG. Da questa libreria hanno scelto un peptide di 28 amminoacidi, denominato Ku3, che si è ancorato strettamente a EndoG nelle simulazioni. Quando Ku3 è stato introdotto in linee cellulari di leucemia e di cancro cervicale portatrici di un reporter MLL ingegnerizzato, ha ridotto i riarrangiamenti indotti da doxorubicina e ha protetto l’integrità del punto caldo, sempre senza ridurre la capacità del farmaco di uccidere le cellule. Saggi di prossimità basati su microscopia hanno mostrato che Ku3 interrompe la formazione di complessi tra EndoG e Ku80 nel nucleo. Il tracciamento a singola molecola ha rivelato inoltre che Ku3 modifica il modo in cui EndoG interagisce con la cromatina, coerente con un freno fisico diretto su EndoG nei siti di DNA vulnerabili.
Dal meccanismo alla terapia futura
Questo lavoro propone un modo preciso per attenuare un pericoloso effetto collaterale della chemioterapia: un peptide su misura derivato da una proteina di riparazione naturale si lega a EndoG, gli impedisce di attaccare un punto fragile del DNA e così riduce la probabilità di riarrangiamenti leukemogenici, mantenendo intatto il danno che elimina il tumore. A lungo termine, tali peptide — o versioni migliorate basate sullo stesso motivo — potrebbero essere co‑somministrati con i comuni farmaci genotossici per proteggere le cellule ematopoietiche dei pazienti e ridurre il rischio di leucemie secondarie che oggi possono oscurare il successo del trattamento antitumorale.
Citazione: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Parole chiave: leucemia correlata alla terapia, punti caldi di rottura del DNA, endonucleasi G, peptide inibitore di Ku80, effetti collaterali della chemioterapia