Clear Sky Science · fr
Découverte d’un peptide de Ku80 inhibiteur de l’endonucléase G protégeant contre les réarrangements leucémiques au cluster de cassures MLL
Protéger les patients d’un effet secondaire caché
La chimiothérapie peut sauver des vies, mais pour un petit nombre de patients elle entraîne une conséquence tardive dangereuse : des années après le traitement, ils développent des cancers sanguins agressifs déclenchés par des lésions à un court segment d’ADN vulnérable. Cette étude révèle comment une enzyme naturelle coupant l’ADN contribue à ces dommages et présente un petit peptide conçu qui protège ce segment d’ADN à risque sans affaiblir le pouvoir cytotoxique de la chimiothérapie.
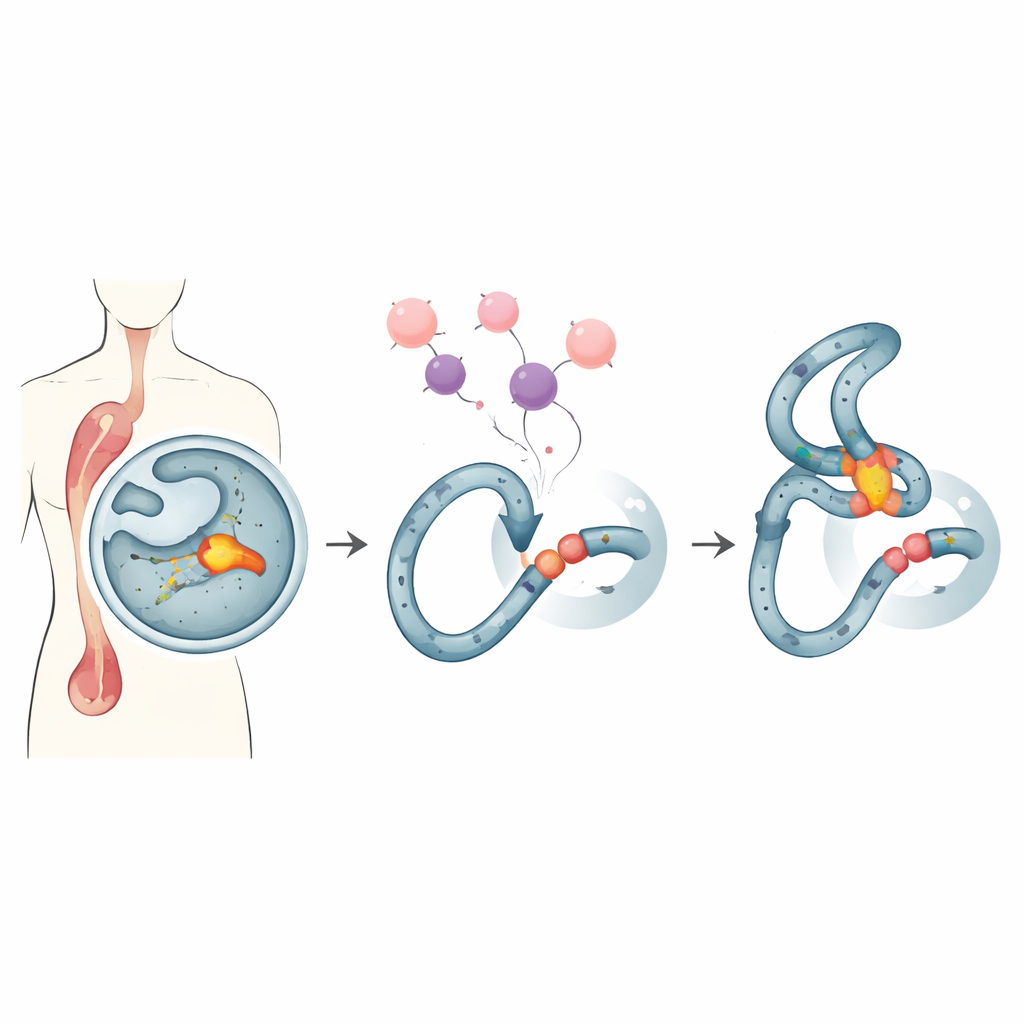
Un point fragile dans nos cellules hématopoïétiques
Certaines personnes traitées par des médicaments anticancéreux puissants développent plus tard une leucémie « liée au traitement », un cancer du sang difficile à soigner. Nombre de ces cas partagent la même signature : des cassures et des réarrangements dans une zone étroite du gène MLL, une région connue sous le nom de cluster de cassures MLL. Ce point chaud se situe dans une portion d’ADN qui tend à adopter des conformations inhabituelles et est particulièrement sensible à certains médicaments. Lorsque des traitements standards, comme le doxorubicine largement utilisé, mettent en tension les cellules en division, cette région fragile peut se fissurer et se recoller de manière erronée, créant des fusions d’ADN promotrices de cancer.
Une enzyme ancestrale devient un facteur de risque
L’équipe se concentre sur l’endonucléase G, ou EndoG, une enzyme évolutivement ancienne qui réside normalement dans les mitochondries mais peut migrer vers le noyau. EndoG est connue pour cliver l’ADN lors de la mort cellulaire, mais à des niveaux plus faibles, non létaux, elle peut aussi entailler le génome d’une façon qui favorise les mutations. Des travaux antérieurs ont montré que sous stress de réplication — conditions créées par des médicaments comme le doxorubicine — EndoG est recrutée au point chaud MLL et contribue à initier les cassures qui précèdent les réarrangements leucémiques. En raison de cette double nature, les chercheurs ont cherché à limiter l’activité néfaste d’EndoG sur ce point chaud sans bloquer ses rôles utiles dans l’élimination des cellules cancéreuses.
Transformer une protéine de réparation en bouclier
Chez la drosophile, EndoG est régulée par une protéine inhibitrice naturelle. Aucun inhibiteur de ce type n’était connu chez l’humain, mais les chercheurs ont remarqué qu’une partie d’un facteur de réparation de l’ADN humain appelé Ku80 ressemble structurellement à l’inhibiteur de la mouche. Ku80 s’associe habituellement à Ku70 pour sceller les extrémités d’ADN cassées, mais sa région terminale flexible semblait capable de lier EndoG. Grâce à des tests biochimiques et à la modélisation structurale, les auteurs ont montré qu’EndoG se fixe effectivement à la queue de Ku80 et qu’un segment spécifique de Ku80, appelé domaine C‑terminal, peut interagir physiquement avec EndoG. Lorsqu’ils ont exprimé uniquement ce fragment de queue dans des cellules humaines, la fréquence des réarrangements de type thérapeutique au point chaud MLL a été réduite de moitié, sans altérer la réparation normale de l’ADN ni la survie cellulaire après chimiothérapie.
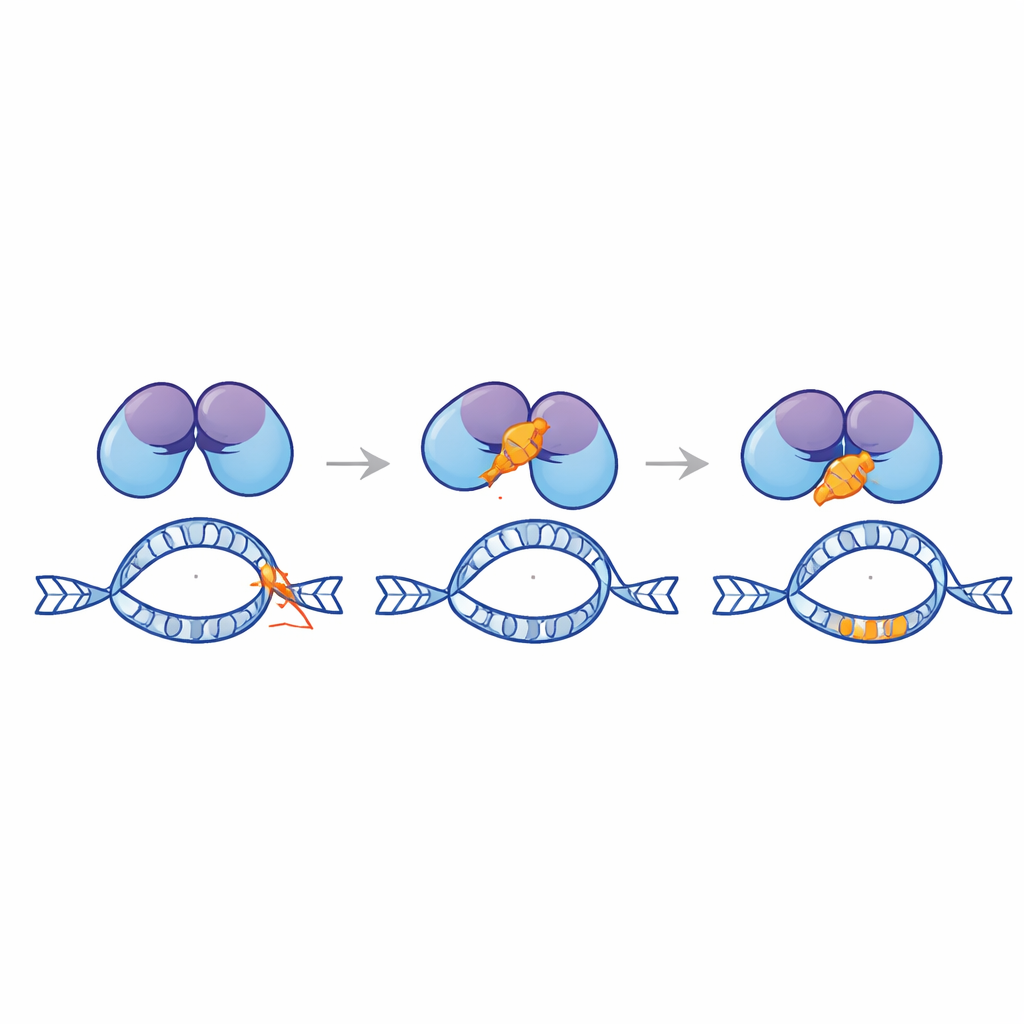
Conception d’un peptide protecteur
Guidée par la modélisation informatique, l’équipe a découpé la queue de Ku80 en milliers de peptides candidats courts et les a dépistés pour leur affinité prédite envers EndoG. De cette bibliothèque, ils ont isolé un peptide de 28 acides aminés, nommé Ku3, qui s’est fortement arrimé à EndoG dans les simulations. Lorsqu’il a été délivré dans des lignées cellulaires de leucémie et de cancer du col porteuses d’un rapporteur MLL artificiel, Ku3 a réduit les réarrangements induits par la doxorubicine et a préservé l’intégrité du point chaud, là encore sans diminuer la capacité du médicament à tuer les cellules. Des essais de proximité basés sur la microscopie ont montré que Ku3 perturbe la formation de complexes entre EndoG et Ku80 dans le noyau. Le suivi de molécules uniques a en outre révélé que Ku3 modifie la façon dont EndoG interagit avec la chromatine, cohérent avec un frein physique direct exercé par Ku3 sur EndoG aux sites d’ADN vulnérables.
Du mécanisme à une thérapie future
Ce travail propose un moyen précis d’atténuer un effet secondaire dangereux de la chimiothérapie : un peptide sur mesure dérivé d’une protéine de réparation naturelle se fixe sur EndoG, l’empêche d’attaquer un point chaud d’ADN fragile et réduit ainsi la probabilité de réarrangements leucémiques, tout en préservant les dommages létaux contre la tumeur. À long terme, de tels peptides — ou des versions améliorées basées sur le même motif — pourraient être coadministrés avec des médicaments génotoxiques standards pour protéger les cellules hématopoïétiques des patients et réduire le risque de leucémies secondaires qui, aujourd’hui, assombrissent des traitements anticancéreux autrement efficaces.
Citation: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Mots-clés: leucémie liée au traitement, points chauds de cassures d’ADN, endonucléase G, inhibiteur peptidique Ku80, effets secondaires de la chimiothérapie