Clear Sky Science · de
Entdeckung eines Endonuclease‑G‑hemmenden Ku80‑Peptids, das vor leukämieauslösenden Umlagerungen an der MLL‑Bruchpunkt‑Region schützt
Patienten vor einer verborgenen Nebenwirkung schützen
Chemotherapie kann Leben retten, doch bei einer kleinen Zahl von Patientinnen und Patienten hat sie eine gefährliche Spätfolge: Jahre nach der Behandlung entwickeln sie aggressive Blutkrebserkrankungen, ausgelöst durch Schäden an einer winzigen, besonders anfälligen DNA‑Region. Diese Studie zeigt, wie ein natürlicher DNA‑schneidender Enzymtyp zu diesen Schäden beiträgt, und stellt ein kleines, entworfenes Peptid vor, das das riskante DNA‑Segment abschirmt, ohne die krebsbekämpfende Wirkung der Chemotherapie zu schwächen.
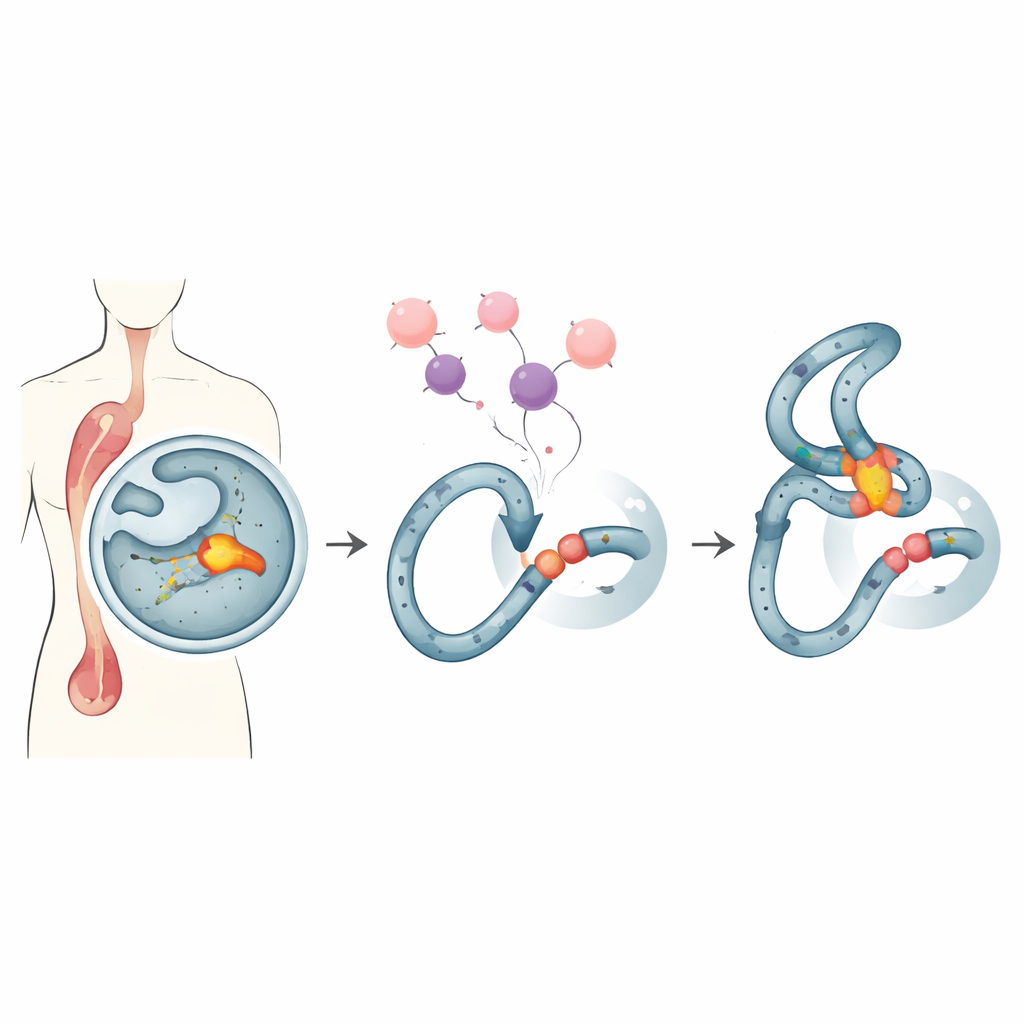
Eine fragile Stelle in unseren blutbildenden Zellen
Bei einigen Personen, die mit starken Krebsmedikamenten behandelt wurden, tritt später eine „therapie‑assoziierte“ Leukämie auf, eine schwer behandelbare Form von Blutkrebs. Viele dieser Fälle weisen dasselbe Kennzeichen auf: Brüche und Umlagerungen in einem engen Hotspot des MLL‑Gens, einer Region, die als MLL‑Bruchpunkt‑Cluster bekannt ist. Dieser Hotspot liegt in einer DNA‑Sequenz, die dazu neigt, ungewöhnliche Strukturen zu bilden und besonders empfindlich gegenüber bestimmten Arzneimitteln zu sein. Wenn Standardbehandlungen wie das weitverbreitete Doxorubicin sich teilende Zellen belasten, kann diese fragile Region aufbrechen und fehlerhaft wieder zusammengefügt werden, wodurch krebsfördernde DNA‑Fusionen entstehen.
Ein uraltes Enzym wird zum Risikofaktor
Die Gruppe konzentriert sich auf Endonuclease G, kurz EndoG, ein evolutionär altes Enzym, das normalerweise in Mitochondrien sitzt, aber in den Zellkern wandern kann. EndoG ist bekannt dafür, DNA während des Zelltods zu zerschneiden, doch in niedrigeren, nicht tödlichen Konzentrationen kann es das Genom auch so ritzen, dass Mutationen begünstigt werden. Frühere Arbeiten zeigten, dass unter Replikationsstress — Bedingungen, die durch Medikamente wie Doxorubicin entstehen — EndoG an den MLL‑Hotspot rekrutiert wird und dort die Brüche einleitet, die leukämieauslösende Umlagerungen vorausgehen. Wegen dieser Doppelrolle suchten Forschende nach einem Weg, EndoG‑schädliche Aktivität an diesem Hotspot zu dämpfen, ohne seine nützlichen Funktionen beim Abtöten von Krebszellen zu blockieren.
Ein Reparaturprotein wird zum Schutzschild
Bei Fruchtfliegen wird EndoG von einem natürlichen Inhibitor in Schach gehalten. Ein solcher Inhibitor war beim Menschen nicht bekannt, doch die Forschenden bemerkten, dass ein Teil eines menschlichen DNA‑Reparaturfaktors namens Ku80 strukturell dem Fliegeninhibitor ähnelt. Ku80 arbeitet normalerweise mit Ku70 zusammen, um gebrochene DNA‑Enden zu verschließen, doch seine flexible Schwanzregion schien in der Lage, an EndoG zu binden. Mithilfe biochemischer Tests und Strukturmodellierung zeigten die Autorinnen und Autoren, dass EndoG tatsächlich an Ku80s Schwanz anbindet und dass ein spezifischer Abschnitt von Ku80, die C‑terminale Domäne, physisch mit EndoG interagieren kann. Wenn sie nur dieses Schwanzfragment in menschlichen Zellen exprimierten, halbierte sich die Häufigkeit therapieähnlicher Umlagerungen am MLL‑Hotspot, ohne die normale DNA‑Reparatur oder das Überleben der Zellen nach Chemotherapie zu verändern.
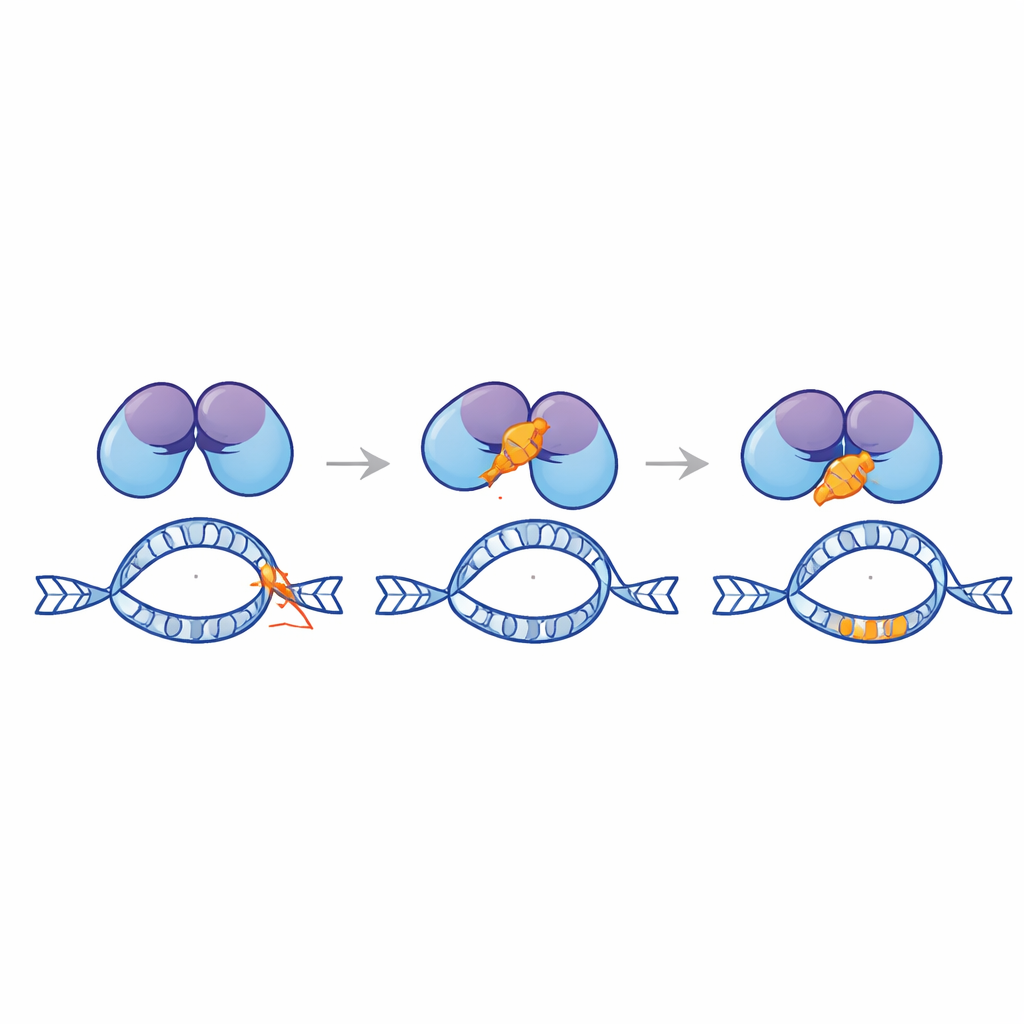
Entwicklung eines schützenden Peptids
Geleitet von Computer‑Modellen schnitt das Team Ku80s Schwanz in Tausende möglicher kurzer Peptide und testete sie daraufhin auf starke vorhergesagte Bindung an EndoG. Aus dieser Bibliothek wählten sie ein 28‑Aminosäure‑Peptid aus, genannt Ku3, das in Simulationen eng an EndoG andockte. Als Ku3 in Leukämie‑ und Gebärmutterhalskrebs‑Zelllinien mit einem konstruierten MLL‑Reporter eingebracht wurde, verringerte es Doxorubicin‑induzierte Umlagerungen und schützte die Integrität des Hotspots, wiederum ohne die zytotoxische Wirkung des Medikaments zu mindern. Mikroskopische Proximitätsassays zeigten, dass Ku3 die Bildung von Komplexen zwischen EndoG und Ku80 im Zellkern stört. Einzelmolekül‑Tracking offenbarte zudem, dass Ku3 verändert, wie EndoG mit der Chromatinstruktur interagiert, was zu einem direkten physischen Bremsmechanismus von EndoG an vulnerablen DNA‑Stellen passt.
Vom Mechanismus zur zukünftigen Therapie
Die Arbeit schlägt einen präzisen Weg vor, eine gefährliche Nebenwirkung der Chemotherapie abzumildern: Ein maßgeschneidertes Peptid, abgeleitet von einem natürlichen Reparaturprotein, bindet an EndoG, hindert es daran, eine fragile DNA‑Hotspot‑Region anzugreifen, und senkt so die Wahrscheinlichkeit leukämieauslösender Umlagerungen, während die krebszerstörenden Effekte erhalten bleiben. Langfristig könnten solche Peptide — oder verbesserte Varianten auf Basis desselben Motivs — zusammen mit standardmäßigen genotoxischen Medikamenten verabreicht werden, um die blutbildenden Zellen der Patientinnen und Patienten zu schützen und das Risiko sekundärer Leukämien zu verringern, das derzeit erfolgreiche Krebsbehandlungen überschattet.
Zitation: Eberle, J., Salem, A., Hofmann, M. et al. Discovery of an Endonuclease G-inhibitory Ku80-peptide protecting against leukemogenic rearrangements at the MLL breakpoint cluster. Nat Commun 17, 3562 (2026). https://doi.org/10.1038/s41467-026-72034-2
Schlüsselwörter: therapiebedingte Leukämie, DNA‑Bruch‑Hotspots, Endonuclease G, Ku80‑Peptid‑Inhibitor, Nebenwirkungen der Chemotherapie