Clear Sky Science · zh
细胞外 K+ 调节 Cys-loop 受体阴离子通道的孔道构象
细胞如何“听见”外部的钾
我们体内的每一次思考、运动和心跳都依赖于带电的微小原子——离子——穿过细胞膜的流动。钾是这些离子中最重要的之一,神经细胞外的钾浓度被严格维持在极窄的范围内。本研究揭示了大脑细胞直接感知细胞外钾变化并将其转化为氯离子通量变化的一种出人意料的途径。该工作发现了一个隐藏在一类神经受体中的感受机制,并提示大脑可能以新方式监测并响应其化学环境。
一种新的钾传感器
迄今为止,动物中已知的大多数钾传感器是把钾作为燃料或货物使用的通道和泵,而不是作为独立信号的受体。作者把注意力集中在果蝇(Drosophila)中一个研究较少的蛋白质 DmAlka 上,它属于 Cys-loop 受体家族。该家族成员通常在结合神经递质时形成开放通道,允许氯离子通过膜以抑制电活动。令人惊讶的是,早期工作表明 DmAlka 并不对常见递质甘氨酸产生反应,而是在碱性条件下被激活。在这里,研究人员展示了 DmAlka 对细胞外正常范围内的钾浓度也具有精细的调谐作用,并且这种调谐强烈影响通道中氯离子的流动。
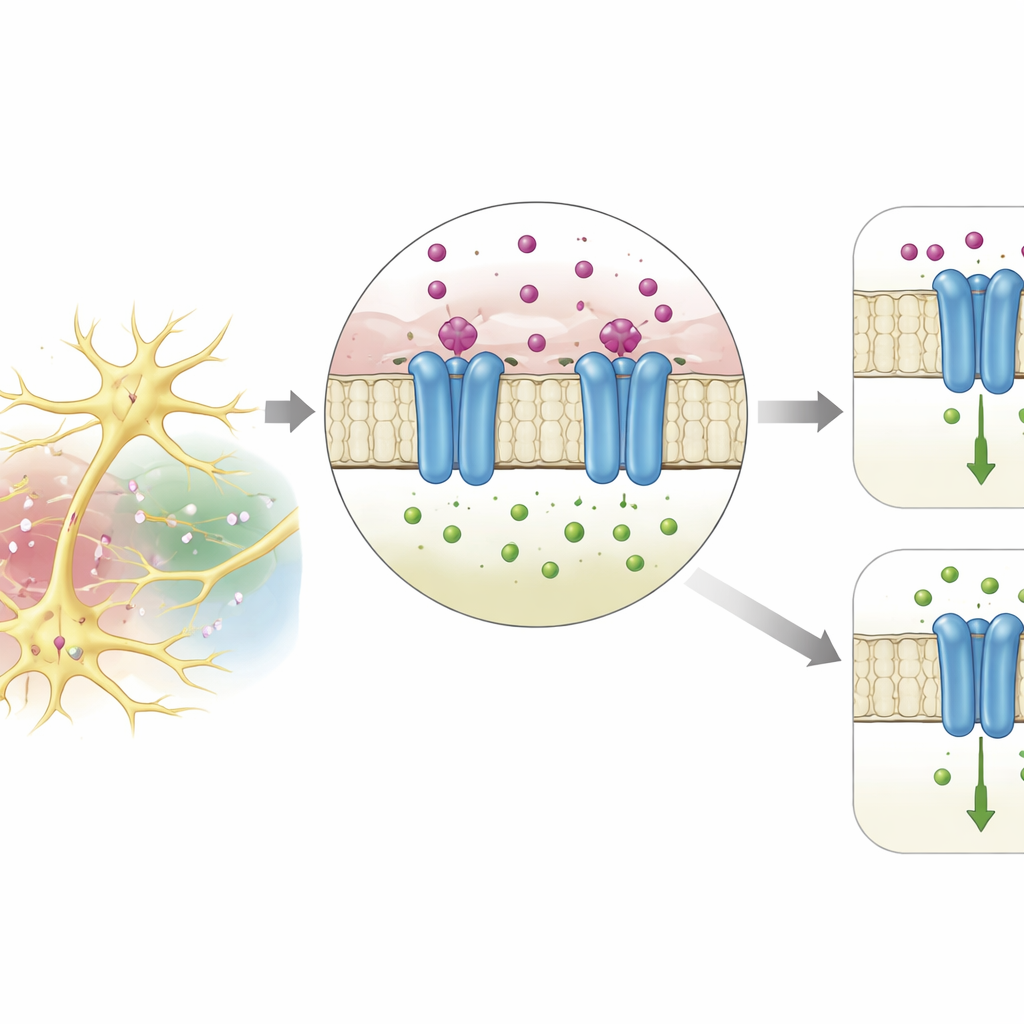
钾在哪里抓住通道
研究团队使用强大的结构预测程序对 DmAlka 的三维形状进行了建模。模型揭示了位于蛋白质外侧信号感受区与穿膜离子通道交界处的一个小口袋。在这个口袋中,一个钾离子被来自附近氨基酸的四个氧原子环抱,其排列方式很像经典钾通道或溶液中水分子对钾的配位方式。通过改变构成该口袋的单个残基,研究者能够削弱或消除通道对钾的敏感性,从而证实该位点是关键的停靠位置。在多种节肢动物的相关蛋白中也发现了相似结构,表明这种钾识别策略在无脊椎动物中被广泛保守。
两种模式,由钾切换
在能作为微型表达工厂的蛙卵中进行的电生理实验显示,DmAlka 的行为类似一个具有两种模式的开关。当细胞外钾浓度较低时,通道更容易保持开放,对碱性条件的反应不同,并且随时间去敏化较少。在这种模式下,孔道相对宽松:它优先通透氯离子,但也允许诸如碳酸氢根等其他阴离子更自由地通过,并且对某些药物阻塞的敏感性降低。当钾在其特定位点结合时,整个蛋白发生细微位移。孔道变窄并对氯离子更具选择性,对其他阴离子的传导能力下降,同时对孔阻断分子的反应增强。实质上,细胞外钾在一种灵活、广谱通透的状态与一种更紧致、更专向氯离子的状态之间切换通道。
在人类大脑中的回声
耐人寻味的是,同样的总体机制在人类中至少以潜在形式存在。人类的一种甘氨酸受体亚型 GlyR α2 通常响应甘氨酸而非钾。通过将 DmAlka 钾口袋的关键特征移植到人类受体中,作者构建了一个获得钾敏感性的突变体:高外部钾在没有甘氨酸存在的情况下也能增强基线电流。他们还显示,某些与癫痫相关的大脑变化相关的人类 GlyR α2 的天然变体也可以获得对钾的响应。在这些人类受体中,正如在 DmAlka 中一样,钾的结合会改变孔的性质,改变氯和碳酸氢根的通透性以及某些阻断剂的作用效果。
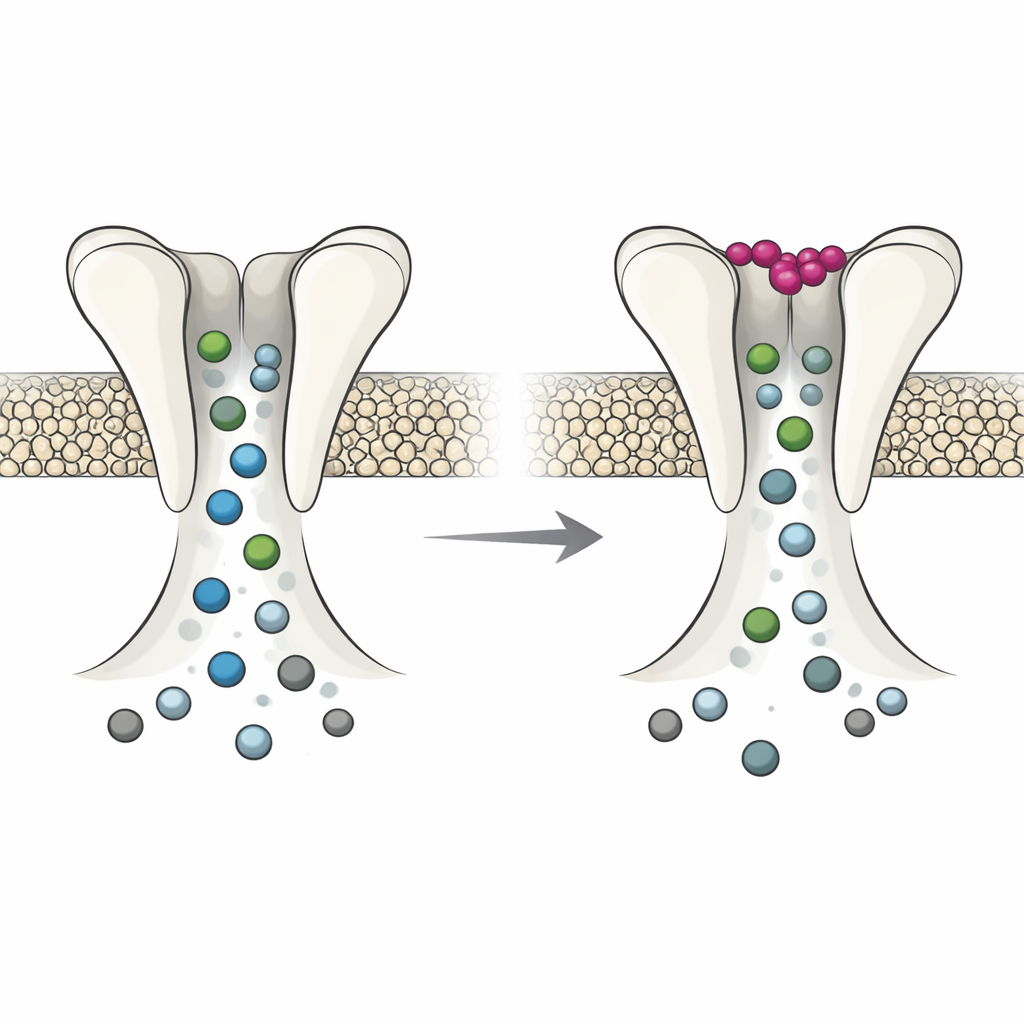
这对大脑健康意味着什么
果蝇版本的这种通道在胶质细胞中富集,胶质细胞是帮助维持神经元周围钾平衡和 pH 的支持细胞。新发现的机制提出了一个简单逻辑:当细胞外钾下降时,DmAlka 以一种允许更多氯进入胶质细胞且更多碳酸氢根离开细胞的方式开放,可能有助于恢复周围空间的钾浓度和酸碱度。在人类中,甘氨酸受体中类似的钾调谐行为在极端情况下(如中风或癫痫发作期间,神经元外的钾可能飙升至远高于正常水平时)可能变得重要。总体而言,这项工作表明部分 Cys-loop 受体并非只是对神经递质的被动响应者;它们也可以作为离子环境的直接传感器,将细胞外钾的变化与跨物种的氯信号调节连接起来。
引用: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
关键词: 细胞外钾感知, 氯离子通道, Cys-loop 受体, 甘氨酸受体变体, 胶质细胞离子稳态