Clear Sky Science · nl
Extracellulair K+ moduleren de porieconformaties van Cys-loop receptor anionkanalen
Hoe cellen naar kalium buiten luisteren
Elke gedachte, beweging en hartslag in ons lichaam berust op het verplaatsen van kleine geladen deeltjes, of ionen, over celmembranen. Kalium is een van de belangrijkste van deze ionen en de concentratie ervan buiten zenuwcellen wordt binnen een zeer nauwe marge gehouden. Deze studie onthult een onverwachte manier waarop hersencellen direct veranderingen in extracellulair kalium kunnen waarnemen en die kunnen omzetten in veranderingen in de stroom van chloride, een ander cruciaal ion. Het werk maakt een verborgen detectiemechanisme zichtbaar in een familie van zenuwreceptoren en suggereert nieuwe manieren waarop de hersenen hun chemische omgeving kunnen monitoren en daarop reageren.
Een nieuw soort kaliumsensor
Tot nu toe waren de bekendste kaliumdetectoren bij dieren vooral kanalen en pompen die kalium gebruiken als brandstof of lading, niet als een signaal op zich. De auteurs richtten zich op een weinig bestudeid eiwit in de fruitvlieg Drosophila, DmAlka genoemd, dat tot de Cys-loop receptorfamilie behoort. Leden van deze familie vormen doorgaans kanalen die openen wanneer ze neurotransmitters binden en vervolgens chloride-ionen doorlaten om elektrische activiteit te dempen. Verrassend genoeg bleek eerder dat DmAlka niet reageert op de gebruikelijke neurotransmitter glycine maar geactiveerd wordt door alkalische (basische) omstandigheden. Hier tonen de onderzoekers aan dat DmAlka ook fijn is afgestemd op het normale bereik van kaliumconcentraties buiten cellen, en dat deze afstemming sterk bepaalt hoe chloride door het kanaal stroomt.
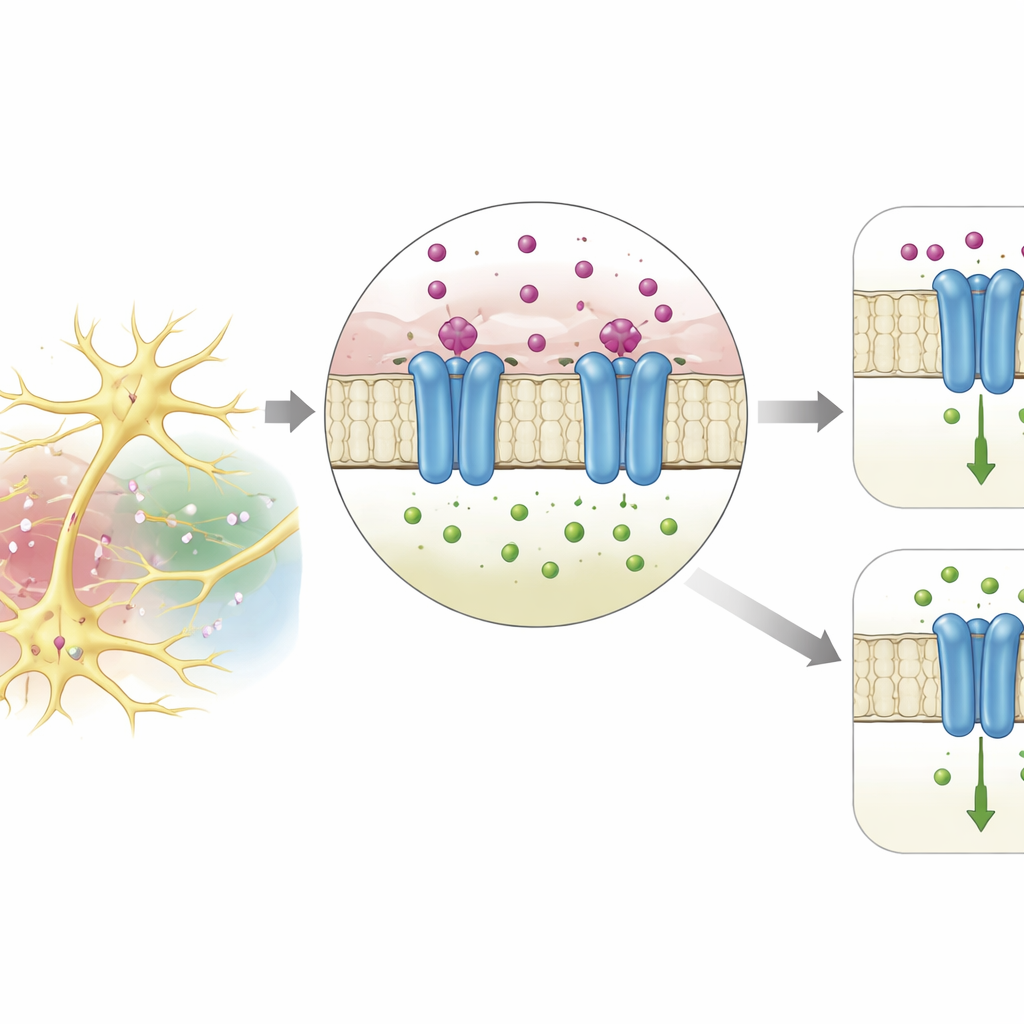
Waar kalium grijpt
Met behulp van een krachtig structuurvoorspellingsprogramma modelleerde het team de driedimensionale vorm van DmAlka. Het model toonde een kleine pocket op de overgang tussen het buitenste, signaaldecterende deel van het eiwit en de membraanverhangende porie die ionen geleidt. In deze pocket wordt een kaliumion omarmd door vier zuurstofatomen van nabijgelegen aminozuren, in een rangschikking die nauw lijkt op hoe kalium wordt vastgehouden in klassieke kaliumkanalen of door watermoleculen in oplossing. Door individuele bouwstenen die deze pocket mede vormen te veranderen, konden de onderzoekers de gevoeligheid van het kanaal voor kalium verzwakken of uitschakelen, waarmee ze bevestigden dat deze plaats de sleutel-dockingsplek is. Vergelijkbare kenmerken werden gevonden in verwante eiwitten bij veel geleedpotige soorten, wat suggereert dat deze kaliumherkenningsstrategie breed bewaard is gebleven bij ongewervelden.
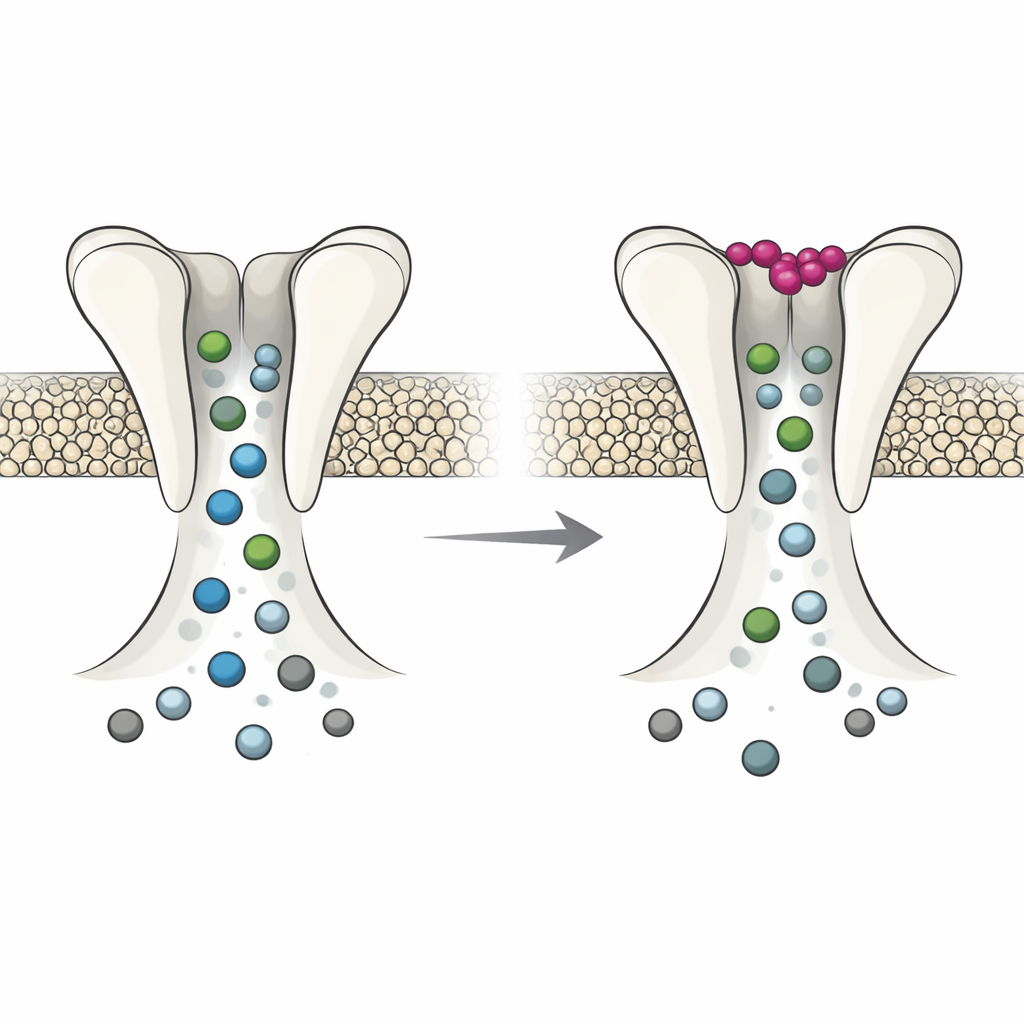
Twee modi, geschakeld door kalium
Elektrofysiologische experimenten in kikkereieren, die kunnen dienen als kleine fabrieken om kanalen te produceren, lieten zien dat DmAlka zich gedraagt als een schakelaar met twee modi. Wanneer extracellulair kalium laag is, blijft het kanaal eerder open, reageert het anders op basische omstandigheden en raakt het minder snel gedesensitiseerd in de tijd. In deze modus is de porie relatief ruim: hij bevoordeelt chloride maar laat ook andere negatieve ionen, zoals bicarbonaat, vrijer passeren, en wordt hij minder gevoelig voor blokkade door bepaalde geneesmiddelen. Wanneer kalium op zijn speciale plaats bindt, verschuift het hele eiwit subtiel. De porie vernauwt en wordt selectiever voor chloride, geleidt andere anionen minder goed en vertoont een sterkere respons op porie-blokkerende moleculen. Effectief schakelt extracellulair kalium het kanaal tussen een flexibele, breed permeabele toestand en een strakkere, meer op chloride gerichte toestand.
Weerklank in het menselijk brein
Intrigerend genoeg lijkt hetzelfde algemene mechanisme, althans in latente vorm, ook bij mensen voor te komen. Een menselijke subtype van de glycine-receptor, GlyR α2, reageert normaal op de neurotransmitter glycine en niet op kalium. Door sleutelkenmerken van de DmAlka-kaliumpocket in de menselijke receptor in te bouwen, creëerden de auteurs een mutant die kaliumgevoeligheid verwierf: hoge extracellulaire kalium verhoogde de basaalstroom zelfs zonder aanwezigheid van glycine. Ze toonden ook aan dat van nature voorkomende menselijke varianten van GlyR α2, sommige geassocieerd met epilepsie-gerelateerde veranderingen in de hersenen, kaliumresponsiviteit kunnen krijgen. In deze menselijke receptoren, net als in DmAlka, verschuift kaliumbinding de porie-eigenschappen, waardoor verandert hoe gemakkelijk chloride en bicarbonaat passeren en hoe effectief bepaalde blokkers zijn.
Waarom dit belangrijk is voor de gezondheid van de hersenen
De fruitvliegversie van dit kanaal is verrijkt in gliacellen, de ondersteunende cellen die helpen het kalium- en pH-evenwicht rond neuronen te behouden. Het nieuw onthulde mechanisme suggereert een eenvoudige logica: wanneer extracellulair kalium daalt, opent DmAlka op een manier die meer chloride in glia laat en meer bicarbonaat naar buiten laat, wat mogelijk helpt zowel de kaliumconcentratie als de zuurgraad in de omgeving te herstellen. Bij mensen kan soortgelijk kalium-gevoelig gedrag in glycine-receptoren belangrijk worden onder extreme omstandigheden, zoals bij een beroerte of epileptische aanvallen, wanneer extracellulair kalium ver boven normaal kan stijgen. Al met al laat dit werk zien dat sommige Cys-loop receptoren niet alleen passieve ontvangers van neurotransmitters zijn; ze kunnen ook directer sensoren van de ionische omgeving zijn en zo veranderingen in extracellulair kalium koppelen aan verschuivingen in chloride-signaalgeving tussen soorten.
Bronvermelding: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Trefwoorden: extracellulaire kaliumdetectie, chloridekanalen, Cys-loop receptoren, glycine-receptorvarianten, ionhomeostase in gliacellen